Servizi di conformità, audit e convalida - Panoramica
Siete conformi? Si tratta di una domanda alla quale qualsiasi azienda operante nei settori farmaceutico, biotecnologico, genomico, chimico, dei dispositivi medici e della gestione della catena di approvvigionamento fatica a rispondere. Queste organizzazioni devono rispettare rigorosi requisiti di qualità, sicurezza e conformità in ogni area geografica in cui vengono distribuiti i loro prodotti. L'attuale tendenza nella gestione della conformità normativa si sta orientando verso l'armonizzazione globale della qualità e della sicurezza, ponendo l'accento su pratiche solide. Che siate produttori o fornitori, l'espansione del vostro mercato, il miglioramento continuo e la soddisfazione dei clienti dipendono principalmente dagli standard di qualità della vostra attività. Il Centro di eccellenza (CoE) per la conformità normativa, l'audit e la convalida di Freyr può aiutarvi in questo sforzo, fornendovi servizi professionali di conformità, audit e convalida per i settori farmaceutico, dei dispositivi medici, dei beni di consumo e sanitario, quali cGMP (Buone Pratiche di Fabbricazione), GCP Buone Pratiche Cliniche), GDP Buone Pratiche di Distribuzione), Buone Pratiche di Laboratorio (GLP), GPVP Buone Pratiche di Farmacovigilanza) eValidazione dei Sistemi Informatici GxP (CSV). Il nostro team di consulenza in materia di conformità farmaceutica fornisce soluzioni su misura per affrontare le vostre sfide specifiche in materia di conformità.
Freyr offre servizi di conformità normativa, audit e convalida che comprendono la valutazione delle vostre esigenze e la formulazione di suggerimenti sui processi aziendali, con l’obiettivo di garantire la soddisfazione del cliente. Grazie alla nostra preparazione di rapporti di audit di conformità e alle nostre strategie di preparazione, forniamo rapporti di conformità e di audit (analisi delle lacune), comprese le azioni correttive e preventive (CAPA) suggerite per evitare potenziali 483 e rilievi di non conformità da parte delle autorità di regolamentazione. La consulenza di Freyr in materia di conformità farmaceutica si estende anche alla consulenza sulla conformità dell'automazione farmaceutica, garantendo che i vostri sistemi automatizzati soddisfino le aspettative normative in continua evoluzione. Il nostro approccio globale alla gestione della conformità garantisce che ogni fase del ciclo di vita del vostro processo sia monitorata e ottimizzata per l'allineamento normativo.
Forniamo servizi di conformità normativa e convalida per garantire che tutti i vostri processi e prodotti siano conformi ai requisiti applicabili in materia di qualità, sicurezza delle informazioni e audit di conformità normativa, quali (a titolo esemplificativo ma non esaustivo) i seguenti:
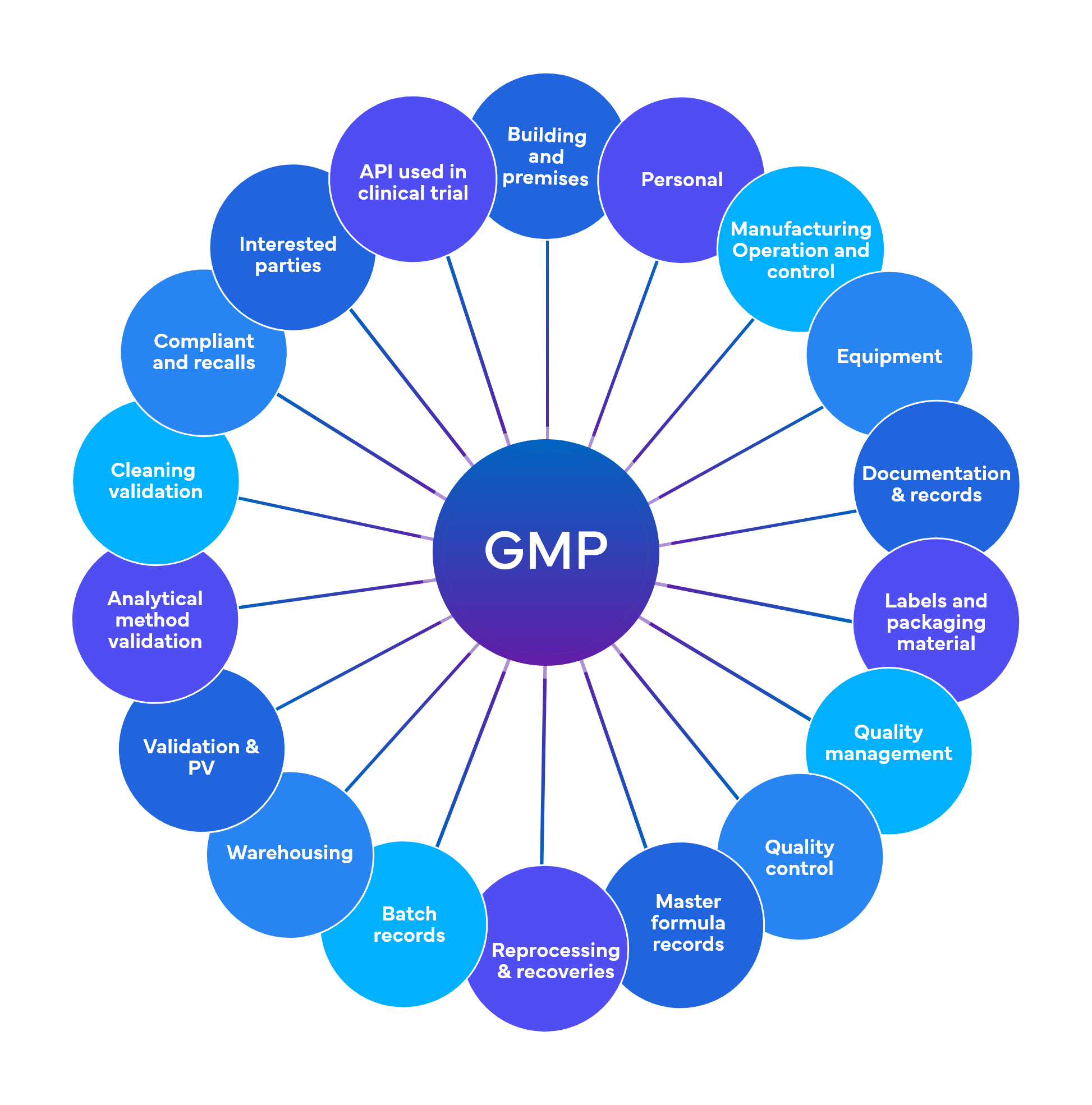
Freyr esegue circa 700 controlli a livello preliminare distribuiti in 18-19 aree funzionali GMP
Conformità, Audit e Validazione di Freyr
Servizi di conformità, audit e convalida
Qualità e conformità normativa – Attuali Norme di Buona Fabbricazione (cGMP)
- ISO / IEC 17025: 2017 - Requisiti generali per la competenza dei laboratori di prova e taratura
- OCSE (Organizzazione per la Cooperazione e lo Sviluppo Economico) - Linee guida di Buona Pratica di Laboratorio
- Guida EURACHEM / CITAC: Guida alla qualità in chimica analitica - Un aiuto per l'accreditamento, 3a edizione (2016), dovrebbe essere seguita nelle procedure analitiche.
- 21 CFR 58: Buone pratiche di laboratorio per studi di laboratorio non clinici
- Guida ai Regolamenti GLP del Regno Unito, Febbraio 2000 (a cura di GLPMA)
- Manuale dell'WHO sulle buone pratiche di laboratorio (GLP): pratiche di qualità per la ricerca e lo sviluppo non clinico regolamentato
- Health Canada: Documento guida finalizzato - Dati di studi di laboratorio non clinici a supporto delle domande e delle presentazioni di prodotti farmaceutici: Adesione alle Buone Pratiche di Laboratorio
- Standard OSHA (Occupational Safety and Health Administration)
- Linee guida ICH applicabili
Buone Pratiche di Laboratorio
- ISO / IEC 17025: 2017 - Requisiti generali per la competenza dei laboratori di prova e taratura
- OCSE (Organizzazione per la Cooperazione e lo Sviluppo Economico) - Linee guida di Buona Pratica di Laboratorio
- Guida EURACHEM / CITAC: Guida alla qualità in chimica analitica - Un aiuto per l'accreditamento, 3a edizione (2016), dovrebbe essere seguita nelle procedure analitiche.
- 21 CFR 58: Buone pratiche di laboratorio per studi di laboratorio non clinici
- Guida ai Regolamenti GLP del Regno Unito, Febbraio 2000 (a cura di GLPMA)
- Manuale dell'WHO sulle buone pratiche di laboratorio (GLP): pratiche di qualità per la ricerca e lo sviluppo non clinico regolamentato
- Health Canada: Documento guida finalizzato - Dati di studi di laboratorio non clinici a supporto delle domande e delle presentazioni di prodotti farmaceutici: Adesione alle Buone Pratiche di Laboratorio
- standard OSHA (Occupational Safety and Health Administration)
- Linee guida ICH applicabili
Good Clinical Practice (GCP) e Good Pharmacovigilance Practice (GVP)
- Linea guida tripartita armonizzata ICH: Linea guida per la buona pratica clinica - E6
- Specifiche del Rapporto di Sicurezza Individuale (ICSR) E2B(R3) e file correlati
- Rapporto Periodico di Valutazione Beneficio-Rischio (PBRER) E2C(R2)
- Altre Linee Guida ICH Applicabili
- Linee guida sui moduli delle Buone Pratiche di Farmacovigilanza (GVP)
- Requisiti FDA per la segnalazione di sicurezza per studi IND e BA/BE
- Segnalazione di sicurezza post-commercializzazione per farmaci umani e prodotti biologici, inclusi i vaccini
- Specifiche di implementazione regionale FDA per la segnalazione ICH E2B(R3) al sistema di segnalazione degli eventi avversi della FDA (FAERS)
- Fornire presentazioni in formato elettronico – Domande e risposte tecniche su ICSR non urgenti post-commercializzazione.
- Pianificazione della Farmacovigilanza E2E
Sicurezza delle informazioni, privacy dei dati e validazione dei sistemi informatici (CSV)
- ISO 27001: 2013 Tecnologia dell'informazione – Tecniche di sicurezza – Sistema di gestione della sicurezza delle informazioni – Requisiti
- ISO 27002: 2013 Tecnologia dell'informazione – Tecniche di sicurezza – Codice di condotta per la gestione della sicurezza delle informazioni
- USFDA 21 CFR Part 11: Registrazioni elettroniche; Firme elettroniche – Ambito e applicazione
- Guida EU GMP Allegato 11
- Notifica della Linea Guida ERES Giapponese N. 0401022
- GAMP 5: un approccio basato sul rischio ai sistemi computerizzati GxP conformi
- USFDA – Linee guida per la convalida del software
- Linee guida ICH QSEM applicabili
- Pianificare e creare SOP e controllare gli impianti di produzione
- Modello di processo integrato
- Mantenere l'immagine del marchio
- Servizi di valutazione del rischio
- Risparmi complessivi sui costi
- Implementare processi aziendali efficaci e conformi
- Definire strategie di convalida e qualificazione
- Competenza in conformità normativa e di audit
- Revisori esperti di conformità
Il nostro approccio di consulenza in materia di qualità e conformità è pensato per fornire indicazioni concrete e miglioramenti duraturi, aiutando la vostra azienda a raggiungere l'eccellenza operativa e il successo normativo.



 Servizi di Conformità e Audit
Servizi di Conformità e Audit










