Panoramica sulla registrazione dei dispositivi medici US FDA
Gli Stati Uniti d'America (USA) sono rinomati per essere un mercato altamente regolamentato per i Dispositivi Medici, con percorsi e requisiti di registrazione ben definiti. Le normative iniziali sui dispositivi medici degli Stati Uniti risalgono al 1976 e si sono evolute nel tempo. Sono regolamentate dal Centre for Devices and Radiological Health (CDRH) sotto la Food and Drug Administration (FDA). Freyr ha aiutato numerosi produttori di dispositivi a conformarsi al processo di registrazione dei dispositivi medici della US FDA.

Autorità Regolatoria: Food and Drug Administration (FDA)
Regolamentazione: Titolo 21 Codice dei Regolamenti Federali (21 CFR) Parti da 800 a 1299
Percorso regolatorio: Notifica pre-immissione sul mercato o Autorizzazione prima dell'immissione in commercio o Classificazione De Novo
Rappresentante autorizzato: Agente negli Stati Uniti
Requisito QMS: Regolamento del Sistema Qualità (QSR) (21 CFR parte 820)
Valutazione dei dati tecnici: Centro per i Dispositivi e la Salute Radiologica.
Validità della Licenza: Illimitata
Requisiti di etichettatura: 21 CFR Parte 801
Formato di sottomissione: Carta e CD/DVD
Lingua: Inglese
Classificazione dei Dispositivi Medici negli US
FDA classifica i Dispositivi Medici in 3 categorie basate sul rischio: Classe I, Classe II e Classe III. I dispositivi di Classe I sono considerati a basso rischio, mentre quelli di Classe III sono associati a rischio elevato. I requisiti di registrazione e il percorso variano in base alla classe del dispositivo.
| Classe del Dispositivo | Rischio | Percorso di Registrazione per approvazione |
|---|---|---|
| I | Basso Rischio | Esente da 510(k) |
| II | Rischio moderato (Con dispositivo di riferimento) | Notifica pre-commercializzazione/510(k) |
Rischio moderato (Senza dispositivo di riferimento) | Domanda De Novo | |
| III | Rischio Elevato | Approvazione pre-commercializzazione (PMA) |
US FDA Agente
Le aziende senza uffici locali negli US devono nominare un Agente US FDA per rappresentare il produttore. L'agente US FDA deve risiedere negli US o mantenere una sede di attività negli US. Le responsabilità da adempiere da parte dell'agente sono predeterminate dalla US FDA come parte delle normative CFR.
Naviga tra le Domande Frequenti (FAQ) sull'Agente US.
Incontri interattivi con la US FDA
US FDA supporta i produttori attraverso vari tipi di incontri di Q-Submission per raggiungere diversi obiettivi. Tali incontri con l'agenzia, prima dell'inizio o durante lo sviluppo del dispositivo, e prima della presentazione delle domande di registrazione di dispositivi medici alla US FDA, aiutano i produttori a ottimizzare i tempi e i costi sostenuti per la commercializzazione del dispositivo.
Registrazione dei Dispositivi Medici negli US
I dispositivi possono essere approvati dal CDRH, FDA attraverso uno dei vari percorsi di registrazione. Sono elencati come:
Dispositivi Medici di Classe I: I dispositivi di classe I sono solitamente esenti da GMP e dalla presentazione 510(k) e non richiedono l'approvazione preventiva della US FDA per essere commercializzati negli US. Altri requisiti come la registrazione dello stabilimento, l'elenco dei dispositivi, l'UDI, il Post-market Surveillance (PMS) ecc. devono essere rispettati dal produttore.
Dispositivi Medici di Classe II: I dispositivi a rischio medio con dispositivi predicati approvati 510(k) possono optare per la Notifica Pre-commercializzazione 510(k) (PMN), chiamata anche registrazione 510(k). Il dispositivo in questione dovrà stabilire l'Equivalenza Sostanziale (SE) con i dispositivi predicati identificati e dichiarati. Questo percorso è il più ampiamente adottato per la registrazione dei dispositivi negli US. I produttori di dispositivi a rischio medio senza predicati possono richiedere la classificazione alla US FDA tramite applicazioni De-Novo.
Dispositivi Medici di Classe III: I produttori di dispositivi di Classe III ad alto rischio devono presentare una domanda di Approvazione Pre-commercializzazione (PMA) alla US FDA. I dispositivi devono essere sottoposti a una valutazione clinica dettagliata e il produttore deve presentare dati dettagliati sulla sicurezza e l'efficacia derivanti da studi clinici. La US FDA effettuerà un'ispezione del QMS come parte della valutazione prima di rilasciare un' Approvazione Pre-commercializzazione per il dispositivo.
Registrazioni di Dispositivi Medici non-CDRH
In base alle indicazioni d'uso, alcuni prodotti borderline considerati dispositivi medici in altri paesi, come respiratori chirurgici, disinfettanti, prodotti combinati, coinvolgono altre Agenzie come il Centro per il Controllo delle Malattie (CDC), l'Istituto Nazionale per la Sicurezza e la Salute sul Lavoro (NIOSH), l'EPA, il Centro per la Valutazione e la Ricerca Biologica (CBER), il Centro per la Valutazione e la Ricerca sui Farmaci (CDER).
Requisiti di conformità post-approvazione per i dispositivi medici.
Tutti i produttori di dispositivi devono rispettare i requisiti post-approvazione elencati di seguito:
- Requisiti di Registrazione e Inserimento in Elenco: Gli stabilimenti di tutte le classi di dispositivi devono essere registrati nel database FURLs e il dispositivo deve essere inserito in elenco dopo aver ottenuto l'approvazione e prima della commercializzazione del dispositivo negli US. Alcuni dispositivi, come quelli a radiazioni, devono rispettare altri requisiti, come il numero di accesso, prima di poter essere importati negli US.
- Identificazione Unica del Dispositivo: Tutte le classi di dispositivi devono essere conformi ai regolamenti sull'Identificazione Unica del Dispositivo (UDI) per commercializzare i dispositivi negli US.
- Tasse di Registrazione dello Stabilimento: Il produttore deve pagare le tasse annuali di registrazione dello stabilimento per mantenere attiva la registrazione del proprio stabilimento e continuare a commercializzare dispositivi negli US. La FDA US ha una struttura tariffaria ridotta per le entità più piccole con un certificato di piccola impresa attivo.
- Audit di Qualità: Per i dispositivi non esenti da GMP, la FDA US può ispezionare lo stabilimento di produzione in qualsiasi momento per la conformità ai Regolamenti sui Sistemi di Qualità (QSR) in conformità con il 21 CFR 820.
Flusso del processo
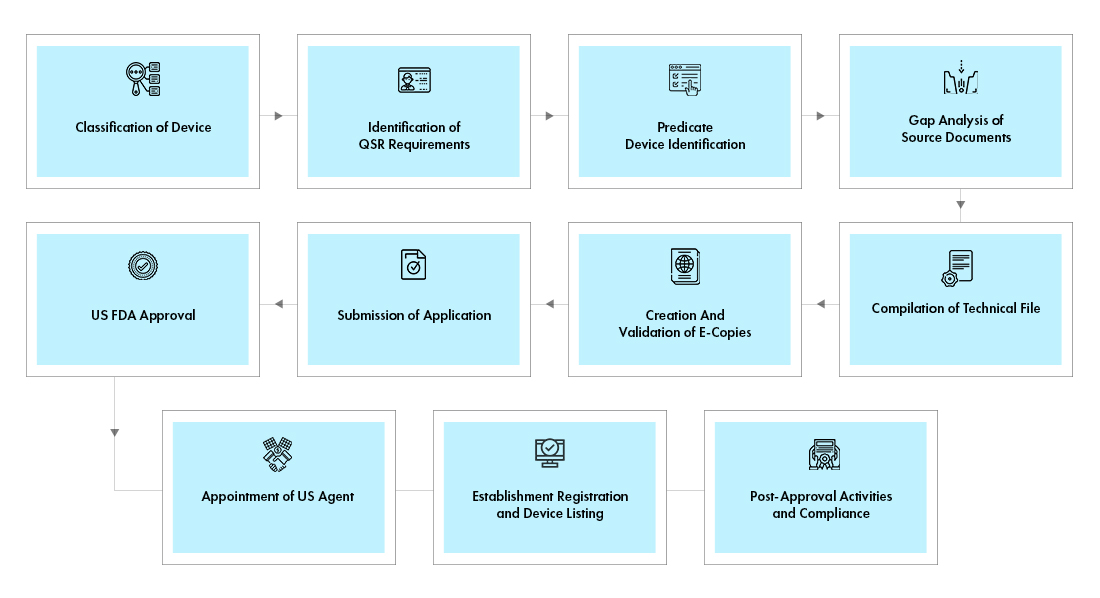
Gestione del ciclo di vita del dispositivo post-approvazione
Freyr supporta i produttori esteri nella gestione End-to-End del ciclo di vita dei dispositivi medici, incluse le attività post-approvazione, quali:
- Gestione delle modifiche post-approvazione - modifiche alle approvazioni esistenti dei dispositivi medici come l'aggiunta di nuove varianti, accessori; l'aggiunta di nuove indicazioni d'uso, tra gli altri.
- Mantenimento delle approvazioni e della registrazione attraverso il pagamento tempestivo delle tariffe MDUFA alla FDA
- Collegamento tra la US FDA e il produttore
Freyr dispone di un centro di distribuzione esclusivo negli US con un team professionale per fornire supporto normativo ai produttori nel mantenimento della qualità e della sicurezza necessarie per l'approvazione. Gli esperti di intelligence di Freyr osservano attentamente gli aggiornamenti normativi e tengono i clienti informati sui passi da intraprendere per la conformità del prodotto agli standard attuali.
Riepilogo
| Rischio | Classe del Dispositivo | Audit QMS | Disponibilità del dispositivo di riferimento | Percorso Regolatorio | Agente degli Stati Uniti | US Tempistiche FDA |
|---|---|---|---|---|---|---|
| Basso Rischio | I | No | Nord America | Esente | Sì | 1 Mese |
| Rischio Medio | II | Sì (dopo l'approvazione) | Sì | PMN/510(k) | Sì | 9 - 12 Mesi |
| Rischio Medio | II | Sì (dopo l'approvazione) | No | Richiesta di Classificazione De Novo | Sì | 18 - 30 Mesi |
| Rischio Elevato | III | Sì (prima dell'approvazione) | Nord America | PMA | Sì | 18 - 30 Mesi |
Servizi di Registrazione di Dispositivi Medici di Freyr
Freyr Competenza
- Due Diligence normativa
- Documentazione dei dispositivi
- Supporto 513(g)
- Registrazione 510(k)
- Richiesta di Classificazione De Novo
- Registrazione PMA
- 21 CFR 820 conformità
- BIMO Audit supporto
- Conformità MDSAP
- Supporto all'etichettatura
- Supporto per la pubblicazione e la presentazione
- Agente negli Stati Uniti
- Incontri Q-Submission
- Riunioni RFD e Pre-RFD
- Certificazione per piccole imprese
- Registrazione dello Stabilimento ed Elenco dei Dispositivi
- Conformità normativa per dispositivi medici a radiazioni
- Gestione delle modifiche post-approvazione
- Sorveglianza post-commercializzazione.
- Conformità UDI
- Consulenza normativa per la risoluzione delle carenze.