Panoramica sulla registrazione dei dispositivi medici di Health Canada
Il Canada, con alcune delle linee guida più rigorose, vanta uno dei migliori sistemi normativi al mondo per i dispositivi medici. In Canada, tutti i dispositivi medici sono regolamentati da Health Canada, Health Products and Food Branch, Therapeutic Products Directorate, Medical Devices Bureau. Health Canada esamina i dispositivi medici per valutarne la sicurezza, l'efficacia e la qualità prima che ne sia autorizzata la vendita in Canada, in conformità al Regolamento canadese sui dispositivi medici SOR/98-282, implementato nel 1998. Freyr è un partner attivo delle aziende di dispositivi medici per aiutarle a conformarsi alle linee guida di registrazione dei dispositivi medici di Health Canada.
Autorità Regolatoria: Health Canada
Regolamentazione: Regolamenti sui Dispositivi Medici (SOR/98-282)
Rappresentante autorizzato: Non richiesto
Requisito QMS: Conformità ISO 13485:2016 come Programma di Audit Unico per Dispositivi Medici (MDSAP)
Valutazione dei dati tecnici: Health Canada
Validità della Licenza: Illimitata
Requisiti di etichettatura: Parte 21 del MDR (SOR/98-282)
Formato di sottomissione: Cartaceo
Lingua: Inglese e Francese
Classificazione dei dispositivi medici di Health Canada
Il sistema di classificazione dei dispositivi medici di Health Canada è in gran parte mutuato dalla Direttiva 93/42/CEE del Consiglio dell'Unione Europea. Molte delle regole e delle interpretazioni dei termini sono simili a quelle proposte dall'Unione Europea. Non è necessariamente vero, tuttavia, che un dispositivo medico classificato in una classe secondo il sistema di classificazione dell'Unione Europea sarà classificato nella stessa classe in base al sistema di classificazione dei dispositivi medici del Canada. Il richiedente deve seguire le regole stabilite nei Regolamenti per determinare la classificazione appropriata per il proprio dispositivo in Canada.
I seguenti indicatori di rischio posti da un determinato dispositivo sono stati utilizzati per creare le regole di classificazione canadesi: grado di invasività, durata del contatto, sistema corporeo interessato ed effetti locali rispetto a quelli sistemici.
| Classe del Dispositivo | Rischio |
|---|---|
| I | Basso |
| II | Basso-moderato |
| III | Elevato-Moderato |
| IV | Elevato |
Rappresentante Autorizzato in Canada
Non è richiesto al produttore di nominare un Rappresentante Autorizzato in Canada. Il distributore, tuttavia, deve conformarsi ai requisiti di Health Canada per le Buone Pratiche di Distribuzione (GDP).
Registrazione dei Dispositivi Medici - Canada
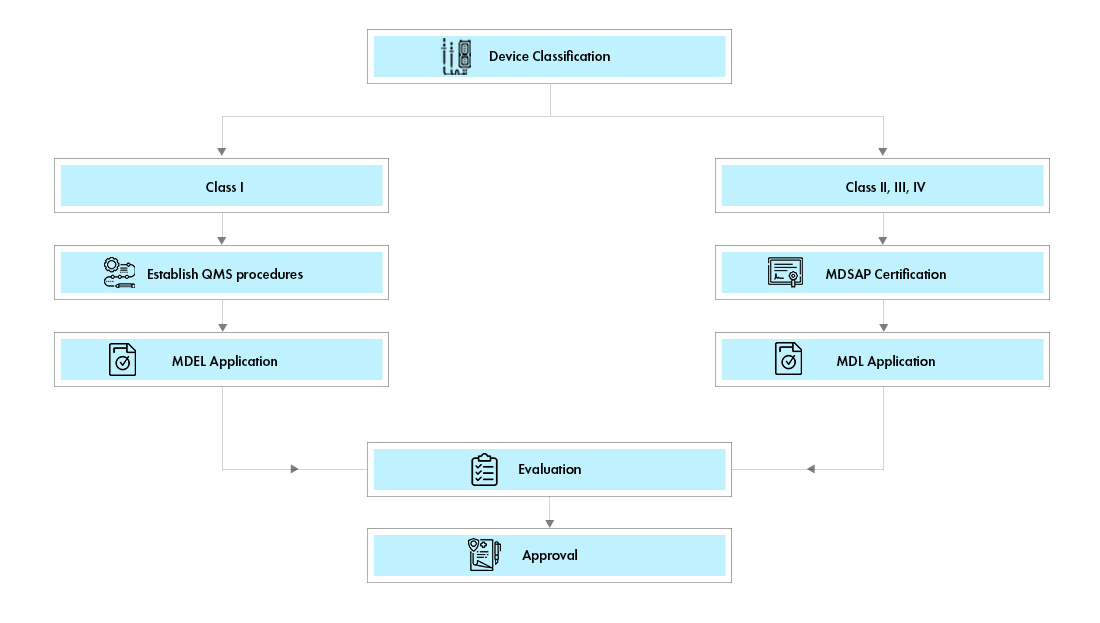
Esistono due percorsi per la registrazione dei dispositivi medici in Canada:
Licenza di Stabilimento per Dispositivi Medici (MDEL): I dispositivi di Classe I possono richiedere la Licenza di Stabilimento per Dispositivi Medici Canada (MDEL) preparando le procedure obbligatorie e pagando le tasse a Health Canada.
Licenza per Dispositivi Medici (MDL): I dispositivi di Classe II, III e IV devono richiedere una Licenza Canadese per Dispositivi Medici (MDL). I requisiti documentali per ciascuna classe di dispositivi variano.
Flusso del processo
Gestione del ciclo di vita del dispositivo post-approvazione
Freyr supporta i produttori esteri nella gestione End-to-End del ciclo di vita dei dispositivi medici, incluse le attività post-approvazione, quali:
- Gestione delle modifiche post-approvazione - modifiche alle approvazioni esistenti dei dispositivi medici come l'aggiunta di nuove varianti, accessori; l'aggiunta di nuove indicazioni d'uso, tra gli altri.
- Mantenimento delle approvazioni e della registrazione attraverso il pagamento tempestivo delle tasse amministrative e di registrazione
- Rinnovo delle licenze
- Collegamento tra Health Canada e il produttore.
Riepilogo
| Rischio | Classe del Dispositivo | Audit QMS | Percorso Regolatorio | Requisiti dei documenti | Tempistiche Health Canada |
|---|---|---|---|---|---|
| Basso | I | Nord America | MDEL |
| Nord America |
| Basso-moderato | II | Certificato MDSAP | MDL |
| 15 Giorni |
| Elevato-Moderato | III | Certificato MDSAP | MDL |
| 60 Giorni |
| Elevato | IV | Certificato MDSAP | MDL |
| 75 Giorni |
Servizi di Registrazione di Dispositivi Medici di Freyr
Freyr Competenza
- Servizi di classificazione e raggruppamento dei dispositivi medici di Health Canada
- Registrazione dei Dispositivi Medici, Canada
- Riunioni preliminari all'invio con Health Canada
- MDSAP, Canada
- Identificazione/Qualificazione del distributore per la conformità ai requisiti di Health Canada.
- Licenza di Stabilimento per Dispositivi Medici in Canada (MDEL)
- Licenze per Dispositivi Medici in Canada (MDL)
- Gestione delle modifiche post-approvazione
- Servizi di etichettatura secondo i requisiti di etichettatura di Health Canada per i dispositivi medici