
Servizi normativi per dispositivi medici
Panoramica a Singapore
I dispositivi medici a Singapore sono regolamentati ai sensi del Health Products Act (HPA) e del suo Health Product (Medical Devices) Regulations 2010.
Autorità Regolatoria: Health Science Authority (HSA)
Regolamentazione: Regolamento sui prodotti sanitari (dispositivi medici) del 2010
Percorso regolatorio: Divisione Dispositivi Medici dell'Autorità per le Scienze della Salute (HSA)
Rappresentante autorizzato: Registrante di Singapore
Requisito QMS: SS 620:2016, Standard di Singapore per le Buone Pratiche di Distribuzione dei Dispositivi Medici, e ISO 13485:2016
Valutazione dei dati tecnici: Health Science Authority (HSA)
Validità della Licenza: Tutte le licenze dei rivenditori sono valide per 12 mesi dalla data di approvazione.
Requisiti di Labelling: Guida normativa, GN- 23 Revisionata (1 marzo 2020)
Formato di sottomissione: Online
Lingua: Inglese
Classificazione Dispositivi Medici HSA
HSA applica 16 serie di regole per classificare i dispositivi medici dal rischio più basso a quello più alto nelle Classi A, B, C e D.
La classificazione del rischio dipende da fattori come la durata del contatto, il grado di invasività, l'uso previsto e il metodo di somministrazione.
Classificazione dei Dispositivi Medici, HSA
| Classe di Rischio | Livello di Rischio | Esempi di Dispositivi Medici |
|---|---|---|
| Classe A | Rischio basso | Visore per pellicole, mano chirurgica, guaina, maschera per ossigeno |
| Classe B | Rischio da basso a moderato | Bracciale per la pressione sanguigna, sterilizzatore a vapore |
| Classe C | Rischio da moderato ad alto | Monitor paziente, macchina a raggi X |
| Classe D | Rischio elevato | Stent cardiaci, pacemaker |
Classificazione IVD
Dispositivi medici diagnostici in vitro sono classificati di seguito dal rischio più basso a quello più alto.
Classe di rischio | Livello di Rischio | Esempi di Dispositivi Medici In Vitro |
|---|---|---|
| Classe A | Basso rischio individuale e basso rischio per la salute pubblica | Contenitore per campioni. |
| Classe B | Rischio individuale moderato o basso rischio per la salute pubblica o entrambi | Vitamina B12, autotest di gravidanza, anticorpo antinucleo, strisce reattive per urina |
| Classe C | Rischio individuale elevato o rischio moderato per la salute pubblica o entrambi | Automonitoraggio della glicemia, tipizzazione HLA, screening PSA, IgM per la rosolia |
| Classe D | Rischio individuale elevato e rischio per la salute pubblica elevato | screening dei donatori di sangue per l'HIV, kit diagnostico per l'HIV |
Rappresentante Autorizzato per Dispositivi Medici a Singapore / Registrante
Un Registrante è l'intermediario tra la tua azienda e l'HSA, che gestisce l'elenco di registrazione dei dispositivi a Singapore. Il rappresentante autorizzato per dispositivi medici di Singapore elabora la domanda di registrazione con l'HSA e detiene la registrazione del tuo dispositivo presso l'HSA. Solo le aziende o entità con sede a Singapore possono agire come Registrante; devono anche essere registrate presso l'HSA.
Registrazione Dispositivi Medici HSA
Il processo di registrazione dei dispositivi medici HSA viene condotto tramite il sistema online HSA Medical Device Information and Communication (MEDICS). Ogni registrazione di dispositivo HSA viene effettuata tramite un percorso di valutazione specifico, a seconda di quanto segue:
- Classificazione del rischio del dispositivo.
- Numero di approvazioni preventive rilasciate dalle agenzie di regolamentazione di riferimento estere.
- Durata dello storico di commercializzazione in sicurezza del dispositivo.
Il percorso di valutazione del dispositivo determinerà il tempo di risposta (TAT), le tariffe e i documenti richiesti per la registrazione.
Registrazione di Classe A - I dispositivi medici di Classe A sono esenti dalla registrazione del prodotto. Tuttavia, è necessario completare l'elenco di esenzione di Classe A in MEDICS durante la domanda di licenza del rivenditore.
Flusso del processo
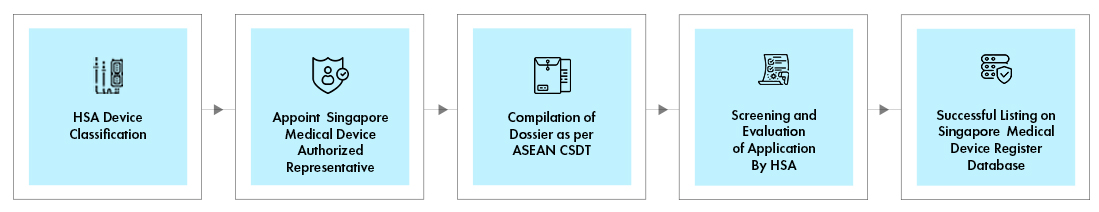
Gestione del ciclo di vita del dispositivo post-approvazione
Freyr supporta i produttori esteri nella gestione End-to-End del ciclo di vita dei dispositivi medici, incluse le attività post-approvazione, quali:
- Gestione delle modifiche post-approvazione - modifiche alle approvazioni esistenti dei dispositivi medici, come l'aggiunta di nuove varianti e accessori; l'aggiunta di nuove indicazioni d'uso, tra gli altri.
- Mantenimento delle approvazioni e delle registrazioni dei dispositivi medici attraverso il pagamento puntuale delle tasse amministrative e di registrazione.
- Rinnovo della licenza.
Con un team professionale per fornire supporto normativo, Freyr supporta i produttori nel mantenere la qualità e la sicurezza necessarie per l'approvazione. Gli esperti di intelligence di Freyr osservano attentamente gli aggiornamenti normativi e informano i clienti sui passi da intraprendere per la conformità dei prodotti agli standard prevalenti.
Riepilogo
Il tempo di elaborazione per la registrazione del prodotto è menzionato nella seguente tabella.
| Classe di Rischio | Immediata | Accelerato | Abbreviato | Valutazione Completa | Completa (Schema di revisione prioritaria) |
|---|---|---|---|---|---|
| Classe B | Registrazione immediata alla presentazione | 100 giorni lavorativi | 160 giorni lavorativi | 120 giorni lavorativi | |
| Classe C | Registrazione immediata alla presentazione (solo per applicazioni mediche mobili standalone di Classe C) | 120 giorni lavorativi | 160 giorni lavorativi | 220 giorni lavorativi | 165 giorni lavorativi |
| Classe D | 180 giorni lavorativi | 220 giorni lavorativi | 310 giorni lavorativi | 235 giorni lavorativi | |
| Classe D (dispositivi che incorporano prodotti medicinali) | 220 giorni lavorativi | 310 giorni lavorativi |
Il tempo di elaborazione per un cambio di registrante è di 40 giorni lavorativi.
NOTA-
- I dispositivi medici di Classe A sono esenti dalla registrazione del prodotto.
- Il tempo di elaborazione esclude il tempo impiegato per rispondere a eventuali richieste di chiarimenti o informazioni aggiuntive da parte dell'HSA durante la fase di valutazione.
Freyr Competenza
- Due diligence normativa per la registrazione dei dispositivi presso l'HSA, Singapore
- Classificazione e Raggruppamento dei Dispositivi Medici HSA
- Supporto per la Valutazione dell'Organismo di Valutazione della Conformità (CAB)
- Compilazione del Dossier secondo il Modello Comune di Presentazione ASEAN (CSDT)
- Registrazione dei dispositivi HSA;
- Rappresentanza Legale
- Supporto all'etichettatura
- Identificazione e Qualificazione del Distributore
- Sorveglianza post-commercializzazione
- Gestione delle modifiche post-approvazione.
- Rinnovo e Trasferimento della Licenza
- Servizi di presentazione e collegamento con la HSA



