
Panoramica sulla Registrazione dei Dispositivi Medici di Taiwan
Taiwan ha una crescente domanda di dispositivi medici. La Taiwan Food & Drug Administration (TFDA) sotto il Ministero della Salute e del Benessere (MOHW) regola i dispositivi medici attraverso il Pharmaceutical Affairs Act (PAA). I produttori stranieri senza un ufficio fisico a Taiwan richiedono la rappresentanza di un agente taiwanese come prerequisito per il processo di registrazione dei dispositivi medici a Taiwan.
Autorità Regolatoria: Amministrazione degli Alimenti e dei Farmaci di Taiwan
Regolamentazione: Legge sugli affari farmaceutici (PAA) e Regolamento per la registrazione dei Dispositivi Medici
Rappresentante autorizzato: Rappresentanza di agente a Taiwan richiesta
Requisito QMS: Documentazione del Sistema di Qualità (QSD) ISO 13485
Valutazione dei dati tecnicia: Divisione Dispositivi Medici e Cosmetici
Validità della Licenza: QSD - 3 anni; Registrazione del Prodotto - 5 anni
Requisiti di etichettatura: Articolo 75, Legge sugli Affari Farmaceutici
Formato di sottomissione: Cartaceo
Lingua: Inglese e Cinese
Classificazione dei Dispositivi Medici di Taiwan
La TFDA classifica i dispositivi medici in 3 classi in base al rischio: Classe I per dispositivi a basso rischio, Classe II per dispositivi a rischio moderato e Classe III per dispositivi ad alto rischio. La necessità di un dispositivo di riferimento rappresenta una sfida per l'ingresso sul mercato di dispositivi innovativi. Un maggiore divario temporale procedurale per i dispositivi di Classe II e III che richiedono la documentazione del sistema qualità è un'altra complessità coinvolta. Tutti i dispositivi medici importati devono ottenere un certificato di registrazione dalla TFDA.
| Classe del Dispositivo | Rischio |
|---|---|
| Classe I | Basso Rischio |
| Classe II | Rischio moderato |
| Classe III | Rischio Elevato |
Rappresentanza di agente a Taiwan
I produttori esteri senza un ufficio fisico a Taiwan dovrebbero nominare un Agente di Taiwan come prerequisito per commercializzare dispositivi a Taiwan. La nomina di un'organizzazione terza come Agente di Taiwan anziché un distributore offre la flessibilità di esplorare più distributori per una migliore penetrazione del mercato. L'Agente di Taiwan deve avere un'entità legale stabilita a Taiwan, certificata con una Licenza di Vendita Farmaceutica.
Registrazione dei Dispositivi Medici di Taiwan
Prima che un dispositivo medico possa essere venduto a Taiwan, è richiesta la registrazione della Documentazione del Sistema di Qualità (QSD) per lo stabilimento di produzione, oltre alla registrazione del dispositivo medico. La registrazione QSD è esentata solo per i dispositivi medici di Classe I (non sterili). Una licenza QSD (ricevuta all'approvazione della registrazione QSD) a Taiwan è simile alle Buone Pratiche di Fabbricazione (GMP) per i dispositivi medici.
La TFDA ha annunciato che, a partire dal 1° giugno 2022, i titolari di licenza di dispositivi medici di Classe III sono tenuti a caricare l'UDI e le informazioni di prodotto corrispondenti nel database UDI (UDID). I produttori di dispositivi medici sono inoltre tenuti ad apporre l'UDI sull'etichetta del prodotto. Inoltre, a partire dal 1° giugno 2023, i dispositivi medici di Classe II dovranno soddisfare le normative pertinenti relative all'UDI.
Flusso del processo
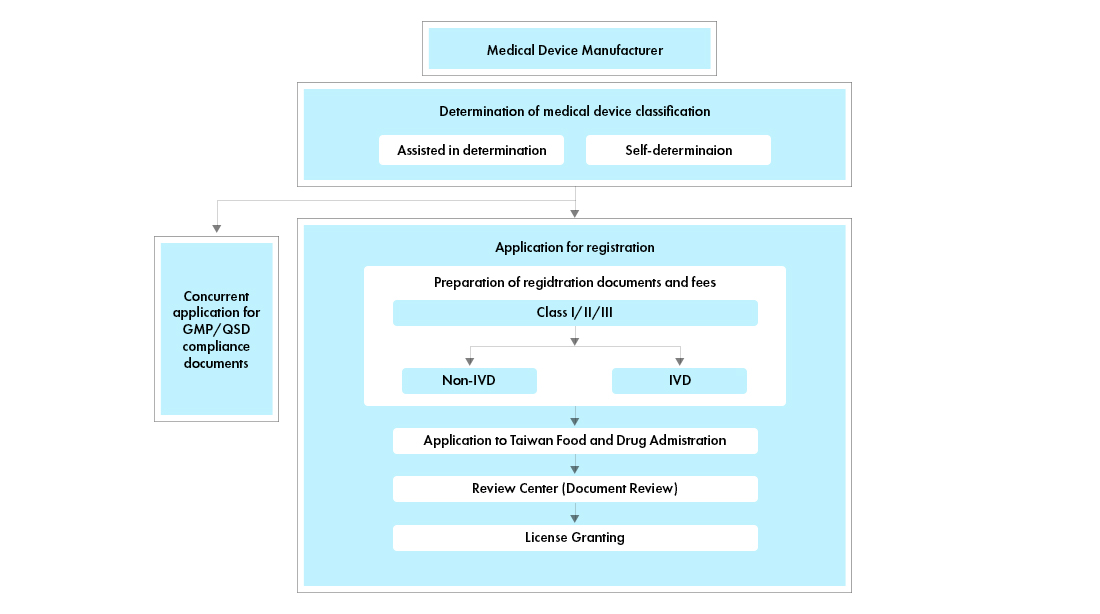
Gestione del ciclo di vita del dispositivo medico post-approvazione
Freyr supporta i produttori esteri nella gestione End-to-End del ciclo di vita dei dispositivi medici, incluse le attività post-approvazione, quali:
- Gestione delle modifiche post-approvazione - modifiche alle approvazioni esistenti dei dispositivi medici come l'aggiunta di nuove varianti, accessori; l'aggiunta di nuove indicazioni d'uso, tra gli altri.
- Mantenimento delle approvazioni e della registrazione attraverso il pagamento tempestivo delle tasse amministrative e di registrazione
- Rinnovo delle licenze
- Collegamento tra la TFDA e il fabbricante
- Gestione dell'Importazione
Freyr è specializzata nel soddisfare le esigenze normative dei dispositivi medici a Taiwan. Grazie a una vasta rete, Freyr aiuta a nominare un agente locale affidabile la cui presenza è di estrema importanza durante tutta la sorveglianza post-commercializzazione. I nostri esperti assistono anche nella selezione di un dispositivo precedente idoneo e delle approvazioni esistenti da altri mercati per supportare l'ingresso di nuovi dispositivi sul mercato.
Riepilogo
| Classe del Dispositivo | Criteri di rischio / classificazione | QMS | Registrazione del Prodotto |
|---|---|---|---|
| Classe I | Basso Rischio | Esente (dispositivi di Classe I non sterili) | Sì |
| Classe II | Rischio moderato | QSD | Sì |
| Classe III | Rischio Elevato | QSD | Sì |
Freyr Competenza
- Due Diligence normativa
- Classificazione Ufficiale
- Approvazioni QSD
- Registrazione dei dispositivi
- Rappresentante Legale
- Supporto all'etichettatura
- Supporto per la traduzione
- Identificazione e qualificazione del distributore
- Sorveglianza post-commercializzazione
- Gestione delle modifiche post-approvazione
- Rinnovo e trasferimento della licenza
- Sottomissione e collegamento


