
Panoramica sulla Registrazione dei Dispositivi Medici in Vietnam
Il mercato dei dispositivi medici del Vietnam è in crescita ed è attualmente uno dei settori in espansione nel paese. I dispositivi medici nel paese sono regolamentati dal Dipartimento delle Attrezzature Mediche e dei Lavori Sanitari (DMEHW) sotto il Ministero della Salute. I produttori stranieri devono nominare un Rappresentante Autorizzato Locale in Vietnam per assisterli nel processo di registrazione dei dispositivi medici in Vietnam.
Autorità Regolatoria: Dipartimento delle Attrezzature Mediche e Opere Sanitarie (DMEHW)
Regolamentazione: Decreto n. 98/2021/ ND-CP
Rappresentante autorizzato: Rappresentante Autorizzato Locale in Vietnam
Requisito QMS: ISO 13485:2016
Valutazione dei dati tecnici: Dipartimento delle Attrezzature Mediche e Costruzioni (DMEC) del MoH
Requisiti di Labelling: Decreto n. 111/2021
Formato di sottomissione: Online- Tempistiche: 15 - 60 giorni
Lingua: Inglese e Vietnamita
Classificazione dei Dispositivi Medici in Vietnam
I dispositivi sono classificati in 4 classi (A, B, C e D), che sono anche suddivise in due gruppi: gruppo 1 (Classe A) e gruppo 2 (Classe B, C e D). La classificazione formale è disponibile presso il Dipartimento vietnamita delle apparecchiature mediche e dei lavori sanitari (DMEHW).
| Gruppo | Classe | Rischio |
|---|---|---|
Gruppo 1 | Classe A | Basso livello |
Gruppo 2 | Classe B | Livello medio di rischio inferiore |
Classe C | Livello medio superiore di rischi | |
Classe D | Livello elevato di rischi |
Rappresentante Autorizzato Locale in Vietnam
La nomina di un agente vietnamita affidabile e competente per i produttori stranieri è cruciale, poiché devono farsi carico dei servizi di garanzia offerti dal produttore come parte della vendita del dispositivo. La traduzione in vietnamita è un requisito indispensabile per entrare nella regione, il che può essere effettivamente impegnativo nella pratica.
Freyr offre supporto normativo che copre l'intera gamma di attività, come l'ottenimento del numero di riconoscimento di libera vendita coinvolto nell'approvazione dei dispositivi medici da parte delle autorità. Forniamo anche supporto linguistico esperto per mantenere intatta la prospettiva normativa della traduzione. Soddisfiamo le esigenze post-approvazione dei clienti per mantenere la conformità durante l'intero ciclo di vita del prodotto in Vietnam.
Registrazione dei Dispositivi Medici in Vietnam
Tutti i prodotti di Classe A e B richiederanno una Licenza di Autorizzazione all'Immissione in Commercio (AIC). I dispositivi di Classe A e B saranno sottoposti a una rapida revisione amministrativa da parte del Dipartimento della Salute della provincia in cui ha sede il Titolare della Registrazione.
I dispositivi di Classe C e D dovranno ora richiedere una licenza di Autorizzazione all'Immissione sul Mercato (MA). Le licenze MA rimarranno valide a tempo indeterminato.
Flusso del processo
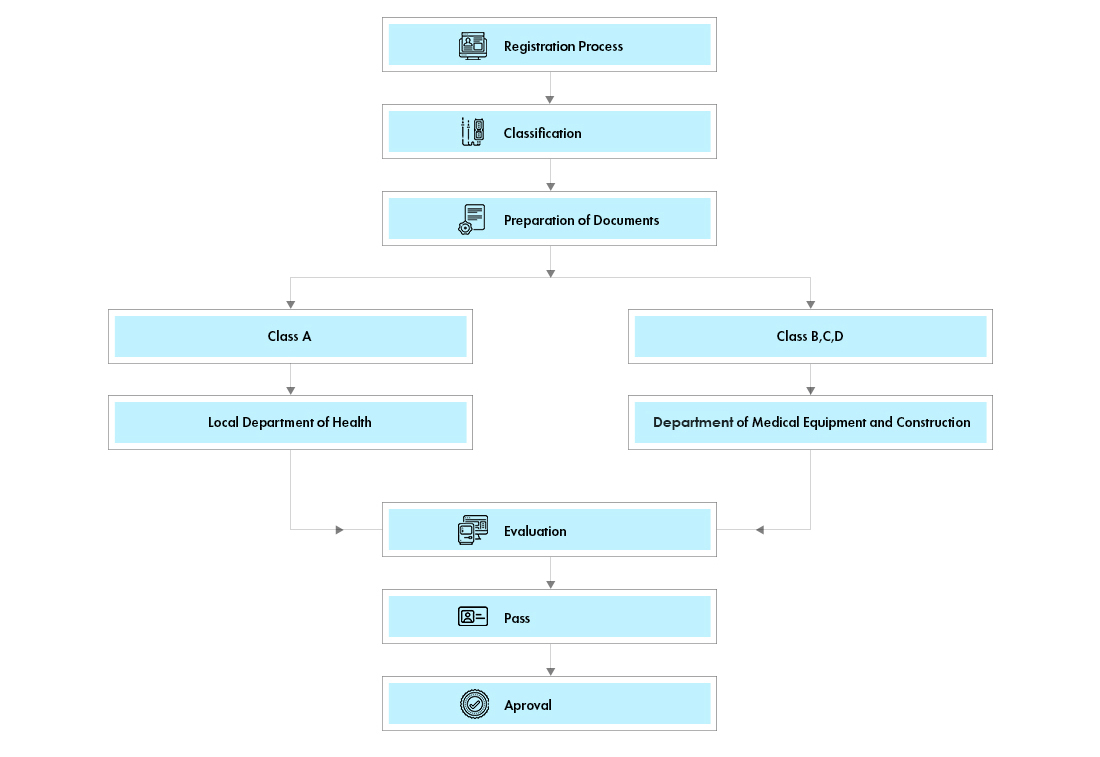
Gestione del ciclo di vita del dispositivo post-approvazione
Freyr supporta i produttori esteri nella gestione End-to-End del ciclo di vita dei dispositivi medici, incluse le attività post-approvazione, quali:
- Gestione delle modifiche post-approvazione - modifiche alle approvazioni esistenti dei dispositivi medici come l'aggiunta di nuove varianti, accessori; l'aggiunta di nuove indicazioni d'uso, tra gli altri.
- Mantenimento delle approvazioni e della registrazione attraverso il pagamento tempestivo delle tasse amministrative e di registrazione
- Rinnovo delle licenze
- Collegamento tra il DMEHW e il fabbricante
- Gestione dell'importazione
Riepilogo
Gruppo | Classe | Rischio | Percorso Regolatorio | Tempistiche | Validità |
|---|---|---|---|---|---|
Gruppo 1 | Classe A | Basso livello | Dichiarazione di norma applicabile | 15 - 60 giorni | Illimitata |
Gruppo 2 | Classe B | Livello medio di rischio inferiore | Certificato di registrazione per la libera vendita. | 15 - 60 giorni | 5 anni |
Classe C | Livello medio superiore di rischi | Certificato di registrazione per la libera vendita. | 15 - 60 giorni | 5 anni | |
Classe D | Livello elevato di rischi | Certificato di registrazione per la libera vendita. | 15 - 60 giorni | 5 anni |
Freyr Competenza
- Due Diligence normativa
- Classificazione Ufficiale
- Registrazione dei dispositivi
- Licenza di importazione
- Supporto all'etichettatura
- Supporto per la traduzione
- Identificazione e qualificazione del distributore
- Sorveglianza post-commercializzazione
- Gestione delle modifiche post-approvazione
- Rinnovo e trasferimento della licenza
- Sottomissione e collegamento
- Sdoganamento


