Panoramica sulla Registrazione dei Dispositivi Medici in Argentina
L'Argentina è uno dei paesi in rapida crescita in America Latina che offre opportunità alle aziende di dispositivi medici, con un sistema sanitario noto per la sua dedizione alla sicurezza dei pazienti e servizi medici di alta qualità. La registrazione dei dispositivi medici in Argentina è supervisionata dall'autorità di regolamentazione – l'Amministrazione Nazionale di Farmaci, Alimenti e Dispositivi Medici (ANMAT).

Autorità Regolatoria: Amministrazione Nazionale dei Farmaci, degli Alimenti e dei Dispositivi Medici (ANMAT)
Normative: Disposizione 2318/2002 e Disposizione 727/2013
Percorso regolatorio: Sistema elettronico di notifica dei dispositivi assistita via web (WAND)
Rappresentante autorizzato: Rappresentante Autorizzato in Argentina (AAR)
Requisito QMS: ISO 13485 (ANMAT MDS), e MDSAP (Membro Affiliato)
Valutazione dei dati tecnici: Amministrazione Nazionale dei Medicinali, degli Alimenti e dei Dispositivi Medici (ANMAT)
Requisiti di etichettatura: Allegato III.B della Disposizione 2318/2002 e Allegato V della Disposizione 727/2013.
Formato di sottomissione: Elettronico (portale HELENA)
Lingua: Spagnolo
Classificazione dei Dispositivi Medici in Argentina
Nel processo normativo ANMAT, il primo passo per determinare il percorso di registrazione e la conformità alle normative argentine è stabilire la classificazione del dispositivo medico. In Argentina, i dispositivi sono classificati in quattro classi in base al rischio (Classe I-IV).
| Classe di Dispositivo Medico | Criteri |
|---|---|
| Classe I | Basso Rischio |
| Classe II | Rischio Basso - Moderato |
| Classe III | Rischio alto - moderato |
| Classe IV | Rischio Elevato |
| Classe IVD | Criteri |
|---|---|
| Classe A | Diagnosi di malattie non infettive o non trasmissibili. |
| Classe B | Diagnosi di malattie infettive ad eccezione di quelle appartenenti alla Classe C. |
| Classe C | Diagnosi di malattie infettive a trasmissione sessuale, o trasmesse dal sangue o dai suoi derivati, nonché per l'identificazione dei gruppi sanguigni. |
| Classe D | Per l'autovalutazione. |
Rappresentante Autorizzato in Argentina (AAR)
Il titolare della registrazione di qualsiasi dispositivo medico in Argentina è legalmente responsabile della registrazione e della commercializzazione del dispositivo nel paese. Questo può essere il fabbricante del dispositivo, o un rappresentante autorizzato locale (AAR) in Argentina che agisce per conto del fabbricante.
Tutti i dispositivi medici commercializzati in Argentina devono essere registrati presso l'ANMAT. Il processo di registrazione può essere complesso e lungo, per cui si raccomanda spesso ai produttori esteri di nominare un AAR per assisterli.
Registrazione di dispositivi medici ANMAT
Il processo di registrazione dei dispositivi medici ANMAT è simile ai processi di notifica e registrazione brasiliani, con l'entità del controllo richiesto per l'approvazione che aumenta in base alla classificazione del dispositivo (Classe I, II, III e IV). Tutti i produttori di dispositivi medici devono inoltre conformarsi all'ANMAT-MDS, che è l'equivalente argentino della BGMP ed è anche in linea con la ISO 13485:2016.
Flusso del processo
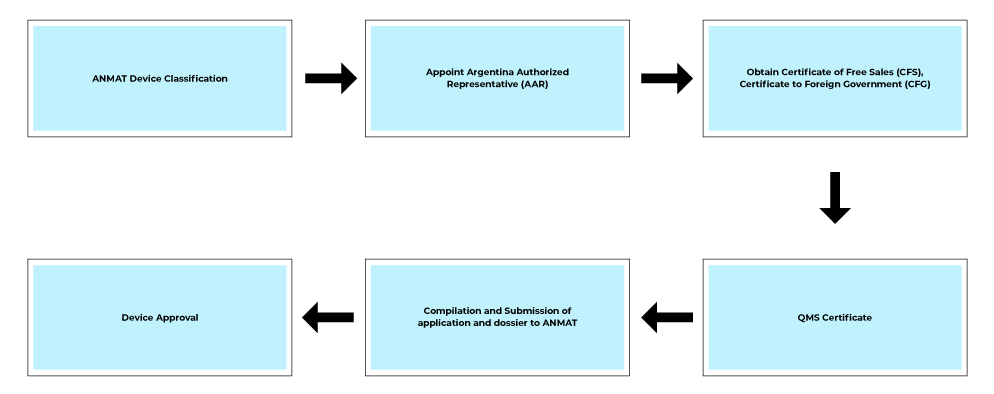
Servizi post-approvazione
Freyr supporta i produttori esteri nella gestione End-to-End del ciclo di vita dei dispositivi medici, incluse le attività post-approvazione, quali –
- Gestione delle modifiche post-approvazione - modifiche alle approvazioni esistenti dei dispositivi medici, come l'aggiunta di nuove varianti, accessori e nuove indicazioni d'uso, tra gli altri.
- Mantenimento delle approvazioni e della registrazione attraverso il pagamento tempestivo delle tasse amministrative e di registrazione.
- Rinnovo delle licenze.
- Collegamento tra ANMAT e il fabbricante.
- Segnalazione di eventi avversi.
- Gestione dell'importazione.
Freyr assiste i produttori nell'identificazione della classificazione dei dispositivi come primo passo. Freyr aiuta i clienti a districarsi nel percorso normativo e a ottenere le certificazioni, contribuendo a risolvere le complessità normative. Con comprovata esperienza nel lancio di numerosi dispositivi nella regione, Freyr offre servizi normativi End-to-End per i dispositivi medici.
Riepilogo
| Classe di Dispositivi | Percorso di Registrazione (Notifica o Registrazione Completa) | Tempistiche dell'Agenzia Sanitaria | Validità della Registrazione (anni) |
|---|---|---|---|
| Dispositivi di Classe I | Registrazione completa. | 4-6 mesi | 5 anni |
| Dispositivi di Classe II | Registrazione completa. | 4-6 mesi | 5 anni |
| Dispositivi di Classe III | Registrazione completa. | 6-8 mesi | 5 anni |
| Dispositivi di Classe IV | Registrazione completa. | 6-8 mesi | 5 anni |
*Si prega di notare che fattori come le limitazioni di larghezza di banda, gli aggiornamenti normativi e altre variabili possono portare a estensioni delle tempistiche dell'Autorità Sanitaria.
Freyr Competenza
- Servizi di Rapporti di Regulatory Intelligence.
- Servizi di Classificazione Ufficiale.
- Compilazione di Documenti Tecnici.
- Servizi di Registrazione del Dispositivo.
- Servizi di Rappresentante Autorizzato in Argentina (AAR).
- Servizi di Importazione.
- Permessi e Autorizzazioni Operative.
- Servizi di Traduzione.
- Servizi di Etichettatura e Artwork.
- Servizi di identificazione e qualificazione del distributore.
- Sorveglianza post-commercializzazione.
- Servizi di rinnovo e trasferimento della licenza.
