Panoramica sulla Registrazione dei Dispositivi Medici in Egitto
Da settembre 2018, la registrazione dei dispositivi medici è diventata obbligatoria in Egitto. L'industria dei dispositivi medici nel paese ha registrato una crescita costante, rendendo il mercato attraente per produttori e distributori. Con una valutazione di 4,0 miliardi di dollari nel 2021, il mercato egiziano dei dispositivi medici è proiettato a raggiungere un Tasso di Crescita Annuo Composto (CAGR) di oltre il 3% dal 2022 al 2027. L'importazione soddisfa in gran parte la domanda di dispositivi medici in Egitto, data la produzione locale relativamente bassa. In particolare, il mercato egiziano dei dispositivi medici si posiziona come il secondo più grande nella regione del Medio Oriente e del Nord Africa (MENA). Questa panoramica esplora gli aspetti chiave del processo di registrazione egiziano, offrendo approfondimenti sul quadro normativo e sui requisiti per portare dispositivi medici innovativi all'avanguardia del settore sanitario egiziano.
Autorità Regolatoria: Autorità Egiziana per i Farmaci (EDA)
Normativa: Legge egiziana sui dispositivi medici Legge n. 10 del 2003
Percorso Normativo: Registrazione del Prodotto (Percorso normale e accelerato) e Classificazione Ufficiale
Rappresentante Autorizzato Locale in Egitto: Titolare della Registrazione Egiziana (ERH)
Requisito SGQ: ISO 13485
Valutazione dei Dati Tecnici: Il Drug Policy and Planning Center (DPPC) e la Central Administration of Pharmaceutical Affairs (CAPA).
Validità della licenza: Dieci anni
Formato di Presentazione: Cartaceo ed Elettronico
Traduzione: Documenti Tradotti in Arabo e Inglese
Classificazione del Dispositivo
In Egitto, la classificazione dei dispositivi medici si allinea al sistema di classificazione europeo, che classifica i dispositivi medici in base all'uso previsto e ai potenziali rischi associati al loro impiego. I produttori dovrebbero identificare la classificazione corretta dei loro dispositivi per garantire la conformità ai requisiti normativi e ottenere le approvazioni necessarie per la commercializzazione e la distribuzione in Egitto.
Classi dei Dispositivi Medici
| Classe | Rischio |
|---|---|
| Classe I | Basso |
| Classe IIa | Basso-Medio |
| Classe IIb | Medio-Alto |
| Classe III | Elevato |
Rappresentante Autorizzato Locale in Egitto
Le aziende di dispositivi medici con sede al di fuori dell'Egitto devono nominare un Agente Locale, denominato “Titolare della Registrazione Egiziano (ERH)”, per gestire la presentazione delle domande di registrazione e dei relativi dossier all'EDA per loro conto. L'ERH agisce da tramite tra il fabbricante e l'autorità regolatoria, assicurando la preparazione e l'invio accurati di tutta la documentazione necessaria e verificando che il dispositivo medico rispetti gli standard di sicurezza, qualità ed efficacia dell'EDA. Inoltre, l'ERH è responsabile della conservazione della documentazione di registrazione, della segnalazione di incidenti o richiami e della garanzia del rispetto continuo di tutti gli standard e regolamenti applicabili per l'intero ciclo di vita del dispositivo. Il Titolare della Registrazione Egiziano (ERH) è pienamente responsabile di assicurare la registrazione di un dispositivo medico presso l'EDA, in particolare all'interno dell'Amministrazione Centrale dei Dispositivi Medici. Questo ruolo comporta la garanzia della conformità del dispositivo ai requisiti regolatori dell'EDA per la sua commercializzazione e distribuzione in Egitto.
Registrazione dei Dispositivi Medici
Ottenere l'autorizzazione all'immissione in commercio per un dispositivo medico in Egitto comprende diverse fasi, tra cui la preparazione della documentazione richiesta, la presentazione della domanda all'EDA, l'adesione ai requisiti di classificazione e del sistema di qualità, la nomina di un ERH, se necessario, e l'adempimento degli obblighi post-commercializzazione. Il processo di registrazione è fondamentale per garantire che i dispositivi medici siano conformi agli standard prescritti di sicurezza, qualità ed efficacia stabiliti dall'Autorità Regolatoria Egiziana. La documentazione richiesta può variare in base al percorso di registrazione scelto, ma generalmente comprende quanto segue:
- Certificato CE (se applicabile).
- Certificato di Libera Vendita (CFS).
- Certificazione ISO 13485.
- Dichiarazione di Conformità (DoC).
Flusso del processo
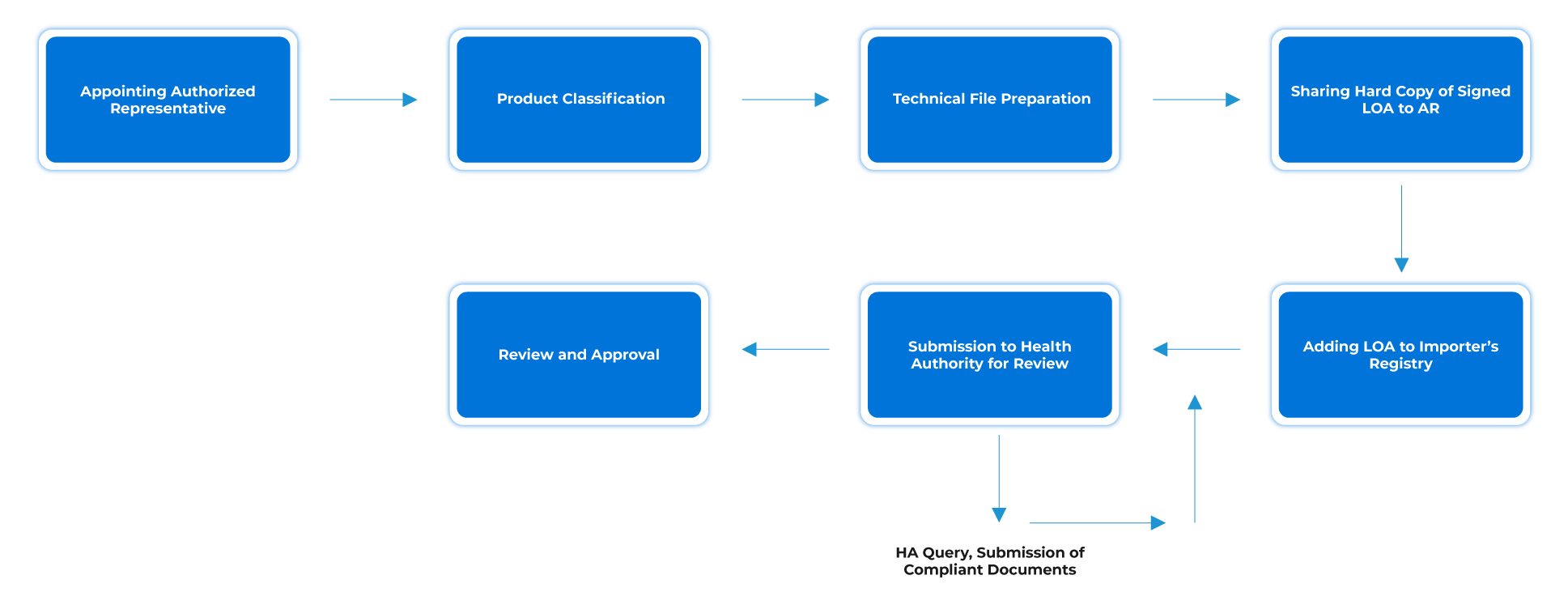
Gestione del ciclo di vita dei dispositivi post-approvazione
Freyr offre un supporto completo ai produttori esteri nella gestione dell'intero ciclo di vita dei dispositivi medici in Egitto, comprese le attività post-approvazione:
- Gestione delle modifiche post-approvazione, che riguardano le modifiche alle approvazioni esistenti dei dispositivi medici, come l'aggiunta di nuove varianti, accessori e indicazioni d'uso.
- Mantenimento della ISO 13485:2016.
- Certificazione CE.
- Agire come intermediario tra l'Organismo Notificato (NB) e il fabbricante.
- Un sistema di vigilanza in atto per monitorare la sicurezza del dispositivo medico dopo che è stata concessa l'autorizzazione all'immissione in commercio.
- Fornire aggiornamenti periodici riguardo alla sicurezza e all'efficacia del dispositivo medico, nonché eventuali modifiche dello stato normativo in altre giurisdizioni.
- Rinnovo dell'autorizzazione all'immissione in commercio, che avviene dopo un certo periodo e dipende dal tipo di dispositivo e dalle normative.
La gestione efficace della Post-market Surveillance (PMS) in Egitto implica la navigazione esperta dei quadri normativi stabiliti dall'EDA. I nuovi operatori del mercato che incontrano difficoltà con queste complessità e che non dispongono di un partner normativo consolidato possono avvalersi degli ampi servizi normativi offerti da Freyr. Questi servizi contribuiscono a un processo di approvazione senza intoppi per i dispositivi medici in Egitto, garantendo la conformità continua con il panorama normativo e le dinamiche di mercato in continua evoluzione.
Competenza nella registrazione dei dispositivi medici in Egitto
- Intelligence Regolatoria.
- Due Diligence Regolatoria.
- Classificazione dei Dispositivi Medici.
- Registrazione dei dispositivi.
- Titolare della Registrazione Egiziana.
- Supporto alla Traduzione.
- Redazione Medica.
- Supporto all'etichettatura.
- Identificazione e Qualificazione del Distributore.
- Gestione delle modifiche post-approvazione.
- Rinnovo e Trasferimento della Licenza.
- Sdoganamento.

