
Registrazione dei dispositivi medici in Indonesia - Panoramica
L'Indonesia ha avviato l'assistenza sanitaria universale per i suoi cittadini nel 2014. Ciò ha influenzato notevolmente la crescita del mercato dei dispositivi medici e ha portato a un aumento delle importazioni di tali dispositivi. I dispositivi in Indonesia sono regolamentati dall'Agenzia Nazionale per il Controllo dei Farmaci e degli Alimenti (NADFC), che opera sotto il Ministero della Salute indonesiano (MoH). L'ultima normativa in vigore per l'importazione di dispositivi medici è il Decreto n. 62, imposto nel 2017. Le aziende straniere devono nominare un rappresentante autorizzato locale in Indonesia per il processo di registrazione dei dispositivi medici nel paese.
Autorità Regolatoria: Agenzia Nazionale per il Controllo dei Farmaci e degli Alimenti (NADFC)
Regolamentazione: N. 62 / 2017
Rappresentante autorizzato: Rappresentante autorizzato locale in Indonesia
Requisito QMS: ISO 13485:2016
Valutazione dei dati tecnici: NADFC
Validità della Licenza: 5 anni
Requisiti di etichettatura: N. 62 / 2017
Formato di sottomissione: Online/Cartaceo
Lingua: Inglese e Indonesiano
Classificazione dei Dispositivi Medici in Indonesia
L'attuale regolamento classifica i dispositivi come A, B, C e D in base al rischio.
| Criteri di Rischio | Classe del Dispositivo |
|---|---|
| Basso Rischio | A |
| Rischio Basso Moderato | B |
| Rischio moderato – alto | C |
| Rischio Elevato | D |
Rappresentante Autorizzato Locale in Indonesia
Le normative indonesiane richiedono ai produttori di nominare un rappresentante locale con una Licenza di Distributore. Un distributore può essere nominato per rappresentare il produttore straniero in Indonesia. Tuttavia, la nomina di una terza parte indipendente fornirebbe flessibilità per cambiare distributori o nominarne più di uno per una migliore penetrazione del mercato.
Registrazione dei Dispositivi Medici in Indonesia
Il Rappresentante Locale deve creare un account nel portale online. Il processo di registrazione è lo stesso per tutte le classi di dispositivi. Tuttavia, i requisiti di documentazione variano in base alla classe del dispositivo. La registrazione è un processo in due fasi –
- Processo di pre-registrazione
- Processo di Valutazione
Il MoH verifica la classificazione del dispositivo e determina il costo della valutazione. Il risultato della pre-registrazione, insieme alla fattura, viene inviato via e-mail al richiedente. Il rappresentante locale, per conto del fabbricante, effettua il pagamento e carica la prova di pagamento. Il MoH esaminerà i documenti e comunicherà i risultati via e-mail al richiedente. Alcuni dispositivi richiedono test in-country presso un laboratorio accreditato.
Panoramica del Processo di Approvazione Normativa
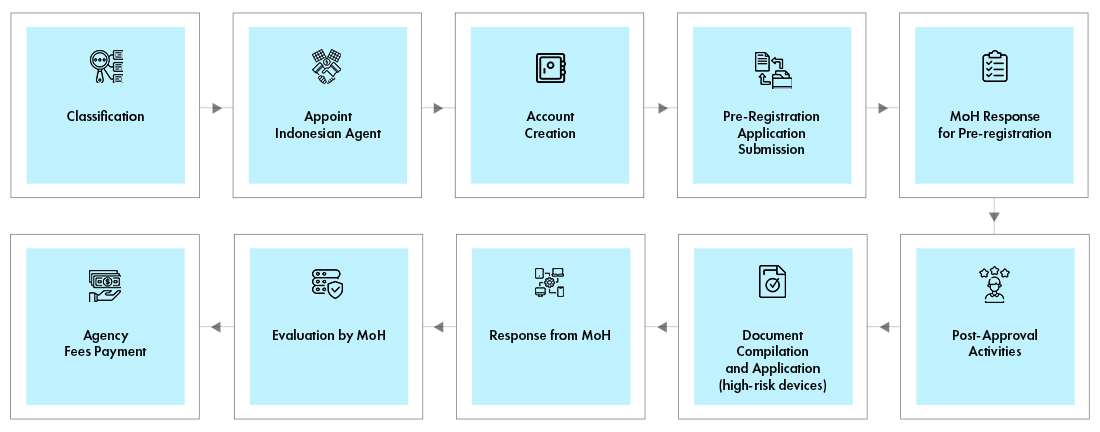
Il team di esperti di Freyr monitora le tendenze e le normative in evoluzione e aiuta gli stakeholder a mantenere la conformità normativa durante l'intero ciclo di vita del prodotto. Offriamo soluzioni normative per mantenere altri aspetti normativi di conformità entro i budget limitati.
Classe del dispositivo | Classe di Rischio | Tempistiche del MoH per Autorizzazione all'immissione in commercio | Tempistiche del MoH per Rinnovo / Variazione | ||
|---|---|---|---|---|---|
| Processo di classificazione (Giorni). | Processo di Valutazione (Giorni) | Processo di classificazione (Giorni). | Processo di Valutazione (Giorni) | ||
| Classe A | Basso Rischio | 7 | 45 | 7 | 45 |
| Classe B | Rischio Basso Moderato | 7 | 90 | 7 | 45 |
| Classe C | Rischio moderato – alto | 7 | 100 | 7 | 45 |
| Classe D | Rischio Elevato | 7 | 120 | 7 | 45 |
Freyr Competenza
- Due Diligence normativa
- Registrazione dei dispositivi
- Test in loco
- Licenze per Distributori
- Legalizzazione e Autenticazione
- Rappresentante Legale
- Supporto per il Labelling
- Supporto per la traduzione
- Identificazione e qualificazione del distributore
- Servizi di sorveglianza post-commercializzazione
- Gestione delle modifiche post-approvazione
- Servizi di rinnovo e trasferimento della licenza
- Servizi di sottomissione e collegamento


