Panoramica sulla Registrazione dei Dispositivi Medici in Nuova Zelanda
I dispositivi medici in Nuova Zelanda sono regolamentati dalla New Zealand Medicines and Medical Devices Safety Authority (Medsafe) in base ai Regolamenti sui Medicinali del 1984, alla Legge sui Medicinali del 1981 e ai Regolamenti sui Medicinali (Database dei Dispositivi Medici) del 2003. Sebbene l'approvazione pre-commercializzazione non sia necessaria, è obbligatorio registrare i prodotti nel database del sistema di Notifica Elettronica Assistita via Web dei Dispositivi (WAND) entro 30 giorni dal lancio commerciale. Medsafe può richiedere documentazione che attesti la sicurezza e l'efficacia, come la certificazione rilasciata da organismi riconosciuti quali un Organismo Notificato dell'UE o Health Canada.
Il team di esperti normativi di Freyr per i dispositivi medici vanta una notevole esperienza nell'accompagnare le aziende di dispositivi medici attraverso il processo di registrazione Medsafe per i dispositivi medici in Nuova Zelanda.

Autorità Regolatoria: Autorità per la Sicurezza dei Dispositivi Medici (Medsafe)
Regolamentazione:Regolamento sui Medicinali (Database dei Dispositivi Medici), 2003
Legge sui Medicinali 1981
Regolamento sui Medicinali 1984
Percorso regolatorio: Sistema elettronico di notifica dei dispositivi assistita via web (WAND)
Rappresentante autorizzato: Sponsor di Dispositivi Medici
Requisito QMS: Certificazione ISO 13485:2016
Valutazione dei dati tecnici: Autorità per la Sicurezza dei Dispositivi Medici (Medsafe)
Validità della Licenza: Le registrazioni dei dispositivi in Nuova Zelanda non scadono. I dispositivi ritenuti una grave minaccia per la salute pubblica possono essere ritirati dal mercato.
Requisiti di etichettatura: Regolamento 12(4) dei Regolamenti sui Medicinali 1984 e GHTF/SG1/N43:2005
Formato di sottomissione: Sistema elettronico di notifica dei dispositivi assistita via web (WAND)
Lingua: Inglese
Classificazione dei Dispositivi Medici in Nuova Zelanda
In Nuova Zelanda, i dispositivi medici sono classificati per rischio nelle Classi I, IIa, IIb, III e AIMD in conformità ai criteri dell'International Medical Device Regulators Forum (IMDRF). Questa classificazione influisce sulla quantità di controllo normativo necessario. La classificazione si basa su caratteristiche quali lo scopo previsto del dispositivo, la durata del contatto con il corpo, l'invasività e se è attivo o inattivo. I dispositivi di classe superiore sono soggetti a una supervisione normativa più rigorosa. Medsafe è l'ente normativo in Nuova Zelanda che supervisiona queste classificazioni e regolamentazioni.
| Classificazione dei dispositivi medici Medsafe diversa dalla classe IVD | Rischio |
|---|---|
| Classe I Base | Basso Rischio |
| Misurazione di Classe I. | Basso Rischio |
| Classe I sterile | Basso Rischio |
| Classe IIa | Rischio basso-medio |
| Classe IIb | Rischio medio-alto |
| Classe III e Dispositivo medico impiantabile attivo (AIMD) | Rischio elevato |
| Classificazione IVD Medsafe | Rischio |
|---|---|
| A partire da luglio 2014, Medsafe non riconosce alcun sistema di classificazione del rischio per i dispositivi medico-diagnostici in vitro (IVD). Tutti gli IVD notificati a WAND devono utilizzare il codice di classificazione del rischio dell'IVD. Il Direttore Generale della Sanità ha autorizzato l'esenzione per gli IVD ai sensi dell'Allegato 1, paragrafo (i) del Regolamento sui Medicinali (Database dei Dispositivi Medici) del 2003. Tuttavia, i fornitori di IVD possono notificare volontariamente i loro dispositivi al database. | |
Rappresentante Autorizzato/Sponsor per dispositivi medici
Il Rappresentante Autorizzato è denominato Sponsor e agisce come intermediario tra il fabbricante e Medsafe. Gli Sponsor fungono da rappresentanti regolatori per i prodotti commercializzati in Nuova Zelanda, presentando le domande WAND e agendo come punto di contatto principale tra il fabbricante e Medsafe per tutte le questioni relative al prodotto. Inoltre, Medsafe ritiene lo Sponsor responsabile per le attività di vigilanza.
Registrazione dei Dispositivi Medici in Nuova Zelanda
La procedura di registrazione dei dispositivi medici in Nuova Zelanda e la procedura di quotazione WAND in Nuova Zelanda variano in base alla classe del dispositivo.
Dispositivi di Classe I- Per le apparecchiature di Classe I non sterili e non di misurazione è richiesta una dichiarazione di conformità del produttore; tuttavia, raramente viene presentata a un organismo di regolamentazione. Invece, lo sponsor (o fornitore) deve inserire i dettagli del dispositivo nel database WAND (Web Assisted Notification of Devices) come parte del processo di notifica Medsafe.
Dispositivi di altre classi
In Nuova Zelanda, gli sponsor o i fornitori hanno il compito di garantire che i dispositivi medici soddisfino standard come la ISO 13485:2016. La presentazione diretta di una Dichiarazione di Conformità, della certificazione SGQ o di prove di fabbricazione a Medsafe non è solitamente richiesta. Tuttavia, conservare questa documentazione è fondamentale per dimostrare la conformità su richiesta.
Medsafe privilegia la sorveglianza post-commercializzazione rispetto a un'approvazione pre-commercializzazione dettagliata per i dispositivi medici. Sebbene gli audit non siano condotti di routine durante la fase di notifica, Medsafe può avviarli per dispositivi a rischio più elevato o a seguito di attività di vigilanza e segnalazioni di eventi avversi, garantendo la sicurezza e la conformità continue.
Una volta che un dispositivo è notificato tramite il database WAND, può essere commercializzato in Nuova Zelanda, a condizione che il fornitore rispetti costantemente i regolamenti di Medsafe. Ciò richiede una conformità continua, in particolare con gli standard di monitoraggio post-commercializzazione e di segnalazione degli incidenti. Gli esperti di dispositivi medici di Freyr supportano i servizi relativi alla gestione di questi requisiti normativi, garantendo che le aziende mantengano la conformità per tutto il ciclo di vita del prodotto.
Flusso del processo
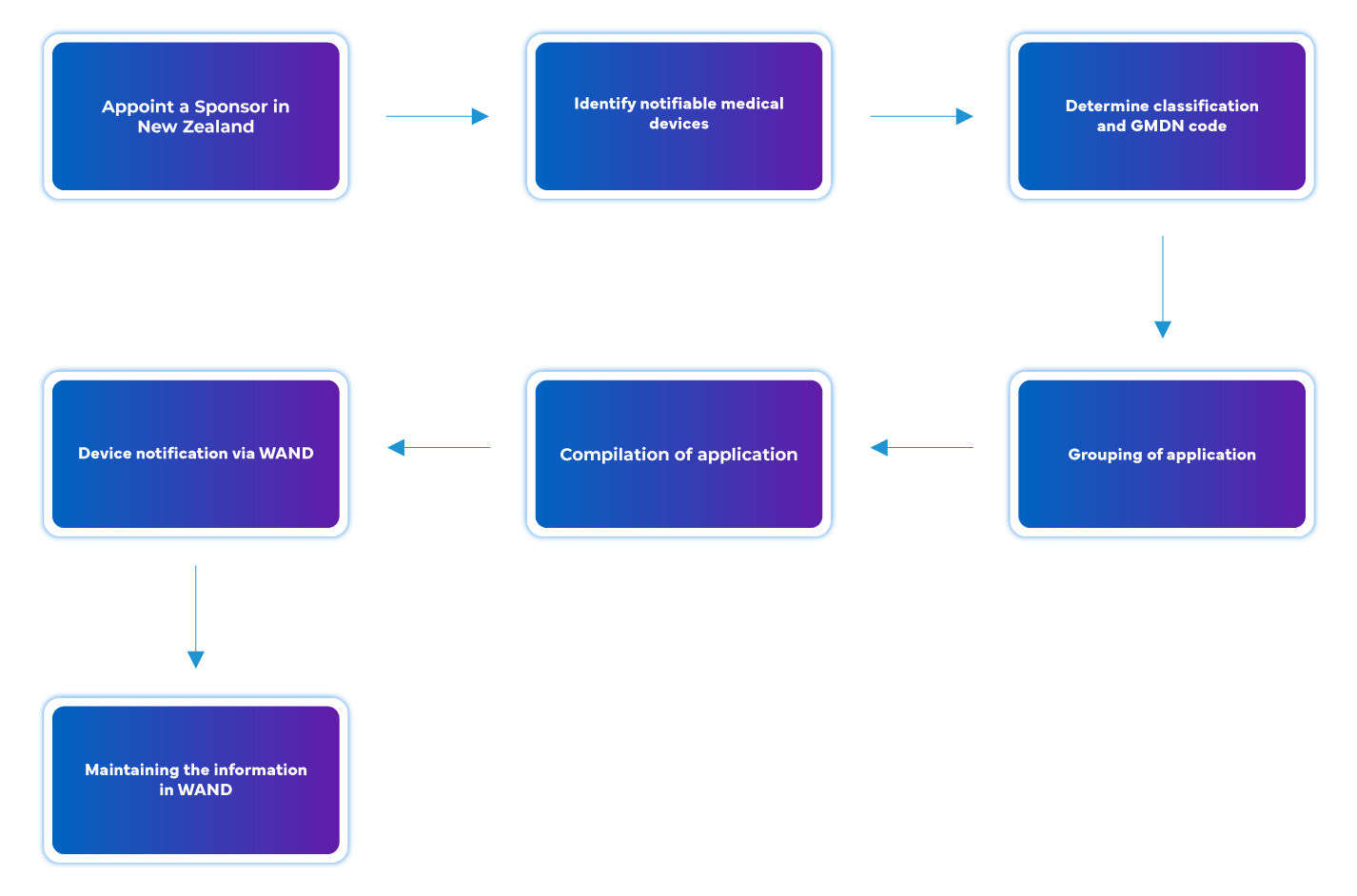
Gestione del ciclo di vita del dispositivo post-approvazione
Freyr supporta i produttori esteri nella gestione End-to-End del ciclo di vita dei dispositivi medici, incluse le attività post-approvazione, notificando le Autorità della Nuova Zelanda tramite WAND, quali –
- Gestione delle modifiche post-approvazione - modifiche alle approvazioni esistenti dei dispositivi medici come l'aggiunta di nuove varianti, accessori; l'aggiunta di nuove indicazioni d'uso, tra gli altri.
- Mantenimento delle approvazioni e delle registrazioni.
Dotata di un team di professionisti della regolamentazione, Freyr offre un supporto completo ai produttori per mantenere gli standard di qualità e sicurezza richiesti per l'approvazione del mercato. Gli specialisti di intelligence normativa dell'azienda monitorano meticolosamente gli aggiornamenti delle normative, assicurando che i clienti siano ben informati sulle azioni necessarie per mantenere la conformità dei loro prodotti agli standard attuali.
Riepilogo
| Rischio | Classe del Dispositivo | Audit QMS | Percorso Regolatorio | Tempistiche di Medsafe | Validità della Registrazione (anni) |
|---|---|---|---|---|---|
| Basso Rischio | Classe I Base | Conformità ISO 13485:2016 Nota: Medsafe non richiede audit del QMS ma raccomanda vivamente di seguire la ISO 13485:2016 per la qualità e la sicurezza. Medsafe ha l'autorità di condurre audit del QMS per qualsiasi classe di dispositivi qualora sorgano preoccupazioni relative alla sicurezza o alla qualità. | Registrazione WAND (Notifica) | 1 settimana |
Nessuna data di scadenza |
| Basso Rischio | Classe I con funzione di misurazione | Registrazione WAND (Notifica) | |||
| Basso Rischio | Classe I sterile | Registrazione WAND (Notifica) | |||
| Rischio basso-medio | Classe IIa | Registrazione WAND (Notifica) | |||
| Rischio medio-alto | Classe IIb | Registrazione WAND (Notifica) | |||
| Rischio elevato | Classe III | Registrazione WAND (Notifica) |
Nota: Secondo la legislazione attuale, le registrazioni dei dispositivi in Nuova Zelanda non scadono, ma i dispositivi che sono considerati a rischio inaccettabile per il pubblico possono essere ritirati dal mercato. Tuttavia, la legislazione attuale potrebbe essere rivista entro il 2026/2027.
Freyr Competenza
- Supporto completo per la registrazione dei dispositivi medici.
- Supporto LR
- Registrazione WAND
- Supporto all'etichettatura
- Gestione delle modifiche post-approvazione
- Trasferimento della licenza
- Servizi di sottomissione e collegamento con WAND

