Descrizione delle attività (SOW) per la presentazione della domanda 510(k) relativa a dispositivi medici attivi e dispositivi medici non attivi – Panoramica
In Freyr, il nostro team di esperti raccoglie e sintetizza con cura le informazioni più recenti e indispensabili per le vostre richieste 510(k), sia per i dispositivi medici attivi che per quelli non attivi. Questo vi garantisce di disporre delle conoscenze necessarie per orientarvi con sicurezza nel quadro normativo. Dal chiarimento delle differenze tra dispositivi attivi e non attivi all'approfondimento delle complessità della presentazione 510(k), abbiamo creato un ampio archivio di risorse a cui potrete fare riferimento. Intraprendete un percorso per padroneggiare la presentazione 510(k) per i dispositivi medici attivi e quella per i dispositivi medici non attivi con la nostra guida completa.
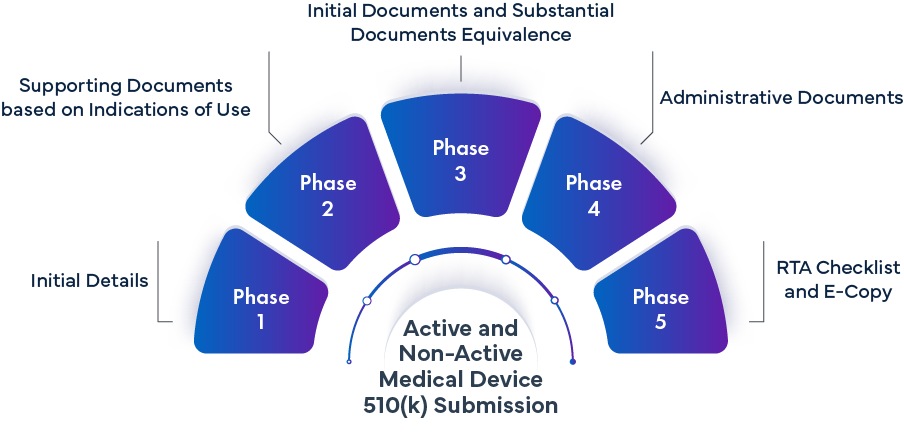
Fase -1 Dettagli Iniziali | ||
|---|---|---|
Requisiti | Ambito di applicazione del richiedente 510(k) | Ambito di Freyr |
| Destinazione d'uso |
|
|
| Dichiarazione delle indicazioni d'uso (Modulo 3881) |
|
|
| Descrizione del Dispositivo |
|
|
| Norme e Linee guida |
|
|
| Dispositivo di riferimento |
|
|
| Sintesi della procedura 510(k) |
|
|
Fase 2: Documentazione a supporto basata sulle indicazioni d'uso | |||
|---|---|---|---|
Requisiti dei documenti | Ambito di applicazione del richiedente 510(k) | Ambito di Freyr | |
| 2.1 | Disegno del Dispositivo | Inviare il fascicolo dei disegni del dispositivo per garantire una rappresentazione accurata del design del dispositivo. | Avviare una richiesta formale per un disegno del dispositivo di un dispositivo attivo. Esaminare attentamente e documentare meticolosamente le informazioni necessarie per la presentazione 510(k). |
| 2.2 | Progettazione e Sviluppo del dispositivo | Inviare il fascicolo di progettazione e sviluppo del dispositivo attivo, che comprende tutte le informazioni e la documentazione pertinenti. | Inviare una richiesta per la progettazione e lo sviluppo di un dispositivo attivo. Esaminare attentamente e documentare meticolosamente tutte le informazioni necessarie in preparazione della presentazione 510(k). |
| 2.3 | Scheda di dati di sicurezza del materiale | Fornire le Schede di Dati di Sicurezza (MSDS) per i componenti essenziali del dispositivo attivo, garantendo informazioni complete sulla loro sicurezza e composizione. | Inviare una richiesta per la scheda di dati di sicurezza dei materiali dei componenti cruciali del dispositivo attivo. Esaminare attentamente e documentare meticolosamente tutte le informazioni necessarie in preparazione della presentazione 510(k). |
| 2.4 | Diagramma di flusso di produzione | Fornire un diagramma di flusso di produzione che dettagli il processo di produzione del dispositivo attivo, fornendo una rappresentazione visiva delle fasi di produzione e della loro sequenza | Inviare una richiesta per la Scheda di Dati di Sicurezza (MSDS) dei componenti essenziali per il dispositivo attivo. Esaminare attentamente e documentare meticolosamente tutte le informazioni necessarie in preparazione della presentazione 510(k). |
| 2.5 | Descrizione del Dispositivo | Fornire dettagli completi, inclusi: o Una panoramica del dispositivo o Funzioni e modalità operative o Diagrammi a blocchi o Fotografie, cavi e accessori pertinenti o Interoperabilità del dispositivo. o Descrizione dell'alimentazione elettricaTop of Form | Inviare una richiesta per informazioni dettagliate sul dispositivo. Esaminare attentamente e documentare meticolosamente tutte le informazioni necessarie in preparazione della presentazione 510(k). |
| 2.6 | Labelling Proposto | Fornire le Istruzioni per l'Uso (IFU), il Manuale Utente e qualsiasi materiale promozionale associato per il dispositivo attivo. | Inviare una richiesta per le Istruzioni per l'Uso (IFU), il Manuale Utente e qualsiasi materiale promozionale, se disponibile. Esaminare l'IFU, il Manuale utente e il materiale promozionale forniti dal richiedente. Documentare le istruzioni per l'uso (IFU), il manuale utente e il materiale promozionale ai fini della presentazione 510(k). |
| 2.7 | Imballaggio e Trasporto | Fornire i piani di studio e i rapporti per la validazione dell'imballaggio e del trasporto. | Inviare una richiesta per il piano di studio e i rapporti relativi alla convalida dell'imballaggio e del trasporto. Esaminare i piani di studio e le relazioni per la convalida dell'imballaggio e del trasporto e fornire eventuali correzioni o feedback necessari. |
| 2.8 | Sterilizzazione (Se la sterilità è applicabile) | Fornire i piani di studio e i rapporti per la validazione della sterilizzazione. | Inviare una richiesta per il piano di studio e i rapporti di convalida della sterilizzazione. Esaminare attentamente e documentare meticolosamente tutte le informazioni necessarie in preparazione della presentazione 510(k). |
| 2.9 | Test di Prestazione al Banco | Avviare una richiesta formale per i piani e i rapporti degli studi di banco sui test di performance, delineando i requisiti e gli obiettivi specifici da affrontare. | Inviare una richiesta per i piani e i rapporti dello studio di laboratorio (Bench Study) del dispositivo attivo per i test di performance. Esaminare attentamente e documentare meticolosamente tutte le informazioni necessarie in preparazione della presentazione 510(k). |
Documentazione di Supporto per la Compatibilità Elettromagnetica e la Sicurezza Elettrica | |||
| 2.10 | Caratteristiche del dispositivo relative alla CEM e ambienti di utilizzo previsto | Fornire dettagli sulle caratteristiche del dispositivo relative alla compatibilità elettromagnetica (EMC) e sugli ambienti di utilizzo previsti, inclusi: o Una panoramica del dispositivo. o Funzioni e modalità operative. o Diagrammi a blocchi. o Fotografie, cavi e accessori pertinenti. o Interoperabilità del dispositivo. o Descrizione dell'alimentazione elettrica, inclusa la fattibilità dell'utilizzo del dispositivo medico alimentato internamente durante la ricarica. o Ambienti in cui il dispositivo medico è destinato all'uso. o Descrizione di qualsiasi tecnologia wireless (se applicabile) per considerazioni aggiuntive sui dispositivi medici con funzionalità wireless. o Descrizione di eventuali emettitori RF interni al dispositivo medico che potrebbero causare disturbi elettromagnetici. o Affrontare gli emettitori elettromagnetici (EM) comuni e gli emettitori medici unici.
| Inviare una richiesta di informazioni sulle caratteristiche del dispositivo relative all'EMC e agli ambienti di utilizzo previsti. Esaminare attentamente e documentare meticolosamente tutte le informazioni necessarie in preparazione della presentazione 510(k). |
| 2.11 | Valutazione del Rischio | Fornire un Piano di Gestione del Rischio che includa una valutazione del rischio che dimostri un'efficace mitigazione del rischio, insieme a un rapporto completo sulla gestione del rischio che comprenda tutti gli elementi di rischio. Fornire il documento revisionato con le correzioni e i miglioramenti suggeriti | Inviare una richiesta per il fascicolo di gestione del rischio e la documentazione del piano e del rapporto di gestione del rischio, inclusa l'identificazione dei pericoli, la valutazione del rischio e la dimostrazione di un'adeguata mitigazione del rischio. Il rapporto di gestione del rischio dovrebbe coprire tutti gli elementi di rischio, preferibilmente con sezioni separate per chiarezza. Fornire un modello del Piano di Gestione del Rischio e del Rapporto di Gestione del Rischio che comprenda tutti i rischi legati al dispositivo su richiesta del richiedente. Esaminare i dati nel Fascicolo di Gestione del Rischio, inclusi il Piano e la Relazione condivisi dal richiedente, e fornire suggerimenti per le correzioni necessarie al fine di garantire una documentazione completa per la presentazione 510(k). Esaminare attentamente e documentare meticolosamente tutte le informazioni necessarie in preparazione della presentazione 510(k). |
| 2.12 | Norma di consenso | Fornire conferma degli standard di consenso pertinenti e una spiegazione di eventuali deviazioni dagli standard riconosciuti dalla FDA. | Inviare una richiesta per gli standard di consenso applicabili relativi all'EMC e alla sicurezza elettrica per il dispositivo attivo. Documentare gli standard di consenso confermati per il dispositivo attivo ai fini della presentazione 510(k). |
| 2.13 | Criteri di superamento/fallimento per prestazioni essenziali e immunità | Presentare il piano di studio e i rapporti relativi ai test di Prestazione Essenziale e Immunità condotti sul dispositivo attivo, in conformità con gli standard riconosciuti dalla FDA. | Presentare una richiesta per il piano di studio e i rapporti dei test di Prestazione Essenziale e Immunità condotti sul dispositivo attivo, in conformità con gli standard riconosciuti dalla FDA. Esaminare attentamente e documentare meticolosamente tutte le informazioni necessarie in preparazione della presentazione 510(k). |
| 2.14 | Configurazione e Funzioni Testate dei Dispositivi Medici | Fornire la configurazione del dispositivo medico e le funzioni testate per il dispositivo attivo, che comprende i seguenti dettagli: o Fornire una descrizione completa del dispositivo medico in esame, includendo informazioni dettagliate sulla sua configurazione, funzioni, modalità e le impostazioni specifiche che sono state testate. o La descrizione del dispositivo in esame dovrebbe includere il nome del dispositivo medico, il numero di modello e indicare se il dispositivo è il prodotto medico finale pronto per la produzione attualmente in fase di revisione. | Inviare una richiesta per la configurazione e le funzioni di test del dispositivo medico attivo. Esaminare attentamente e documentare meticolosamente tutte le informazioni necessarie in preparazione della presentazione 510(k). |
| 2.15 | Risultati delle prove EMC | Fornire il piano di studio e il rapporto sui test EMC (Compatibilità Elettromagnetica) in conformità con lo standard di consenso riconosciuto dalla FDA e raccomandato per il dispositivo attivo. | Avviare una richiesta formale per il piano di studio e il rapporto sui test EMC, allineato allo standard di consenso riconosciuto dalla FDA e raccomandato per i dispositivi attivi. Esaminare attentamente e documentare meticolosamente tutte le informazioni necessarie in preparazione della presentazione 510(k). |
Fase 3 – Documenti iniziali e documenti di equivalenza sostanziale | |||
|---|---|---|---|
Requisiti dei documenti | Ambito di applicazione del richiedente 510(k) | Ambito di Freyr | |
| 3.1 | Foglio di Copertina per la Presentazione della Revisione Preliminare di CDRH (Modulo FDA 3514) | - | Completare il Modulo FDA 3514 utilizzando i dettagli forniti dal richiedente |
| 3.2 | Riepilogo e Certificazione di Classe III | - | Questo passaggio non è necessario se gli studi clinici non sono richiesti |
| 3.3 | Certificazione finanziaria o Dichiarazione di divulgazione | - | Questo passaggio non è necessario se gli studi clinici non sono richiesti |
| 3.4 | Riepilogo esecutivo | - | Sviluppare un modello e preparare meticolosamente il documento. Fornire giustificazioni per eventuali discrepanze osservate tra il dispositivo proposto e il dispositivo di riferimento. Se viene scelto uno studio comparativo tra il dispositivo proposto e il dispositivo di riferimento, creare un modello e preparare il documento corrispondente. |
| 3.5 | Discussione sull'Equivalenza Sostanziale | - | Sviluppare un modello e preparare meticolosamente il documento. Se viene scelto uno studio comparativo tra il dispositivo proposto e il dispositivo di riferimento, creare un modello e preparare il documento corrispondente. |
Fase 4 – Documenti amministrativi | |||
|---|---|---|---|
Requisiti dei documenti | Ambito di applicazione del richiedente 510(k) | Ambito di Freyr | |
| 4.1 | Lettera di accompagnamento 510(k) | Firmare il documento stampato su carta intestata dell'azienda e organizzare la spedizione di una copia cartacea all'ufficio US. Fornire una copia digitale della lettera di accompagnamento 510(k) firmata per l'inclusione nella documentazione 510(k). | Preparare un modello completo che includa tutti i dettagli necessari per la lettera di accompagnamento e fornirlo al richiedente. Istruire il richiedente a utilizzare la propria carta intestata ufficiale e assicurarsi che la lettera di accompagnamento sia firmata da una persona autorizzata |
| 4.2 | Dichiarazione di Veridicità e Accuratezza | Assicurarsi che il documento sia firmato dalla persona di contatto designata presso l'azienda e fornito di conseguenza. | Sviluppare un modello completo contenente tutti i contenuti necessari da includere nel documento di presentazione. |
| 4.3 | Dichiarazioni di conformità e Rapporto riepilogativo | Assicurarsi che il documento sia firmato dalla persona di contatto designata presso l'azienda e fornito di conseguenza. | Sviluppare un modello completo per elencare e preparare sistematicamente i documenti richiesti. |
| 4.4 | MDFUSC (Modulo FDA 3601) | Effettuare il pagamento richiesto alla FDA prima della presentazione formale del fascicolo 510(k). | Generare un foglio di copertura per la tassa utente e un numero di identificazione personale (PIN) univoco specificamente per la presentazione del dispositivo medico. |
Fase 5 – Lista di controllo RTA ed eCopy | |||
|---|---|---|---|
Requisiti dei documenti | Ambito di applicazione del richiedente 510(k) | Ambito di Freyr | |
| 5.1 | Checklist RTA | Approvazione per la verifica della Checklist RTA (Ready to Accept), che indica che tutti i requisiti sono stati soddisfatti con successo. | Sviluppare un modello di lista di controllo RTA personalizzato adattato al tipo specifico di presentazione. Completare la checklist compilando meticolosamente tutti i campi richiesti e assicurandosi che i documenti menzionati siano debitamente presentati alla FDA e condivisi con il richiedente. |
| 5.2 | Copia elettronica | Approvazione per la documentazione contenuta nella Cartella di Presentazione Finale, che ne attesta la conformità a tutti i requisiti e gli standard necessari. | Organizzare le sezioni della cartella di presentazione in conformità con la guida FDA e condividerle tempestivamente con il richiedente. Convertire il fascicolo di presentazione in una copia elettronica per un facile accesso e revisione. Inviare la copia elettronica della presentazione all'agente US designato. |
Registrazione dei Dispositivi Medici
- Strategia normativa US FDA completa
- Identificazione del dispositivo di riferimento
- Stabilire l'Equivalenza Sostanziale con il Dispositivo Predicato
- Analisi delle lacune per la conformità alla US FDA
- Compilazione di 21 sezioni del Fascicolo Tecnico 510(k)
- Pubblicazione e creazione di eCopy
- Convalida e presentazione dell'eCopy
- Servizi di collegamento per l'approvazione dei dispositivi.
- Gestione della risposta RTA e delle carenze
- Servizi di consulenza per affrontare le carenze
- Registrazione del dispositivo e manutenzione del database FURLS

- Aver gestito numerose registrazioni 510(k) per diverse categorie di dispositivi
- Team di esperti per la compilazione 510(k) secondo i requisiti della Notifica Premarket (510(k)) della US FDA.
- Supporto aggiuntivo per la gestione delle domande relative al 510(k)
- Consigli per il tipo adatto di 510(k) secondo i requisiti di presentazione 510(k) della US FDA per il dispositivo
- Presentazione puntuale dei documenti
- Aggiornato con i nuovi emendamenti US FDA

