Servizi di regolamentazione farmaceutica in Cile – Panoramica
Il mercato farmaceutico cileno è regolamentato dall'Instituto de Salud Pública de Chile (ISP), che sovrintende all'autorizzazione, alla registrazione e alla sorveglianza dei medicinali. Tutti i prodotti farmaceutici devono essere registrati prima della vendita, al fine di garantire che soddisfino gli standard di qualità, sicurezza ed efficacia stabiliti dalle linee guida internazionali.
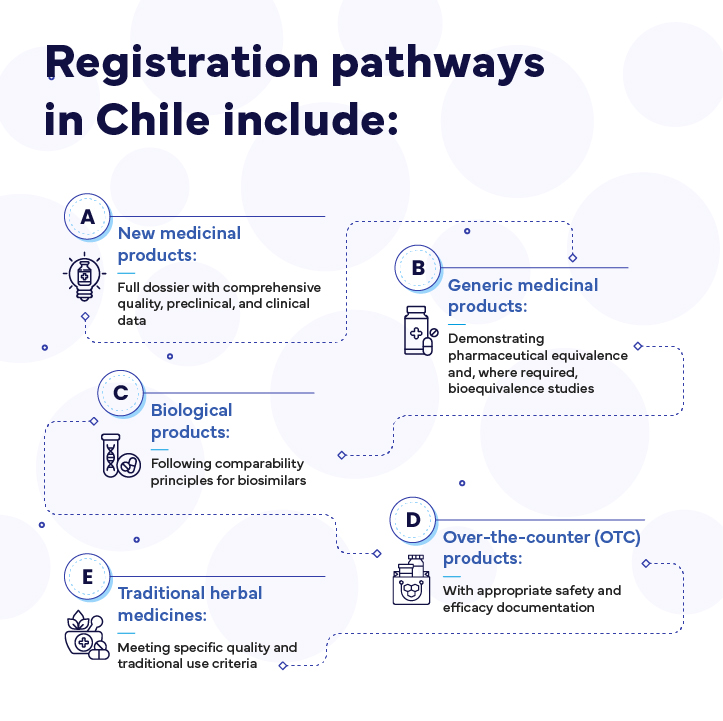
Le modalità di registrazione in Cile comprendono:
Tra i requisiti principali figurano la documentazione in spagnolo, i certificati con apostille rilasciati nel paese d'origine, un titolare registrato in Cile e i certificati di conformità alle norme GMP. Per determinati principi attivi, come indicato dall'ISP, sono richiesti studi di bioequivalenza.
Il quadro normativo richiede competenze specifiche in materia di procedure di presentazione delle domande, documentazione e conformità a livello locale. produttori stranieri produttori complesse procedure amministrative, garantendo al contempo il rispetto delle norme cilene in materia di etichettatura, farmacovigilanza e qualità.
Freyr offre un supporto normativo completo alle aziende farmaceutiche che intendono ottenere l'autorizzazione all'immissione in commercio in Cile, dalla pianificazione strategica alla gestione del ciclo di vita del prodotto dopo l'approvazione.
Servizi di regolamentazione farmaceutica in Cile - L'esperienza di Freyr
Strategia di registrazione e preparazione del fascicolo
- Preparazione di fascicoli in formato CTD per le richieste di autorizzazione all'immissione in commercio
- Valutazione/i del percorso (innovativo, generico, biosimilare)
- Informazioni normative (RI) e analisi delle lacune
- Pianificazione delle prove per i moduli relativi alla qualità, alla fase preclinica e alla fase clinica
Servizi di rappresentanza locale
- Servizi per i titolari di registrazione con sede in Cile
- Relazioni con gli ISP e gestione della corrispondenza ufficiale
- Servizi di registrazione e conformità per gli stabilimenti produttivi
Documentazione e assistenza amministrativa
- Gestione dei certificati dei prodotti farmaceutici (CPP)
- Preparazione del certificato GMP e gestione dell'apostille
- Traduzione in spagnolo e autenticazione notarile di documenti normativi
- Preparazione e legalizzazione di procure
Servizi di bioequivalenza e qualità
- Pianificazione e supervisione degli studi di bioequivalenza
- Preparazione dei fascicoli giustificativi per le deroghe biologiche
- Supporto alla convalida dei metodi analitici
- Sviluppo del protocollo di stabilità e valutazione dei dati
Gestione delle richieste e del ciclo di vita
- Invio elettronico tramite piattaforme ISP
- Gestione delle risposte alle richieste e delle carenze
- Modifiche successive all'autorizzazione (CMC, etichettatura, amministrative, ecc.) e emendamenti
- Assistenza annuale per la manutenzione e il rinnovo
Conformità e farmacovigilanza
- Artwork dell'etichettatura e Artwork per il Cile
- Implementazione del sistema di farmacovigilanza
- Procedure di segnalazione degli eventi avversi (AE)
- Elaborazione del piano di gestione dei rischi (RMP)
La nostra sede in Cile
Av. Manquehue n. 151,
, Uff. 1205, Las Condes,
, Cile

