Materiale promozionale: MLR - Panoramica
Il successo del lancio di un prodotto e un ingresso efficace sul mercato di medicinali o dispositivi medici dipendono dalla sinergia tra un reparto di Affari regolatori e promozionali altamente competente e un solido processo di revisione in ambito medico, legale e normativo (MLR). Questa sinergia è fondamentale per garantire la piena conformità in materia di pubblicità, etichettatura promozionale o diffusione di informazioni non promozionali relative agli affari medici.
Prevenire affermazioni fuorvianti, non compromettere la sicurezza dei pazienti e garantire una diffusione etica.
Ridurre al minimo i rischi legati alla mancata conformità, alle diffide o alle sanzioni e al danno d'immagine.
Garantisce l'accuratezza delle affermazioni relative alla sicurezza, all'efficacia o alle prestazioni del dispositivo e la loro fondatezza sulla base di prove scientifiche.
Coerenza e conformità con l'etichettatura del prodotto approvata e con le istruzioni per l'uso (IFU).
Rispetto delle linee guida stabilite dagli organismi di regolamentazione e dei codici deontologici del settore per i diversi paesi e regioni.
In Freyr, i nostri esperti in ambito medico e normativo, forti di un background clinico e biomedico senza pari, di competenze MLR e di esperienza in materia di affari regolatori promozionali in oltre 120 paesi, forniscono assistenza 24 ore su 24 per garantire la perfetta conformità delle vostre promozioni di marca, pubblicità, campagne di sensibilizzazione sulle patologie o iniziative senza marchio.
Servizi
- Verifica del rispetto delle linee guida specifiche per ciascun Paese stabilite dalle autorità di regolamentazione quali FDA, EMA, EU MDR, MHRA, TGA, HSA, PMDA, ANVISA, Health Canada e altre.
- Confermare il rispetto delle linee guida specifiche per ciascun Paese relative alle leggi anti-corruzione e ai codici etici del settore, quali FTC, PhRMA, EFPIA, ABPI, PAAB, TGA, Medicines New Zealand, ANVISA, ANAMED, IFPMA, AIFA, AEMPS, Mdeon e altri.
- Verificare il corretto utilizzo delle affermazioni e dei riferimenti. Le affermazioni devono essere suffragate da riferimenti pertinenti e adeguati e da prove scientifiche, e l'efficacia o la sicurezza non devono essere esagerate.
- Garantire un giusto equilibrio nella presentazione dei rischi e dei benefici del prodotto, compresi eventuali effetti collaterali o conseguenze derivanti dal suo utilizzo.
- Valutare il linguaggio, le immagini e gli altri elementi utilizzati nella presentazione delle informazioni per garantire chiarezza, accuratezza e l'assenza di informazioni fuorvianti per il pubblico di destinazione.
- Verificare che gli elementi grafici e di sfondo siano in linea con il contenuto per evitare discrepanze (ad esempio, assicurandosi che le immagini relative alla popolazione pediatrica non vengano utilizzate in contesti in cui il prodotto non è prescritto per tale popolazione).
- Esattezza dei marchi commerciali e aziendali, dei marchi di servizio e delle certificazioni di conformità dei dispositivi, quali il marchio CE, UKCA mark, il marchio CCC e altri.
- Svolgere il ruolo di esperti in materia (SME) per le questioni normative durante le riunioni della PRC.
- Procedure relative alle richieste HA, quali l'OPDP/APLP 2253 o la verifica da parte dell'HA dei materiali promozionali.
- Documentazione relativa alla pubblicità e all'etichettatura promozionale presentata alle autorità sanitarie, comeForm 2253 APLB Form 2253 FDA US ,FDA formato cartaceo ed eCTD.
Il nostro team è altamente innovativo ed è in grado di sviluppare contenuti per qualsiasi piattaforma o canale; pertanto, la nostra offerta e la nostra competenza non si limitano a quanto sopra menzionato: possiamo fare molto di più!
- Esaminare i contenuti relativi al farmaco, comprese le indicazioni, il dosaggio, le istruzioni per l'uso e il meccanismo d'azione, per garantirne l'adeguatezza e l'accuratezza in conformità con l'etichettatura approvata del prodotto, le informazioni sulla prescrizione (PI), SmPC, i foglietti illustrativi (PIL) e le istruzioni per l'uso (IFU), e assicurarsi che siano supportati da adeguate prove cliniche e scientifiche.
- Valutare l'allineamento del materiale promozionale con le attuali linee guida di trattamento e gli standard di cura all'interno della specifica area terapeutica.
- Personalizzazione dei punti di controllo della revisione per adattarli alle aree terapeutiche con linee guida o regolamenti per le attività promozionali, come l'oncologia o le malattie rare.
- Garantire un "giusto equilibrio" tra la presentazione dei rischi e dei benefici nel materiale promozionale, riflettendo accuratamente i potenziali svantaggi accanto ai vantaggi.
- Le sperimentazioni cliniche e altri dati scientifici accurati e attendibili confermano adeguatamente tali affermazioni.
- Verificare che le affermazioni comparative rispetto ad altri prodotti siano supportate da dati validi e attendibili.
- Assicurarsi che la terminologia medica e i sinonimi siano scelti con cura per garantire una comunicazione chiara.
- Assicurarsi che il pubblico di destinazione sia quello appropriato (ad esempio, operatori sanitari, pazienti, caregiver) e che i materiali siano adattati al loro livello di comprensione e alle loro esigenze.
- Collaborare con team interfunzionali al processo MLR (Global to Local) specifico per ciascun Paese e alla valutazione dello scenario attuale nell’ambito del processo del Comitato di revisione promozionale (PRC), effettuare analisi delle lacune e individuare le aree da ottimizzare e armonizzare.
- Definizione delle procedure operative standard (SOP), delle istruzioni di lavoro per MLR e degli indicatori chiave di prestazione (KPI) per misurare l'efficienza dei processi.
- Esperienza nella definizione dei flussi di lavoro dei processi MLR per sistemi LCM quali Veeva PromoMats MedComms.
- Facilitare la MLR e il processo PRC per gli annunci pubblicitari e i materiali promozionali e non promozionali nei sistemi LCM quali Veeva PromoMats, Veeva MedComms, Pepperflow, ecc.
- Redigere e distribuire gli ordini del giorno delle riunioni alle parti interessate, partecipare alle riunioni del PRC e redigere i verbali e le decisioni prese dal PRC.
- Inviare il materiale promozionale e pubblicitario ai recensori in modo tempestivo e secondo un ordine di priorità.
- Pianificare e gestire tutte le riunioni con le parti interessate relative alla fase di ideazione, alla fase preliminare alla presentazione e alla fase di revisione una volta il progetto online.
- Tenere traccia delle approvazioni relative alla revisione dei materiali e assicurarsi che le modifiche siano state integrate correttamente.
- Garantisce che il materiale pubblicitario e promozionale soddisfi i criteri necessari per essere inviato.
Revisione MLR dei Materiali Promozionali
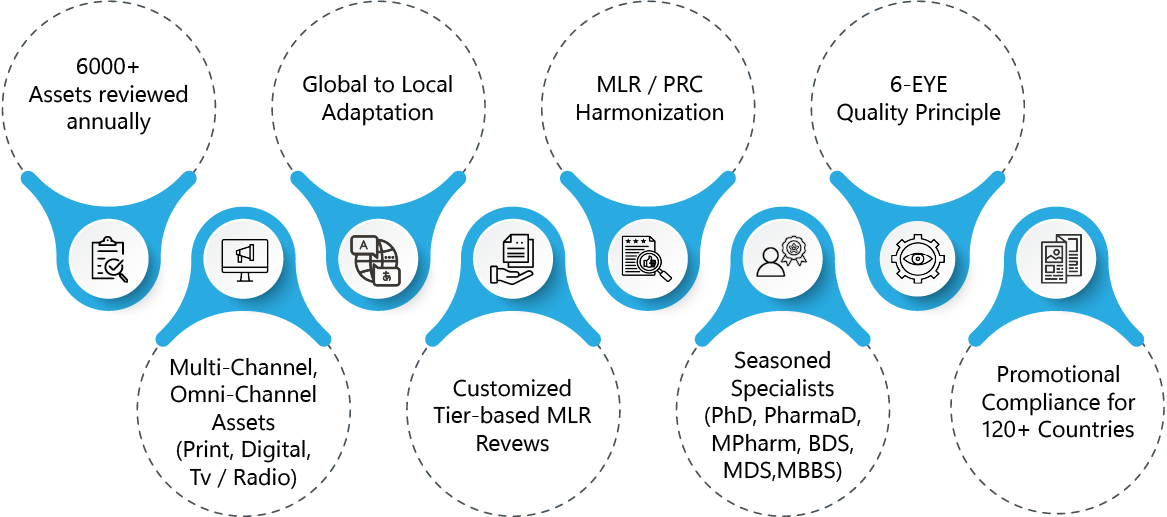
- Oltre 6000 risorse sottoposte a verifica ogni anno ai fini MLR
- Esperienza nell'adattamento delle risorse promozionali dal livello globale a quello locale e nell'armonizzazione dei processi MLR
- Il principio dei "6 punti chiave" per una verifica più accurata della conformità normativa, adattato alle complessità dell'area terapeutica
- MLR : competenza in una vasta gamma di materiali pubblicitari, promozionali e non promozionali per diversi canali di comunicazione – digitale, stampa, TV/radio
- MLR personalizzata e strutturata in livelli in base alla complessità degli asset
- Specialisti in conformità promozionale e MLR con esperienza nel settore e formazione clinica/biomedica (PharmaD, PhD, Mpharm, BDS, MDS, MBBS)
- Consulenza strategica specifica per ogni regione in materia di conformità del materiale promozionale per oltre 120 paesi.
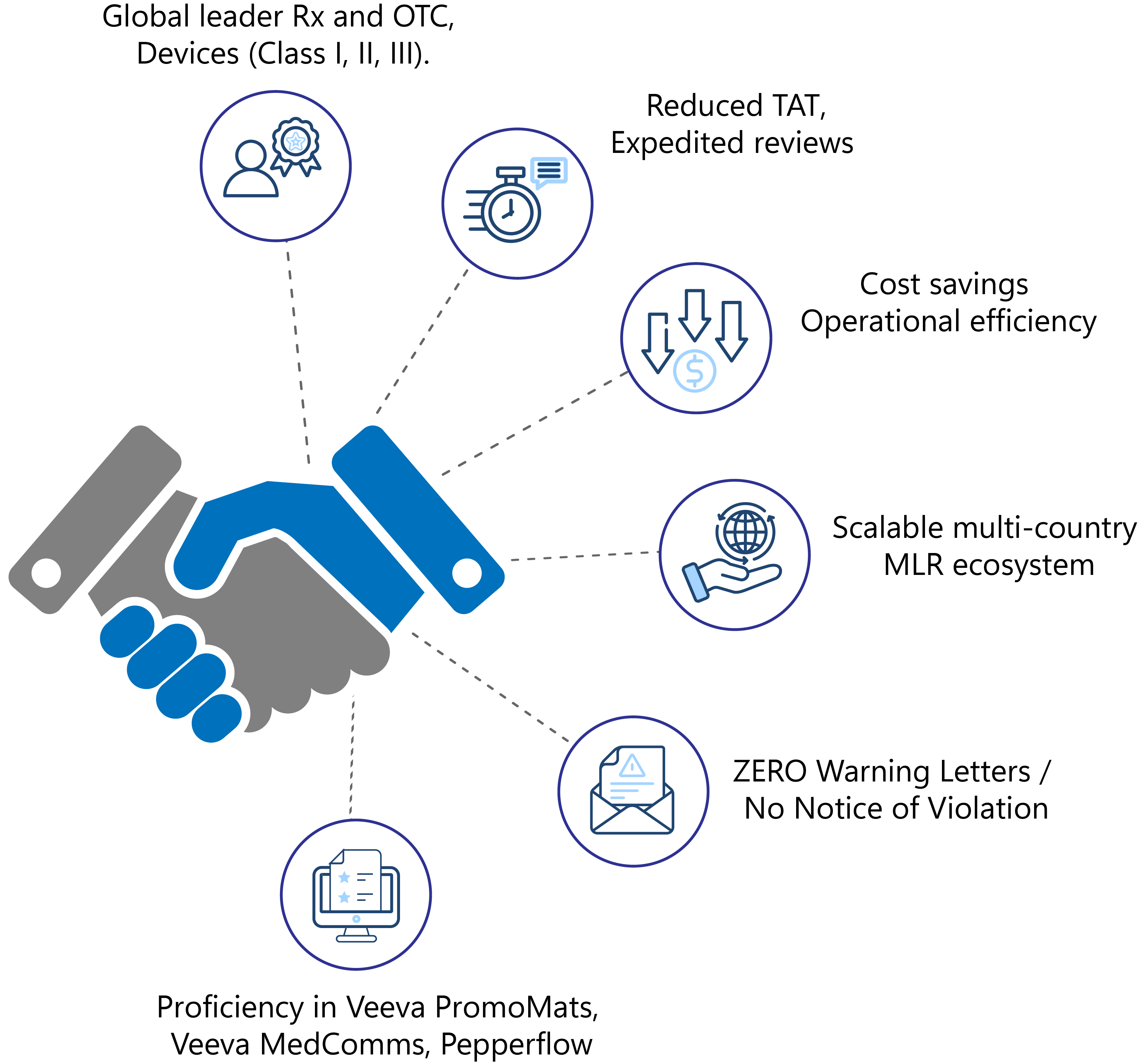
- Leader mondiale nei settori farmaceutico, biofarmaceutico (farmaci soggetti a prescrizione medica e OTC) e dei dispositivi medici (Classi I, II, III).
- Ridurre il tempo di ciclo complessivo per la revisione
- Riduzione del TAT con revisioni accelerate per rispettare le scadenze
- Notevoli risparmi sui costi e miglioramento dell'efficienza operativa
- Ecosistema MLR scalabile multi-paese
- Nessuna lettera di avvertimento / Nessuna notifica di violazione
- Ottima padronanza dei sistemi MLR quali Veeva PromoMats, Veeva MedComms, Pepperflow, ecc.