Servizi di Audit di Conformità e Validazione Farmaceutica
Sfruttate un decennio di esperienza con i nostri servizi attraverso valutazioni di conformità, audit meticolosi e robusti processi di convalida.
Esplora argomenti
- Cos'è la conformità, l'audit e la convalida nel settore farmaceutico?
- Qual è l'importanza della conformità, dell'audit e della convalida nell'industria farmaceutica?
- Principali sfide nell'ambito della conformità, dell'audit e della convalida
- Cosa sono gli Audit GxP?
- Comprendere gli Audit da remoto
- Cos'è la convalida dei sistemi informatici (CSV) e perché è fondamentale nell'industria farmaceutica?
- In cosa differisce la CSV da Computer System Assurance (CSA)
- Quali sono i componenti di un programma CSA?
- Come contribuisce la CSA all'integrità dei dati nell'industria farmaceutica?
- Che ruolo svolge la conformità normativa nella CSA?
- In che modo un partner strategico per la conformità normativa può essere d'aiuto?
- Perché scegliere Freyr?
- I nostri servizi
Cos'è la conformità, l'audit e la convalida nel settore farmaceutico?
Ultimo aggiornamento: settembre 2024
Nel settore farmaceutico, i processi di conformità, audit e convalida sono fondamentali per garantire il rispetto degli standard normativi, l'integrità dei dati e la produzione di prodotti sicuri ed efficaci. La conformità implica l'allineamento delle operazioni con le normative di settore e le politiche interne. Gli audit, revisioni sistematiche, verificano la conformità, identificano le aree di miglioramento e mitigano i rischi. La convalida garantisce che sistemi, processi e attrezzature soddisfino costantemente i requisiti predefiniti.
Le aziende ricorrono alla consulenza di esperti per operare senza intoppi. I leader del settore gestiscono con competenza questi processi, garantendo il rispetto degli standard globali senza compromettere l'efficacia o la sicurezza dei prodotti. Con l'evoluzione del settore farmaceutico, gli approcci strategici in materia di conformità, audit e convalida diventano fondamentali per un successo duraturo. Attraverso l'attuazione di questi processi, le aziende soddisfano i requisiti normativi e promuovono una cultura dell'eccellenza e dell'innovazione in un settore dinamico e competitivo.
Collaborare con un partner affidabile per una guida strategica e soluzioni personalizzate che consentano alle vostre operazioni farmaceutiche di prosperare in un panorama normativo dinamico.

Qual è l'importanza della conformità, dell'audit e della convalida nell'industria farmaceutica?
Conformità, audit e convalida sono componenti fondamentali nell'industria farmaceutica, garantendo che i prodotti siano sicuri, efficaci e prodotti secondo gli standard normativi.
- Garantisce la Sicurezza e l'Efficacia del Prodotto: La conformità alle normative assicura che i prodotti farmaceutici soddisfino rigorosi standard di sicurezza ed efficacia prima di essere immessi sul mercato. Ciò implica rigorosi processi di test e convalida per confermare che i prodotti funzionino come previsto e non comportino rischi per i pazienti.
- Mantiene l'Adesione Normativa: Audit e convalide regolari aiutano le aziende ad aderire a normative complesse ed in evoluzione stabilite dalle autorità sanitarie. Ciò include la conformità alle Good Manufacturing Practice (GMP), alle Good Clinical Practice (GCP) e ad altri standard di settore, riducendo il rischio di sanzioni normative e richiami di prodotti.
- Migliora la Garanzia di Qualità: I processi di convalida, incluse le convalide di apparecchiature e sistemi, assicurano che i processi di produzione e test generino costantemente prodotti di alta qualità. Le verifiche (audit) accertano che questi processi siano seguiti correttamente, portando a una migliore qualità e affidabilità del prodotto.
- Favorisce l'accesso al mercato e rafforza la reputazione: pratiche efficaci di conformità e convalida favoriscono l'accesso al mercato dimostrando il rispetto dei requisiti normativi. Ciò rafforza la reputazione e la credibilità dell'azienda, instaurando un rapporto di fiducia con gli operatori sanitari, i pazienti e le autorità di regolamentazione.
- Facilita il Miglioramento Continuo: Le verifiche (audit) forniscono approfondimenti sull'efficienza dei processi e sulle aree di miglioramento, portando a un migliore controllo qualità e a pratiche operative. Questa valutazione e adeguamento continui aiutano a mantenere standard elevati e ad adattarsi ai cambiamenti nelle normative e nelle migliori pratiche del settore.
Principali sfide nell'ambito della conformità, dell'audit e della convalida
Il settore della conformità, audit e convalida affronta diverse sfide importanti che possono influenzare la capacità delle aziende farmaceutiche di soddisfare i requisiti regolatori e mantenere elevati standard di qualità e sicurezza:
| Sfida | Descrizione |
|---|---|
| Conformità Regolatoria | Le aziende farmaceutiche devono aderire a rigorose normative di agenzie come la FDA e l'EMA, che richiedono una documentazione rigorosa e misure di controllo qualità. La non conformità può portare a sanzioni severe, incluse multe e richiami di prodotti. |
| Controllo degli accessi e sicurezza | È fondamentale garantire che solo il personale autorizzato possa accedere ad aree e informazioni sensibili. Ciò comporta l'implementazione di sistemi avanzati di controllo degli accessi e il mantenimento della sicurezza informatica contro le minacce, il che può essere complesso e costoso. |
| Convalida del sistema informatico (CSV) | La convalida dei sistemi informatici utilizzati negli ambienti GxP è essenziale ma spesso onerosa e poco definita. Il processo richiede tempo e risorse significativi, specialmente quando un approccio standard viene applicato indiscriminatamente. |
| Formazione e sensibilizzazione dei dipendenti | Programmi di formazione continua sono necessari per garantire che i dipendenti comprendano i protocolli di conformità e la loro importanza. Una formazione inadeguata può portare a non conformità ed errori nei processi. |
| Documentazione e tenuta dei registri | Mantenere una documentazione accurata e completa è vitale per la conformità. Una documentazione inadeguata è un problema comune che può portare a osservazioni normative e fallimenti durante gli audit. |
| Integrità dei dati | Garantire l'integrità e l'accuratezza dei dati è fondamentale, specialmente nella gestione di grandi volumi di informazioni. Le sfide includono la gestione manuale dei dati e la necessità di sistemi robusti per la gestione dei dati. |
| Gestione dei Fornitori | La dipendenza da fornitori terzi per software e servizi richiede validazioni approfondite e controlli di conformità. Gestire queste relazioni e assicurarsi che soddisfino gli standard regolatori può essere impegnativo. |
| Complessità Tecnologica | La crescente complessità delle tecnologie, inclusi l'IA e i sistemi Cloud-based, presenta nuove sfide di validazione e richiede un adattamento continuo ai contesti normativi in evoluzione. |
| Controllo qualità inadeguato | Molte aziende farmaceutiche faticano a mantenere elevati standard di qualità in tutti i processi, il che può portare a contaminazione, contaminazione incrociata e altri problemi di qualità. |
| Miglioramento continuo e monitoraggio | Audit e ispezioni regolari sono essenziali per identificare le debolezze nei sistemi di conformità. Tuttavia, molte organizzazioni non riescono a implementare misure proattive per il miglioramento continuo. |
- Normative in Evoluzione: Tenere il passo con le normative e le linee guida in rapida evoluzione nelle diverse regioni può essere impegnativo. Le aziende farmaceutiche devono aggiornare continuamente le loro pratiche di conformità per aderire a standard normativi nuovi o rivisti, il che può richiedere risorse e aggiustamenti significativi.
- Complessità degli Standard Globali: Navigare tra i diversi e complessi requisiti normativi di paesi e regioni differenti aggiunge alla sfida. Ogni giurisdizione può avere il proprio insieme di regole e standard, rendendo difficile raggiungere una conformità coerente nei mercati globali.
- Integrità e sicurezza dei dati: Garantire l'integrità e la sicurezza dei dati durante i processi di conformità, audit e convalida è fondamentale. Le aziende devono implementare sistemi e controlli robusti per proteggere da violazioni dei dati, manomissioni o inesattezze, che possono avere gravi conseguenze per l'approvazione dei prodotti e la sicurezza dei pazienti.
- Vincoli di risorse: Risorse limitate, inclusi tempo, personale e budget, possono ostacolare l'efficacia delle attività di conformità e audit. Le aziende spesso faticano a bilanciare le esigenze di mantenimento della conformità con la necessità di allocare risorse per altre funzioni aziendali critiche.
- Gestione della Documentazione e della Tenuta dei Registri: Una corretta documentazione e tenuta dei registri sono essenziali per dimostrare la conformità e condurre audit efficaci. Tuttavia, gestire grandi quantità di documentazione, garantirne l'accuratezza e mantenerne l'accessibilità può essere impegnativo, specialmente in un ambiente altamente regolamentato.
- Integrazione di nuove tecnologie: L'integrazione di tecnologie innovative nei processi di conformità e convalida esistenti può essere complessa. Sebbene tecnologie come l'automazione e l'IA (Intelligenza Artificiale) offrano vantaggi significativi, la loro integrazione deve essere gestita con attenzione per garantire che siano conformi ai requisiti normativi e non introducano nuovi rischi.
- Formazione e competenza: È fondamentale assicurare che il personale sia adeguatamente formato e competente nei processi di conformità, audit e convalida. Sono necessari programmi di formazione continua per mantenere il personale aggiornato sui cambiamenti normativi e sulle migliori pratiche, il che può richiedere molte risorse.
- Affrontare i risultati degli audit: Affrontare e correggere efficacemente i problemi individuati durante gli audit può essere difficile. Le aziende devono implementare tempestivamente azioni correttive e preventive, assicurandosi che tali azioni non interrompano le operazioni in corso o influiscano sulla qualità del prodotto.
- Bilanciare la conformità con l'innovazione: Trovare un equilibrio tra il rispetto di normative rigorose e la ricerca dell'innovazione può essere difficile. Le aziende devono orientarsi nel panorama normativo continuando a sviluppare e introdurre nuovi prodotti e tecnologie.
- Garantire Coerenza tra le Operazioni: Mantenere la coerenza nelle pratiche di conformità e nei processi di convalida tra i diversi reparti, strutture e fasi del ciclo di vita del prodotto è essenziale ma impegnativo. La variabilità nelle pratiche può portare a non conformità e problemi di qualità.
Cosa sono gli Audit GxP?
Cos'è un audit di conformità indipendente GxP e chi lo esegue?
Un audit GxP è un processo ideato per garantire che le aziende rispettino gli standard prestabiliti in materia di qualità, sicurezza e conformità normativa. Può riguardare diversi aspetti dei prodotti e dei processi farmaceutici, quali le Buone Pratiche di Laboratorio (GLP), le Buone Pratiche Cliniche (GCP), le Buone Pratiche di Fabbricazione (GMP) e le Buone Pratiche di Farmacovigilanza (GVP).
L'audit valuta il livello di conformità alle leggi, ai regolamenti, alle linee guida e alle procedure operative standard (SOP) applicabili e individua le lacune, i rischi e le opportunità di miglioramento. L'audit fornisce inoltre raccomandazioni e azioni correttive per dare seguito ai risultati emersi e migliorare i sistemi di qualità.
I vantaggi di un audit GxP includono:
- Fornire una valutazione imparziale e oggettiva dei sistemi di qualità e del livello di conformità.
- Rafforzare la fiducia dei regolatori, dei clienti, dei fornitori e degli altri stakeholder.
- Riduzione della probabilità e della gravità di ispezioni normative, osservazioni e sanzioni.
- Migliorare la qualità, la sicurezza e l'efficacia dei prodotti e dei processi.
- Aumentare l'efficienza e l'efficacia delle operazioni e ridurre i costi e gli errori.
- Supporto per il miglioramento continuo e l'innovazione dei prodotti e dei processi.
Un audit GxP è condotto da un auditor qualificato ed esperto o da un team di auditor con conoscenze, competenze e credenziali pertinenti nell'industria farmaceutica e nell'area GxP specifica. L'auditor o il team di audit dovrebbe essere indipendente dall'azienda sottoposta ad audit e seguire gli standard professionali e i principi etici dell'auditing. Dovrebbero inoltre utilizzare strumenti e metodi appropriati per condurre l'audit, come checklist, interviste, osservazioni, revisioni di documenti, campionamenti, test, ecc. Freyr offre supporto End-to-End negli audit GxP. In qualità di leader del settore, i nostri esperti renderanno il vostro percorso di conformità senza intoppi.
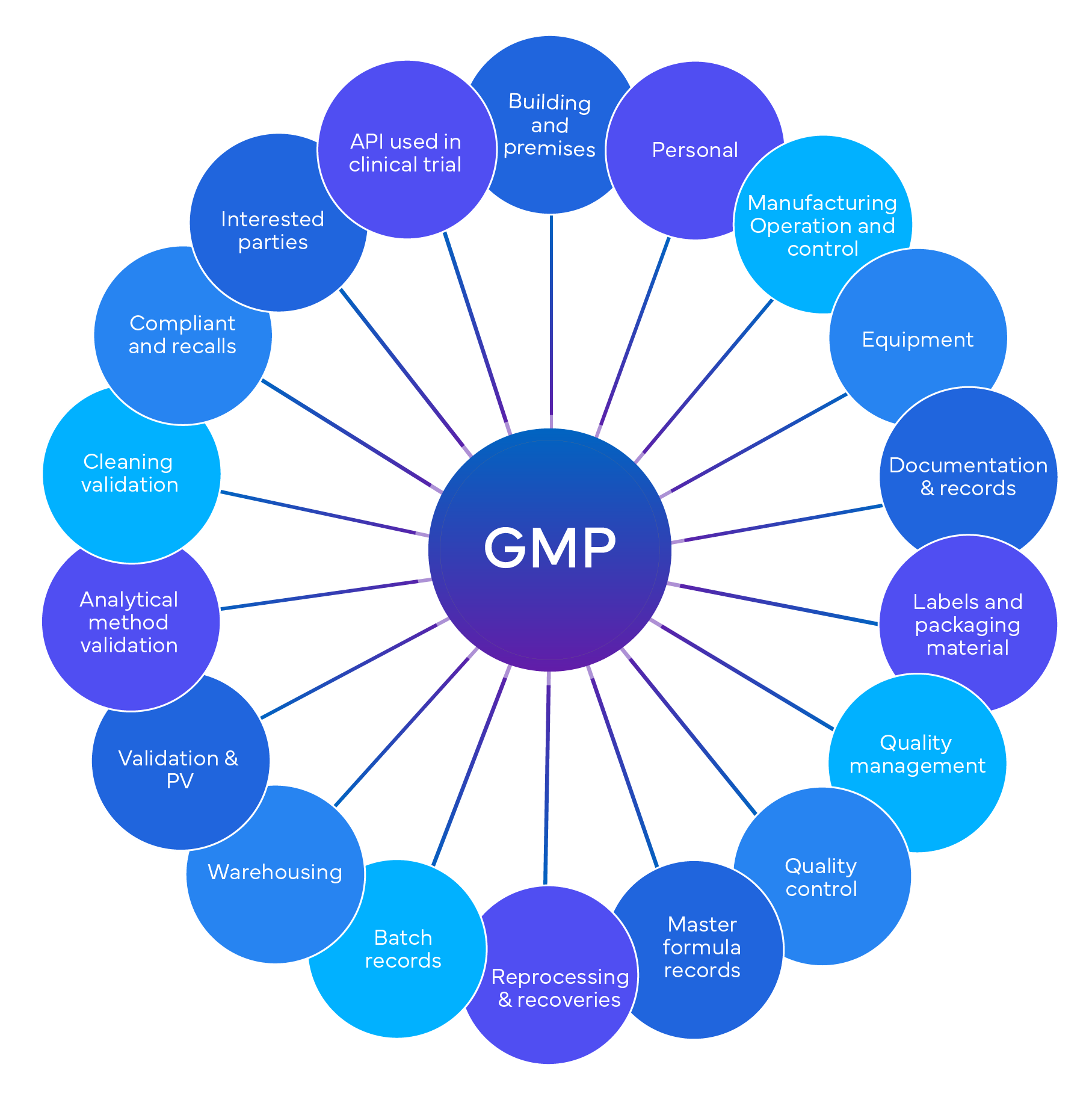
Quadro Normativo per gli Audit GxP
La conformità GxP è un insieme di regolamenti che disciplinano diverse industrie regolamentate, tra cui prodotti farmaceutici, dispositivi medici, alimenti, bevande e biotecnologie. L'obiettivo principale della conformità GxP è mantenere la qualità del prodotto e garantire la sicurezza pubblica. Ecco alcuni punti chiave:
- Panoramica sulla conformità GxP:
- GxP comprende diversi standard, tra cui le Buone Pratiche di Laboratorio (GLP), le Buone Pratiche Cliniche (GCP), le Buone Pratiche di Fabbricazione (GMP) e le Buone Pratiche di Farmacovigilanza (GVP).
- Questi standard assicurano che i prodotti siano accuratamente testati, fabbricati e gestiti durante tutto il loro ciclo di vita.
- Conferenza Internazionale sull'Armonizzazione (ICH):
- L'ICH fornisce linee guida per la conformità GxP.
- Le Linee Guida ICH Q7A sulle Buone Pratiche di Fabbricazione affrontano specificamente le pratiche di fabbricazione per i principi attivi farmaceutici (APIs).
- Ispezioni della FDA:
- La Food and Drug Administration degli US (FDA) conduce ispezioni per valutare la conformità con i regolamenti GxP.
- Queste ispezioni valutano l'aderenza a specifiche normative e linee guida FDA.
- Ispezioni di Health Canada:
- Health Canada, l'autorità di regolamentazione in Canada, effettua anche ispezioni per garantire la conformità GxP.
- Queste ispezioni si concentrano su vari aspetti, inclusi produzione, controllo qualità e distribuzione.
- Criteri di valutazione per gli audit GxP:
La conformità negli audit indipendenti GxP viene solitamente valutata in base a una serie di criteri, che possono includere:
- Requisiti Normativi: Conformità a normative, linee guida e leggi specifiche applicabili all'area GxP (ad es. regolamenti FDA, linee guida ICH o standard ISO).
- Sistemi di qualità: Valutazione dei sistemi di gestione della qualità, delle pratiche di documentazione e della tenuta dei registri.
- Validazione dei processi: Verifica che i processi siano validati e soddisfino criteri predefiniti.
- Formazione e competenza: Valutazione della formazione e delle qualifiche del personale.
- Gestione del Rischio: Identificazione e mitigazione dei rischi relativi alla qualità e alla sicurezza del prodotto.
Scopri come un esperto normativo comprovato può aiutarti a creare il quadro di audit GxP ideale adatto alle tue esigenze e a rimanere conforme alle normative globali.
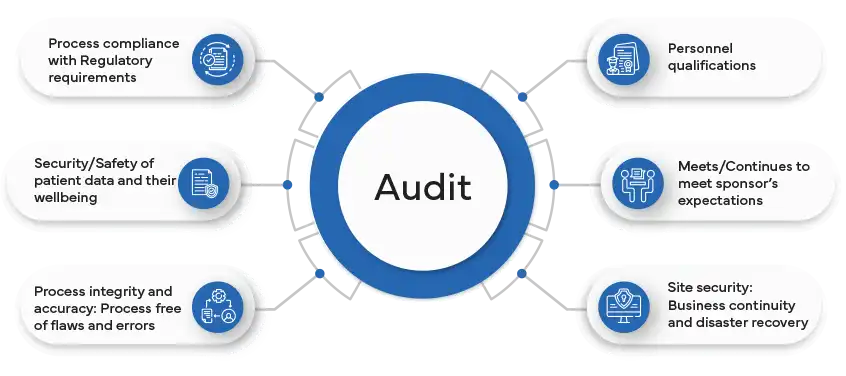
Vantaggi della conduzione di audit di conformità GxP
Gli audit GxP offrono numerosi vantaggi a qualsiasi organizzazione. In primo luogo, forniscono una valutazione imparziale e indipendente del rischio e della conformità all'interno dell'organizzazione, consentendo alle aziende di identificare aree di non conformità o rischi potenziali che potrebbero essere trascurati dagli audit interni. Questi audit sono essenziali per garantire che le aziende aderiscano a determinati standard di qualità, sicurezza e conformità normativa.
| Aspetto | Descrizione |
|---|---|
| Revisione completa | Valutazione approfondita da parte di una terza parte qualificata per identificare le aree di non conformità. |
| Normative Regolatorie | Aderenza agli standard GxP (buone pratiche) come GMP, GCP e GLP. |
| Ambito personalizzato | Ambito di audit personalizzato basato su prodotti e processi specifici. |
| Auditor qualificati | Auditor esperti e a conoscenza delle normative. |
| Quadro Normativo | Segue le linee guida ICH Q7A, FDA e Health Canada. |
| Vantaggi | Valutazioni imparziali, prevenzione dei rischi, mantenimento della qualità e scalabilità. |
Ecco alcuni punti chiave sugli audit di conformità GxP:
- Revisione Approfondita: Gli audit GxP prevedono un processo di revisione approfondito condotto da un'organizzazione o un consulente terzo qualificato. Lo scopo è identificare eventuali aree di non conformità all'interno dell'organizzazione e fornire raccomandazioni per il miglioramento.
- Standard Normativi: Le normative esaminate durante questi audit sono definite dagli standard GxP (buone pratiche), come le Buone Pratiche di Fabbricazione (GMP), le Buone Pratiche Cliniche (GCP) e le Buone Pratiche di Laboratorio (GLP). Questi standard garantiscono che prodotti, servizi e processi soddisfino costantemente i requisiti normativi pertinenti.
- Ambito personalizzato: L'ambito di un audit indipendente è personalizzato in base ai prodotti e ai processi specifici dell'organizzazione. Può includere la gestione del personale, la gestione delle strutture, la tenuta dei registri, la garanzia e il controllo della qualità, la progettazione di prodotti e processi e le operazioni tecniche.
- Auditor Qualificati: L'audit deve essere condotto da un auditor qualificato ed esperto che abbia familiarità con le normative applicabili e possieda l'esperienza necessaria per valutare efficacemente le procedure e i processi dell'organizzazione.
- Quadro Normativo: Gli audit GxP seguono quadri normativi come la Guida alle Buone Pratiche di Fabbricazione Q7A dell'International Conference on Harmonization (ICH), le ispezioni della FDA e le ispezioni di Health Canada. Questi quadri forniscono indicazioni sui requisiti di base per la produzione, l'assicurazione della qualità, la distribuzione e altre attività critiche relative alla fabbricazione sicura dei prodotti.
- Vantaggi: Gli audit GxP offrono valutazioni imparziali, aiutano a prevenire problemi di non conformità, mantengono gli standard di qualità e garantiscono la responsabilità. L'outsourcing di questi audit fornisce accesso a competenze, obiettività, efficienza dei costi e scalabilità, consentendo alle aziende di concentrarsi sulle competenze chiave.
Se cerchi soluzioni per la conformità GxP, considera Freyr. Siamo specializzati nella conformità normativa, nella garanzia di qualità e nella sicurezza in tutto il settore delle scienze della vita. Con la nostra esperienza, puoi garantire l'aderenza agli standard GxP, ottimizzare i processi e mantenere prodotti e servizi di alta qualità.
Consigli per Preparare la Vostra Organizzazione per un Audit
Preparare la propria organizzazione per un audit è un processo strategico che richiede una pianificazione meticolosa e un approccio proattivo. Innanzitutto, assicurarsi che tutti i registri, la documentazione e i file pertinenti siano organizzati e facilmente accessibili. Un sistema di archiviazione ben organizzato facilita un processo di audit più fluido e riflette positivamente sulla professionalità della vostra organizzazione.
In secondo luogo, si raccomanda di condurre un pre-audit interno per identificare potenziali aree di preoccupazione. Questa autovalutazione permette di affrontare eventuali problemi o discrepanze prima dell'audit esterno. Risolvendo proattivamente le questioni, si dimostra il proprio impegno verso la conformità e la trasparenza.
In terzo luogo, comunicare e collaborare efficacemente con il team di audit. Fornire le informazioni necessarie, l'accesso al personale pertinente e un ambiente di lavoro favorevole. Una comunicazione chiara aiuta a costruire un rapporto positivo con gli auditor, favorendo un'atmosfera collaborativa durante il processo di audit.
Infine, assicuratevi che il vostro team sia ben formato e consapevole del processo di audit. Educate i dipendenti sui loro ruoli, responsabilità e sull'importanza della conformità. Instillando una cultura di preparazione e cooperazione, la vostra organizzazione potrà affrontare gli audit con fiducia e professionalità.
Comprendere gli Audit da remoto
Cos'è un audit da remoto nell'industria farmaceutica e in cosa si differenzia dagli audit tradizionali in loco?
Un audit a distanza nel settore farmaceutico è una valutazione completa dei processi, delle strutture e dei sistemi di un'azienda, condotta dalle autorità di regolamentazione o da revisori senza una presenza fisica in loco. Tale audit viene effettuato tramite strumenti di comunicazione digitale, software collaborativi e l'accesso remoto ai documenti e ai sistemi pertinenti. Ha lo scopo di garantire la conformità agli standard normativi, valutare i sistemi di gestione della qualità e verificare il rispetto delle Buone Pratiche di Fabbricazione (GMP), delle Buone Pratiche Cliniche (GCP) o di altre normative applicabili.
La differenza tra gli audit da remoto e quelli tradizionali in loco è l'assenza di presenza fisica durante un audit da remoto. Invece di visitare le sedi dell'azienda, gli auditor si affidano a interazioni virtuali, documentazione elettronica e accesso remoto ai sistemi. Questo approccio offre flessibilità ed efficienza, consentendo lo svolgimento degli audit indipendentemente dalle distanze geografiche e dalle restrizioni di viaggio. Tuttavia, è necessario affrontare sfide come la limitata osservazione diretta delle strutture e le potenziali preoccupazioni sulla sicurezza informatica per garantire l'efficacia degli audit da remoto.
Nonostante le differenze, gli obiettivi degli audit sia remoti che tradizionali rimangono gli stessi – verificare la conformità, identificare aree di miglioramento e garantire la qualità e la sicurezza dei prodotti farmaceutici. La scelta tra audit remoti e in loco dipende da fattori quali la natura dell'audit, i requisiti normativi e le capacità dell'azienda di facilitare una valutazione approfondita tramite mezzi remoti.
Freyr sfrutta un decennio di esperienza per fornire soluzioni normative ineguagliabili, garantendo conformità e successo nel dinamico panorama farmaceutico.
Esplora l'eccellenza normativa con noi – il tuo partner strategico per il successo della conformità nell'industria farmaceutica in continua evoluzione. Contattaci per gestire le complessità normative senza problemi.
Quali sfide possono sorgere durante gli audit da remoto e come vengono affrontate per garantire valutazioni approfondite?
Durante gli audit da remoto possono sorgere diverse sfide, ma le organizzazioni possono adottare misure per affrontarle e garantire valutazioni approfondite. Ecco alcune sfide chiave e le loro potenziali soluzioni:
- Costruire relazioni chiave con gli stakeholder dell'audit:
- Sfida: Il lavoro remoto può ostacolare lo sviluppo di relazioni solide con le parti interessate all'audit.
- Soluzione: Riunioni virtuali regolari, comunicazione aperta e coinvolgimento attivo possono aiutare a costruire e mantenere le relazioni. Utilizzare le videochiamate per stabilire una connessione personale.
- Investire nella tecnologia per il lavoro virtuale:
- Sfida: Gli audit remoti dipendono fortemente dalla tecnologia e strumenti inadeguati possono ostacolare l'efficienza.
- Soluzione: Investire in software robusti per la gestione degli audit, piattaforme di comunicazione sicure e strumenti di collaborazione. Assicurarsi che gli auditor dispongano dell'hardware e del software necessari.
- Sviluppo dei dipendenti e promozione di una cultura positiva da remoto:
- Sfida: Il lavoro remoto può portare all'isolamento e ostacolare la crescita professionale.
- Soluzione: Fornire formazione virtuale, mentorship e opportunità di sviluppo delle competenze. Promuovere una cultura positiva attraverso attività di team building, riconoscimento e controlli regolari.
- Coltivare una mentalità intenzionale e adattiva:
- Sfida: Gli auditor remoti devono adattarsi alle circostanze mutevoli e mantenere la concentrazione.
- Soluzione: Incoraggiare la flessibilità, l'adattabilità e una mentalità orientata alla crescita. Formare gli auditor a gestire situazioni impreviste e ad adattare il loro approccio secondo necessità.
Freyr è un partner affidabile per le soluzioni di conformità normativa e sicurezza per il settore delle scienze della vita. Con una profonda esperienza nel settore, tecnologia innovativa e una presenza globale, Freyr consente alle organizzazioni di navigare senza problemi in complessi scenari normativi. Esplorate i nostri servizi e contattateci oggi stesso per migliorare il vostro percorso di conformità.
In che modo Freyr è meglio posizionata per aiutarvi con i vostri audit da remoto?
Freyr, con la sua esperienza decennale, eccelle nel facilitare audit remoti senza interruzioni per l'industria farmaceutica. Sfruttando tecnologie avanzate e una profonda comprensione dei requisiti normativi, Freyr garantisce un processo di audit approfondito ed efficiente, affrontando sfide come la presenza fisica limitata e le preoccupazioni sulla sicurezza informatica.
Il nostro team dedicato di esperti normativi è in grado di utilizzare soluzioni digitali innovative, garantendo una valutazione virtuale completa dei vostri processi, strutture e documentazione. La nostra comprovata esperienza negli audit da remoto riflette il nostro impegno a fornire soluzioni normative affidabili ed efficaci, adattate alle esigenze in evoluzione del panorama farmaceutico. Con Freyr, acquisite un partner fidato che comprende le complessità degli audit da remoto e adotta un approccio proattivo e collaborativo per migliorare il vostro percorso di conformità.
Cos'è la convalida dei sistemi informatici (CSV) e perché è fondamentale nell'industria farmaceutica?
Convalida dei Sistemi Informatici (CSV) è un processo critico nell'industria farmaceutica che garantisce l'integrità, l'affidabilità e la conformità dei sistemi computerizzati utilizzati per vari scopi. Approfondiamo i dettagli:
- Definizione e scopo:
- CSV è il processo documentato che assicura che un sistema informatico produrrà informazioni o dati che soddisfano requisiti predefiniti.
- Il suo scopo principale è convalidare e verificare che i sistemi informatici funzionino costantemente come previsto, mantenendo l'accuratezza, l'affidabilità e la sicurezza dei dati.
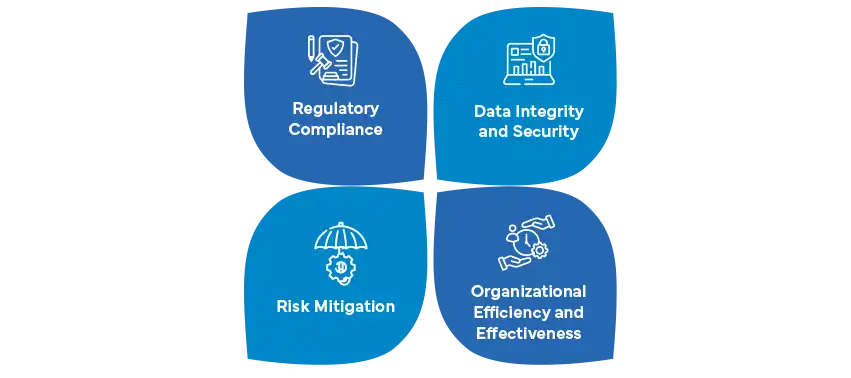
- Importanza nel settore farmaceutico.:
- Conformità Normativa: L'industria farmaceutica opera sotto severe normative (come le Buone Pratiche di Fabbricazione o GMP) per garantire la qualità, la sicurezza e l'efficacia dei prodotti.
- Integrità dei dati: Dati accurati e affidabili sono cruciali per lo sviluppo di farmaci, gli studi clinici, la produzione e la distribuzione.
- Mitigazione del Rischio: La CSV aiuta a identificare e mitigare i rischi associati ai sistemi informatici, prevenendo errori, perdita di dati e non conformità.
- Sicurezza del Paziente: Sistemi adeguatamente validati contribuiscono alla sicurezza dei pazienti garantendo qualità costante e aderenza agli standard.
- Aspetti chiave della CSV:
- Definizione dei requisiti: Definire chiaramente i requisiti di sistema, le funzionalità e le aspettative degli utenti.
- Progettazione e configurazione: Sviluppare e configurare il sistema secondo le specifiche.
- Test e qualificazione: Test rigorosi (inclusi test unitari, test di integrazione e test di accettazione utente) per verificare le prestazioni del sistema.
- Documentazione: Mantenere una documentazione completa per tutto il ciclo di vita del sistema.
- Controllo delle Modifiche: Gestire le modifiche al sistema, assicurando che non ne compromettano l'integrità.
- Sfide affrontate dalla CSV:
- Integrità dei dati: Prevenire accessi non autorizzati, corruzione o manipolazione dei dati.
- Sicurezza del sistema: Proteggere da minacce informatiche e modifiche non autorizzate.
- Registro delle modifiche (Audit Trail): Mantenere un registro elettronico indelebile dei dati per gli audit normativi.
- Manutenzione della Validazione: Rivedere e aggiornare regolarmente la validazione per adattarsi ai cambiamenti del sistema.
In cosa differisce la CSV da Computer System Assurance (CSA)?
La Validazione dei Sistemi Informatici (CSV) e la Garanzia dei Sistemi Informatici (CSA) rappresentano approcci distinti per assicurare l'integrità e la conformità dei sistemi computerizzati nell'industria farmaceutica. La CSV, una pratica consolidata, si concentra principalmente sulla fase di validazione del ciclo di vita di un sistema, assicurando che i sistemi software soddisfino i requisiti normativi attraverso protocolli predefiniti. D'altra parte, la CSA adotta un approccio più ampio e dinamico, coprendo l'intero ciclo di vita di un sistema computerizzato, dallo sviluppo e implementazione all'uso operativo e al suo eventuale ritiro.
CSV risponde all'esigenza di rigorosi processi di convalida, sottolineando approcci basati sul rischio per identificare e mitigare potenziali problemi. Tuttavia, il panorama farmaceutico è in evoluzione, favorendo l'emergere di CSA come strategia più completa. CSA estende il suo focus oltre la convalida adattando metodologie agili e incorporando il monitoraggio continuo durante l'intero ciclo di vita di un sistema. Questa prospettiva olistica consente alle organizzazioni di gestire proattivamente i rischi, specialmente nella cybersecurity e nell'integrità dei dati, allineandosi con la crescente enfasi del settore sulla tecnologia e sulla sicurezza dei dati.
La flessibilità del CSA rappresenta un vantaggio in un contesto normativo in rapida evoluzione. Mentre il CSV segue le pratiche di convalida tradizionali, il CSA si allinea alle aspettative in continua evoluzione delle autorità di regolamentazione. Va oltre le semplici attività di riconvalida periodica, integrando il monitoraggio continuo, l’analisi dei dati in tempo reale e strategie proattive di gestione del rischio per garantire una conformità costante e prestazioni ottimali. Mentre l'industria farmaceutica abbraccia la trasformazione digitale, comprendere le sfumature tra CSV e CSA diventa imperativo per le aziende che mirano a rimanere all'avanguardia nella conformità normativa e nell'integrità dei sistemi.
In questo contesto, Freyr, con la sua vasta esperienza e competenza, è ben attrezzata per guidare le aziende farmaceutiche attraverso le complessità di CSV e CSA, offrendo soluzioni personalizzate per soddisfare le esigenze in evoluzione della conformità normativa e dei progressi tecnologici.
Quali sono i componenti di un programma CSA?
Computer Software Assurance (CSA) è un approccio moderno che migliora l'affidabilità, la sicurezza e la conformità nei sistemi computerizzati. Esploriamo i suoi componenti e i benefici a lungo termine:
- Approccio basato sul rischio:
- Componente: CSA si concentra sulla valutazione e gestione del rischio.
- Importanza: Identificare le aree critiche aiuta ad allocare efficacemente gli sforzi di validazione.
- Test senza script:
- Componente: CSA include test non scriptati oltre i tradizionali casi di test scriptati.
- Importanza: Il testing non scriptato simula scenari reali, scoprendo problemi nascosti.
- Monitoraggio continuo delle prestazioni:
- Componente: CSA prevede un monitoraggio continuo delle prestazioni del sistema.
- Importanza: Rilevare precocemente le anomalie previene guasti del sistema e problemi di integrità dei dati.
- Supervisione dei dati:
- Componente: CSA pone l'accento sulla qualità e l'integrità dei dati.
- Importanza: Garantisce dati accurati per il processo decisionale e la conformità.
- Attività di convalida esterna:
- Componente: CSA collabora con i fornitori di software per la validazione esterna.
- Importanza: La validazione indipendente aggiunge fiducia e riduce i pregiudizi.
- Passaggio da CSV a CSA:
- Fasi iniziali:
- Comprendere i principi della CSA.
- Valutare i rischi dei sistemi esistenti.
- Dare priorità alle funzionalità critiche.
- Vantaggi:
- Carico di lavoro di convalida ridotto.
- Risposta agile ai cambiamenti.
- Maggiore affidabilità del sistema.
- Fasi iniziali:
- Affidabilità del sistema a lungo termine:
- CSA garantisce:
- Adattabilità: I sistemi si evolvono senza compromettere l'affidabilità.
- Sicurezza: Protezione contro le minacce informatiche.
- Conformità: Allineamento continuo con le normative.
- Qualità: Qualità costante dei dati e dei prodotti.
- CSA garantisce:
Come contribuisce la CSA all'integrità dei dati nell'industria farmaceutica?
CSA garantisce l'integrità dei dati nell'industria farmaceutica assicurando accuratezza, coerenza e affidabilità dei dati durante l'intero ciclo di vita di un sistema. A differenza degli approcci tradizionali, CSA adotta una strategia olistica che va oltre la convalida, affrontando attivamente potenziali sfide e discrepanze che possono sorgere nel tempo.
Un contributo della CSA all'integrità dei dati risiede nelle sue capacità di monitoraggio continuo. Invece di affidarsi esclusivamente a sforzi di convalida periodici, la CSA implica analisi dei dati in tempo reale e misure proattive di gestione del rischio. Questo approccio consente alle organizzazioni di rilevare e affrontare potenziali discrepanze nei dati, evitando che le imprecisioni si accumulino nel tempo. L'enfasi della CSA su un modello di ciclo di vita dinamico e adattivo garantisce che l'integrità dei dati rimanga un obiettivo costante, allineandosi alle aspettative normative.
Per prevenire discrepanze nei dati nel tempo, CSA incorpora diverse misure strategiche. In primo luogo, impiega robusti processi di controllo delle modifiche, documentando meticolosamente qualsiasi modifica ai sistemi o ai processi computerizzati che potrebbe influire sull'integrità dei dati. Audit e valutazioni regolari dei sistemi vengono condotti per identificare e correggere potenziali problemi prima che si aggravino. Inoltre, CSA sottolinea l'importanza dei programmi di formazione e sensibilizzazione degli utenti per garantire che il personale comprenda l'importanza di mantenere l'integrità dei dati e aderisca alle migliori pratiche.
In conclusione, l'approccio proattivo e completo di CSA all'integrità dei dati la distingue come soluzione strategica nell'industria farmaceutica. Incorporando il monitoraggio continuo, la gestione del rischio e rigorose misure di controllo delle modifiche, CSA mantiene l'integrità dei dati e assicura che le aziende farmaceutiche siano ben preparate a gestire il panorama in evoluzione delle aspettative normative. Mentre le organizzazioni si sforzano di mantenere i più alti standard nell'integrità dei dati, CSA emerge come un alleato chiave nel loro percorso, allineandosi con le tendenze del settore e i progressi normativi.
Per le organizzazioni che cercano una guida sull'implementazione di strategie CSA efficaci, Freyr è un partner affidabile che offre soluzioni personalizzate per affrontare le sfide uniche del panorama farmaceutico.
Che ruolo svolge la conformità normativa nella CSA?
La conformità normativa è una pietra angolare della CSA, garantendo che le aziende farmaceutiche aderiscano a standard e linee guida in evoluzione durante l'intero ciclo di vita di un sistema. A differenza dell'approccio tradizionale della convalida dei sistemi informatici (CSV), la CSA enfatizza la conformità continua e l'adattabilità ai mutevoli scenari normativi. Man mano che le aziende passano dalla CSV alla CSA, rimanere aggiornati sulle normative in evoluzione diventa fondamentale.
Nel contesto della CSA, la conformità normativa implica l'allineamento dei sistemi computerizzati con i requisiti normativi globali e locali, dallo sviluppo all'uso operativo e al ritiro finale. La CSA enfatizza la conformità continua piuttosto che la convalida periodica, promuovendo un approccio proattivo per affrontare tempestivamente i potenziali cambiamenti normativi. Questo allineamento strategico assicura che le aziende farmaceutiche siano ben preparate a soddisfare le aspettative normative, salvaguardando l'integrità dei dati, la sicurezza dei pazienti e l'affidabilità complessiva del sistema.

Il coinvolgimento regolare con le autorità di regolamentazione, la partecipazione a forum di settore e l'abbonamento a pubblicazioni normative forniscono preziose informazioni sugli standard in evoluzione. Sfruttare l'esperienza dei consulenti normativi e investire nella formazione continua del personale coinvolto nei processi CSA migliora ulteriormente la consapevolezza normativa. Collaborare con partner normativi, come Freyr Solutions, offre un approccio proattivo, garantendo l'accesso a informazioni normative aggiornate e soluzioni personalizzate per gestire senza problemi la transizione.
La conformità normativa in CSA è un impegno dinamico e continuo che si allinea con il passaggio del settore verso l'adattabilità e il miglioramento continuo. Rimanere informati, essere proattivi e collaborare con esperti normativi sono aspetti cruciali per le aziende che passano dalla CSV alla CSA, facilitando un'evoluzione fluida e conforme nel panorama farmaceutico in continua evoluzione.
In qualità di partner normativo fidato, Freyr fornisce il supporto e la competenza necessari per guidare le aziende attraverso questa transizione, garantendo l'eccellenza normativa e la conformità nell'era della CSA.
In che modo un partner strategico per la conformità normativa può essere d'aiuto?
Un partner strategico per la conformità normativa svolge un ruolo critico nell'assicurare che le aziende farmaceutiche soddisfino i requisiti normativi e mantengano elevati standard di qualità. Ecco come possono aiutare:
- Guida Esperta: Un partner strategico fornisce consulenza esperta su come orientarsi tra normative complesse e in evoluzione in diverse regioni. Offre approfondimenti sulle ultime modifiche normative, aiutando le aziende ad adeguare le loro pratiche e a mantenere la conformità.
- Processi ottimizzati: Aiutano a ottimizzare i processi di conformità implementando le migliori pratiche e flussi di lavoro efficienti. Ciò include lo sviluppo di sistemi robusti per la documentazione, l'audit e la convalida, riducendo gli oneri amministrativi e migliorando l'efficienza complessiva.
- Mitigazione del Rischio: Identificando potenziali rischi di conformità e vulnerabilità, un partner strategico aiuta a mitigare i rischi prima che diventino problemi. Essi conducono audit e valutazioni approfondite per garantire che tutti i processi siano conformi e per affrontare proattivamente eventuali lacune.
- Formazione e supporto: Offrono formazione e supporto per garantire che il personale sia ben informato sui requisiti normativi e sulle migliori pratiche. Ciò contribuisce a costruire la competenza interna e assicura che tutti coloro che sono coinvolti nelle attività di conformità siano aggiornati sugli standard attuali.
- Integrazione tecnologica: Un partner strategico assiste nell'integrazione di tecnologie innovative, come l'automazione e l'intelligenza artificiale, nei processi di conformità. Garantisce che queste tecnologie siano implementate in modo efficace e in conformità con i requisiti normativi, migliorando l'integrità dei dati e l'efficienza dei processi.
- Documentazione e tenuta dei registri: Gestiscono la creazione, l'organizzazione e la manutenzione della documentazione cruciale per la conformità. Ciò garantisce che tutti i registri siano accurati, completi e facilmente accessibili per audit e ispezioni.
- Presentazioni e approvazioni normative: Gestiscono la preparazione e la presentazione di documenti e domande normative. Ciò include la garanzia che le presentazioni soddisfino tutti i requisiti necessari e la gestione delle comunicazioni con le autorità di regolamentazione per facilitare approvazioni tempestive.
- Azioni Correttive e Preventive: Un partner strategico supporta lo sviluppo e l'implementazione di azioni correttive e preventive in risposta ai risultati degli audit o a problemi di conformità. Aiutano a garantire che queste azioni siano efficaci e non interrompano le operazioni in corso.
- Strategia di Conformità Globale: Sviluppano e implementano strategie per raggiungere la conformità globale, affrontando i diversi requisiti normativi dei vari mercati. Ciò garantisce che i prodotti soddisfino tutti gli standard necessari per la distribuzione e l'uso internazionale.
- Monitoraggio Continuo: Forniscono monitoraggio e supporto continui per mantenere le aziende informate su eventuali aggiornamenti o modifiche normative. Questo approccio proattivo aiuta le aziende a rimanere conformi e ad adattarsi alle nuove normative man mano che emergono.
Perché scegliere Freyr?
Oltre dieci anni di eccellenza nella conformità normativa.
Gamma completa di conformità, audit e convalida.
Competenza in diversi settori e aree geografiche
Utilizza strumenti innovativi per risultati accurati.
Professionisti esperti con una profonda conoscenza del settore.
Gestione riuscita di sfide complesse in materia di conformità.
Domande Frequenti
La conformità farmaceutica implica l'adesione a leggi, regolamenti e linee guida che regolano l'industria farmaceutica. Garantisce che le aziende allineino le loro operazioni agli standard del settore, salvaguardando così la sicurezza e l'efficacia dei prodotti e mantenendo l'integrità dei dati.
Lo scopo di un audit è valutare sistematicamente l'aderenza di un'azienda agli standard normativi e alle politiche interne. Gli audit aiutano a identificare aree di miglioramento, mitigare i rischi e garantire che i processi siano efficaci nella produzione di prodotti farmaceutici sicuri e conformi.
La convalida nel settore farmaceutico è il processo che conferma che sistemi, processi e attrezzature soddisfano costantemente i requisiti predefiniti. È essenziale per garantire la conformità agli standard normativi e per mantenere la qualità e la sicurezza dei prodotti farmaceutici durante tutto il loro ciclo di vita.
Questi processi sono fondamentali per garantire la sicurezza e l'efficacia dei prodotti, mantenere l'aderenza normativa, migliorare la garanzia di qualità, supportare l'accesso al mercato e facilitare il miglioramento continuo. Aiutano le aziende a soddisfare standard rigorosi e a costruire fiducia con gli stakeholder.
Le sfide includono la gestione delle normative in evoluzione, la garanzia dell'integrità dei dati, la gestione dei vincoli di risorse e il mantenimento di una documentazione adeguata. Inoltre, l'integrazione di tecnologie innovative e la garanzia della competenza del personale possono complicare gli sforzi di conformità.
Gli audit GxP sono valutazioni condotte per garantire l'adesione agli standard delle Buone Pratiche (GxP), che includono le Buone Pratiche di Fabbricazione (GMP), le Buone Pratiche Cliniche (GCP) e le Buone Pratiche di Laboratorio (GLP). Questi audit aiutano a identificare le lacune di conformità e a migliorare i sistemi di qualità.
Un audit di conformità indipendente GxP è una valutazione oggettiva dell'aderenza di un'azienda agli standard di qualità e normativi. Condotto da auditor qualificati, identifica rischi e aree di miglioramento, migliorando la conformità e la sicurezza del prodotto.
Gli audit GxP forniscono valutazioni imparziali, migliorano la conformità normativa e identificano aree di miglioramento operativo. Contribuiscono a mantenere elevati standard di qualità e a costruire fiducia con le autorità di regolamentazione e i clienti.
CSV garantisce che i sistemi computerizzati utilizzati nel settore farmaceutico producano costantemente dati affidabili e soddisfino i requisiti normativi. È vitale per mantenere l'integrità dei dati, mitigare i rischi e garantire la sicurezza del paziente durante l'intero ciclo di vita del prodotto.
CSV si concentra sulla convalida che un sistema soddisfi i requisiti normativi e funzioni come previsto, mentre CSA comprende un approccio più ampio che include la garanzia continua delle prestazioni e della conformità del sistema durante il suo ciclo di vita.














