
L'idea di presentazioni normative elettroniche per i prodotti farmaceutici precede lo strumento eCTD stesso. Alla fine degli anni '80, iniziative come CANDA (Computer-Aided New Drug Application) furono esplorate dalla US FDA (Food and Drug Administration) e dalle agenzie europee. Questi primi sforzi miravano a migliorare l'efficienza e l'accesso ai dati per i revisori.
Introduzione dello standard eCTD (2003):
La Conferenza Internazionale sull'Armonizzazione (ICH) è intervenuta nel 2003 con un elemento rivoluzionario: lo standard eCTD (electronic Common Technical Document). Questo formato standardizzato è stato progettato per stabilire un linguaggio universale per le presentazioni elettroniche a livello mondiale.
L'emergere degli strumenti eCTD:
Con l'adozione dello standard eCTD, la domanda di strumenti eCTD specializzati è aumentata. Questi strumenti hanno apportato diversi vantaggi chiave:
- Creazione di Contenuti Ottimizzata: Gli utenti possono creare e organizzare documenti senza sforzo in linea con la struttura eCTD.
- Validazione Robusta: gli strumenti eCTD hanno assicurato che le presentazioni rispettassero le specifiche tecniche, prevenendo ritardi causati da errori di formattazione.
- Gestione efficiente del ciclo di vita: Gestire le revisioni, tracciare le versioni e mantenere la conformità normativa diventa più facile.
Queste innovazioni hanno rivoluzionato il processo di presentazione normativa, rendendolo più efficiente e affidabile.
Come il software di Freyr Digitale automatizza la creazione di eCTD
La soluzione software avanzata di Freyr Digitale, Freyr SUBMIT PRO, affronta queste sfide automatizzando gli aspetti chiave della creazione di eCTD, migliorando così l'efficienza e riducendo l'errore umano.
Ottimizzazione delle risorse: Automatizzando le attività ripetitive, il nostro software libera risorse umane preziose. I professionisti possono concentrarsi su attività più strategiche e di alto valore, come l'analisi dei dati, lo sviluppo della strategia normativa e il coinvolgimento degli stakeholder. Questo cambiamento non solo migliora la produttività, ma riduce anche i costi operativi, fornendo un significativo ritorno sull'investimento.
Rischio di errore umano minimizzato: L'automazione minimizza il rischio di errore umano garantendo che i dati siano trasferiti con precisione e che i documenti siano formattati correttamente. I controlli di convalida integrati nel software e i meccanismi di rilevamento degli errori migliorano ulteriormente la qualità e la conformità delle presentazioni normative. Ciò riduce la necessità di rilavorazioni e contribuisce a garantire approvazioni tempestive.
Tracker delle presentazioni per una panoramica completa delle presentazioni eCTD
Un sistema automatizzato e intuitivo per la pianificazione e il monitoraggio delle complesse attività di sottomissione eCTD globali, la gestione del flusso di lavoro delle attività e l'archiviazione e la gestione delle domande normative e delle informazioni di sottomissione è essenziale per garantire che i richiedenti affrontino le sfide associate ben prima del tempo. Ottenere visibilità sulle operazioni di sottomissione e pubblicazione a un livello granulare rende l'intero processo di sottomissione più fluido e veloce.
Monitoraggio delle presentazioni
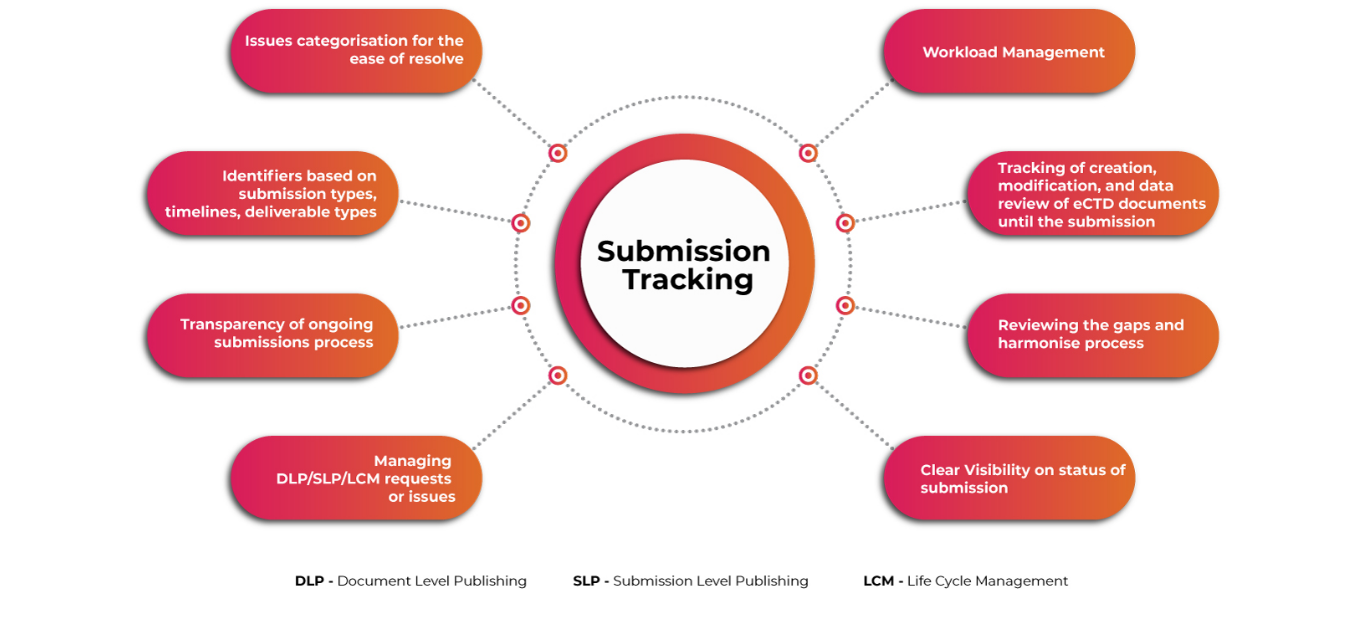
L'ultimo aggiornamento dell'eCTD
Il passaggio all'eCTD 4.0 annuncia una maggiore efficienza e una standardizzazione globale nel processo di approvazione dei farmaci farmaceutici. Preparandosi a questa transizione, la vostra azienda può gestire il cambiamento senza problemi e capitalizzare le numerose opportunità che questa nuova era offre. Sebbene il passaggio all'eCTD 4.0 possa porre delle sfide, queste sono superabili con la dedizione e la determinazione di tutti i paesi coinvolti. Anche se saranno necessari investimenti e sforzi significativi, i sostanziali benefici dell'eCTD 4.0 rendono l'impresa davvero degna di nota.
Revisione del processo di presentazione: eCTD 4.0 promette di rivoluzionare il modo in cui le aziende farmaceutiche presentano i dati sullo sviluppo dei farmaci alle autorità sanitarie. Mira a semplificare il processo di presentazione.
Tempistiche di Implementazione: La FDA prevede di accettare nuove domande nel formato eCTD 4.0 a partire dal 2024. Le fasi future riguarderanno le applicazioni v3.2.2 esistenti e la comunicazione bidirezionale.
Compatibilità futura: eCTD 4.0 include la compatibilità futura, consentendo il riutilizzo del ciclo di vita e dei documenti del contenuto v3.2.2. Ciò semplifica la conversione delle applicazioni v3.2.2 a eCTD 4.0.
Criteri di Convalida: Sono disponibili le specifiche per i criteri di convalida eCTD 4.0. Questi criteri garantiscono la qualità e l'accuratezza delle presentazioni.
Conformità Globale: Entro il 2026, gli organismi di regolamentazione di tutto il mondo potrebbero richiedere la conformità agli standard eCTD 4.0. Sebbene attualmente volontaria, l'applicazione diventerà obbligatoria tra il 2026 e il 2029.
Il futuro dell'eCTD:
È necessario accogliere l'IA e rendere dinamica la vostra funzione normativa, poiché aggiunge valore al vostro business. Freya Fusion è una piattaforma all'avanguardia per la gestione delle informazioni normative (RIM), basata su IA e nativa del cloud, che offre prestazioni, sicurezza e scalabilità eccezionali, mantenendo al contempo una rigorosa conformità GxP. Arricchita con funzionalità avanzate di IA/ML e automazione, Freya Fusion eccelle nel campo digitale, fornendo funzionalità superiori e un'esperienza utente eccezionale. I progressi dell'IA di Freyr Digitale promettono moduli di produzione e tracciamento delle sottomissioni, che includono funzionalità per la compilazione, la pubblicazione e la convalida senza interruzioni delle sottomissioni normative, garantendo una meticolosa conformità alle Linee Guida eCTD. Rimanere all'avanguardia nella conformità normativa con SaaS basato su IA è sicuramente un vantaggio per la vostra azienda. Che si tratti di un sistema di allerta precoce per i cambiamenti normativi, di una revisione e analisi semplificata dei documenti normativi o di analisi predittive per la gestione del rischio, Freyr Digitale vi offre una copertura completa. Contattate hello@freyrdigital.com per scoprire le nostre innovazioni basate su IA/ML che semplificano le operazioni normative nel settore medico.
Rimanete all'avanguardia con aggiornamenti regolari e progressi tecnologici. Collaborate con noi per ottimizzare le vostre operazioni normative, aumentare la produttività ed elevare la qualità delle presentazioni. Richiedete una demo oggi stesso e sperimentate la perfetta combinazione di competenze e strumenti. Portate la vostra organizzazione da buona a eccellente. Contattateci oggi stesso.









