
Per la maggior parte dei team che si occupano di affari regolatori, il rinnovo della registrazione non è solo un’altra formalità amministrativa. È il momento in cui anni di registrazioni relative alla qualità, dati post-commercializzazione e cronologie delle modifiche vengono sottoposti al vaglio delle autorità di regolamentazione.
Eppure, spesso i rinnovi vengono affrontati in modo reattivo.
I file vengono raccolti all'ultimo momento. I dati del PMS sono sparsi in cartelle diverse. I certificati vengono gestiti tramite fogli di calcolo. E all'improvviso, quello che avrebbe dovuto essere un processo strutturato si trasforma in una corsa contro il tempo.
I rinnovi delle autorizzazioni dei dispositivi medici non falliscono perché i team non si impegnano a sufficienza. Falliscono perché la pianificazione del rinnovo inizia troppo vicino alla scadenza.
Una solida strategia di rinnovo cambia questa situazione. Considera il rinnovo come un’attività che si svolge lungo tutto il ciclo di vita, non come un’operazione da sbrigare all’ultimo minuto.
Analizziamo cosa significa realmente per RA .
Perché il rinnovo delle autorizzazioni dei dispositivi medici richiede una strategia
La maggior parte delle registrazioni dei dispositivi ha una validità compresa tra 3 e 5 anni, a seconda del mercato. Alcune regioni prevedono rinnovi annuali, mentre altre adottano modelli di mantenimento con pagamenti periodici. Indipendentemente dalla struttura, una volta scaduta la licenza, il dispositivo non può più essere legalmente prodotto, importato o distribuito.
Le richieste di rinnovo sono ad alto rischio perché le autorità procedono a una nuova valutazione:
- Andamento post-quotazione
- Andamento dei reclami ed eventi avversi
- Modifiche al sistema di produzione e di qualità
- Dati clinici e relativi alla sicurezza
- Storia della conformità normativa
In molte regioni, tra cui l'India e l'Unione Europea, le autorità di regolamentazione richiedono dati PMS consolidati, prove relative alle azioni correttive e preventive (CAPA) e documentazione tecnica aggiornata nell'ambito della procedura di rinnovo.
Ecco perché il rinnovamento dovrebbe essere considerato una disciplina operativa che accompagna l'intero ciclo di vita del prodotto.
Non come un compito da svolgere entro una scadenza.
Inizia con un calendario normativo: la tua prima linea di difesa
Uno dei motivi più frequenti di insuccesso nei processi di rinnovo è dovuto alla frammentazione del monitoraggio. Mercati diversi. Tempistiche diverse. Requisiti diversi.
Un calendario normativo centralizzato dovrebbe includere:
- Numeri dei certificati e date di scadenza per paese
- Periodi di presentazione delle richieste di rinnovo
- Tempi di pagamento delle commissioni di mantenimento
- Validità della certificazione ISO 13485 del marchio CE
- Scadenze interne (12 mesi, 6 mesi, 3 mesi prima del rinnovo)
Da un RA pratico, la pianificazione dovrebbe iniziare almeno 12 mesi prima della scadenza.
Molte aziende utilizzano ormai piattaforme RIMS unificate per avere una visione d'insieme dello stato delle registrazioni in tutti i mercati, evitando così di dipendere dai fogli di calcolo e garantendo al contempo la visibilità e la gestibilità delle scadenze di rinnovo.
freya fusion la prima soluzione nel suo genere a consentire alle organizzazioni di disporre di un'unica fonte attendibile per tutti i dati relativi alla conformità.
Documentazione essenziale di cui avrai sempre bisogno
La documentazione relativa al rinnovo rispecchia fedelmente quella della registrazione iniziale, ma pone maggiore enfasi sulla continuità e sulle prestazioni.
La maggior parte delle autorità prevede che:
- Lettera di accompagnamento in cui si dichiara chiaramente l'intenzione di rinnovare
- Dichiarazione di conformità continuativa (produzione, progettazione, proprietà)
- File master dei dispositivi e file master degli stabilimenti aggiornati (se applicabile)
- ISO 13485 in corso di validità
- Certificati CE o certificati di garanzia della qualità, ove richiesti
- Licenze di produzione e documentazione relativa alle buone pratiche di fabbricazione (GMP)
- Dichiarazione di conformità
- Cronologia della corrispondenza normativa
Eventuali modifiche apportate durante il periodo di validità devono essere segnalate tramite gli appositi canali previsti dopo l'approvazione. Le modifiche non comunicate sono uno dei modi più rapidi per suscitare interrogativi da parte delle autorità di regolamentazione.
È proprio qui che la gestione strutturata dei documenti fa la differenza. RA traggono vantaggio dal fatto che tutte le proposte, le revisioni e le approvazioni siano conservate in un unico ambiente controllato, anziché essere sparse tra unità di disco e caselle di posta elettronica.
La sorveglianza post-commercializzazione è il fulcro del rinnovo
Se c'è un ambito che le autorità di regolamentazione devono esaminare attentamente in occasione del rinnovo, è proprio quello della sorveglianza post-commercializzazione.
Le autorità si aspettano prove che dimostrino che il dispositivo abbia continuato a funzionare in modo sicuro ed efficace nell'uso quotidiano.
In genere, ciò comprende:
- Dati di vendita per anno e per modello
- Registri dei reclami e segnalazioni di eventi avversi
- Analisi delle cause alla radice per ciascun problema
- Documentazione CAPA con prove della chiusura
- Cronologia dei richiami (globale e per paese)
- Analisi delle tendenze nell'intero periodo di validità
I dispositivi a rischio più elevato potrebbero inoltre richiedere:
- Rapporti PMS
- Aggiornamenti del rapporto di valutazione clinica
- PMCF
- Relazioni periodiche sull'aggiornamento della sicurezza
L'efficacia delle strategie di fidelizzazione dipende dalla costanza con cui questi dati vengono raccolti nel tempo, non dalla qualità del loro assemblaggio finale.
Molti RA integrano ormai il monitoraggio del PMS direttamente nei propri flussi di lavoro normativi utilizzando piattaforme unificate come freya fusion, consentendo di mantenere collegati reclami, CAPA e registrazioni per una più facile tracciabilità durante la preparazione del rinnovo.
Adegua il tuo sistema di qualità alla preparazione al rinnovo
Il vostro sistema di gestione della qualità non è slegato dal rinnovamento. Ne costituisce il fondamento.
Le autorità di regolamentazione ricercano prove in settori chiave quali:
- Controllo dei documenti e cronologia delle versioni
- Gestione del cambiamento nei settori della produzione, dell'etichettatura e del confezionamento
- Qualificazione dei fornitori e audit
- Gestione dei reclami e analisi delle tendenze
- Efficacia della CAPA
- Audit interni
- Documentazione relativa alla formazione e alle competenze
Un approccio pratico consiste nell’effettuare un’analisi delle lacune prima del rinnovo circa sei mesi prima della presentazione della domanda:
- Verificare che i certificati rimangano validi fino alla revisione
- Verificare la completezza dei dati PMS
- Verifica le chiusure CAPA
- Controlla i registri delle modifiche
- Assicurarsi che i registri di formazione siano aggiornati
Questa verifica preventiva spesso evita di dover ricorrere a misure correttive dell'ultimo minuto.
Affrontare per tempo la complessità dei mercati multipli
I rinnovi raramente avvengono in modo isolato. I portafogli globali coinvolgono diversi agenti, distributori, organismi notificati e autorità.
Il coordinamento comprende solitamente:
- Produttore che fornisce schede tecniche e dati PMS
- Agenti locali incaricati della gestione delle richieste e delle licenze
- Distributori che condividono dati relativi alle vendite e ai reclami
- Organismi notificati che rilasciano certificati di audit
Senza una chiara attribuzione delle responsabilità e senza scadenze precise, i ritardi si moltiplicano.
Un sistema centralizzato in grado di monitorare i requisiti specifici di ciascuna giurisdizione, lo stato delle richieste e le comunicazioni normative può ridurre notevolmente le difficoltà. È proprio in questo ambito che freya fusion RA , riunendo registrazioni, documenti e collaborazione tra le parti interessate in un unico spazio di lavoro normativo unificato.
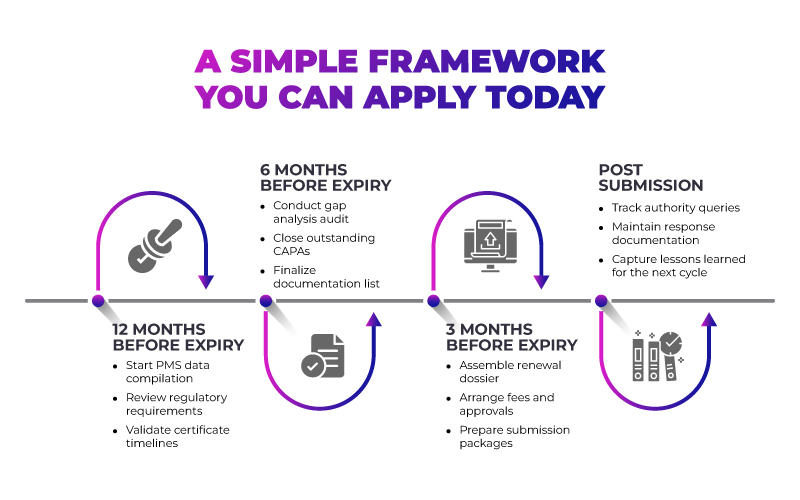
Questo approccio graduale trasforma il rinnovo in un processo prevedibile anziché in una crisi ricorrente.
Il rinnovamento riguarda la continuità, non solo la conformità
Il rinnovo della registrazione dei dispositivi medici mira, in definitiva, a garantire un accesso ininterrotto al mercato. Se gestito in modo strategico, rafforza i sistemi di qualità, migliora la disciplina relativa al sistema di monitoraggio post-commercializzazione (PMS) e rafforza la fiducia delle autorità di regolamentazione.
RA svolgono già ogni giorno un lavoro impegnativo. La sfida consiste nel dare a quel lavoro struttura, visibilità e continuità.
In questo caso, piattaforme come freya fusion entrano in gioco. Unificando registrazioni, documenti, PMS e collaborazione, aiutano RA a passare da rinnovi reattivi a una gestione proattiva del ciclo di vita normativo.
Sei pronto a semplificare il rinnovo delle autorizzazioni dei tuoi dispositivi medici?
Se i rinnovi vi sembrano ancora frammentari, manuali o stressanti, forse è giunto il momento di ripensare alla struttura delle vostre operazioni normative.
Scopri come freya fusion, con le sue funzionalità AI-First, supporti RA dei dispositivi medici con il monitoraggio centralizzato delle registrazioni, il controllo dei documenti e la visibilità del ciclo di vita, il tutto progettato per i professionisti del settore normativo, non per i team IT.
Prenota oggi stesso una demo e fai il primo passo verso una rinnovata fiducia, una conformità costante e una continuità operativa più fluida.









