BIMO sta per Bioresearch Monitoring, un programma di ispezioni in loco e audit dei dati per monitorare tutti gli aspetti della condotta e della rendicontazione della ricerca regolamentata dalla Food and Drug Administration (FDA) degli Stati Uniti. Il programma è stato istituito nel 1977 dopo che è stata identificata la necessità di verificare i siti di ricerca clinica. L'obiettivo principale di questo programma è garantire la qualità e l'integrità dei dati presentati per le approvazioni di nuovi prodotti e le domande di commercializzazione. Inoltre, questo programma protegge anche i diritti e il benessere dei soggetti umani e animali coinvolti nella ricerca regolamentata dalla FDA.
Gli obiettivi chiave del Programma BIMO
Ogni anno vengono condotte oltre 1000 ispezioni. Gli obiettivi principali del programma BIMO sono:
- Audit dei dati clinici
- Ispezione della ricerca clinica in corso
- Ispezione dei laboratori non clinici
- Ispezione dei Comitati Etici Istituzionali (IRB)
Quali prodotti rientrano nell'ambito dell'Audit BIMO?
Il BIMO è applicabile a farmaci, prodotti biologici, dispositivi medici, prodotti alimentari, prodotti del tabacco e prodotti veterinari. Il programma di conformità è supervisionato dai sei centri di prodotto della FDA: Center for Biologics Evaluation and Research (CBER), Center for Devices and Radiological Health (CDRH), Center for Drug Evaluation and Research (CDER), Center for Food Safety and Applied Nutrition (CFSAN), Center for Tobacco Products (CTP) e Center for Veterinary Medicine (CVM).
Quali aziende sono soggette all'Audit BIMO?
Sia le aziende nazionali che quelle internazionali che svolgono o rientrano in una delle attività elencate di seguito sono soggette ai requisiti del Monitoraggio della Ricerca Biologica -
- Laboratori di test non clinici per la conformità alle Buone Pratiche di Laboratorio (GLP)
- Sperimentatori clinici per la conformità alle Buone Pratiche Cliniche (GCP)
- Sponsor
- Organizzazioni di Ricerca a Contratto (CRO)
- Monitor di studi clinici
- Strutture per la bioequivalenza in vivo
- Comitati Etici Istituzionali (IRB)
Quali programmi di conformità rientrano nel programma BIMO?
La FDA degli US può condurre un audit BIMO in qualsiasi momento attraverso i sette programmi di conformità multicentrici. Questi sette programmi di conformità multicentrici sono implementati tramite –
- Ispezione dello Sperimentatore Clinico (CI) e dello Sperimentatore Sponsor (SI)
- Ispezione del Comitato Etico Istituzionale (IRB)
- Ispezione dell'Organizzazione di Ricerca a Contratto/Sponsor/Monitor (CRO/S/M)
- Ispezione delle Buone Pratiche di Laboratorio (GLP)
- Ispezione di Bioequivalenza-Biodisponibilità (BEQ)
- Ispezione della segnalazione di esperienze avverse da farmaco post-commercializzazione (PADE)
- Ispezione sulla segnalazione del piano di valutazione e mitigazione del rischio (REMS)
Ciascuno di questi programmi delinea un ambito dettagliato di revisione o ispezione da condurre per garantire la conformità con la FDA.
Quali regolamenti sono applicabili per l'Audit BIMO?
I regolamenti - 21 CFR 50 - Protezione dei Soggetti Umani, 21 CFR 54 - Divulgazione Finanziaria, 21 CFR 56 - IRBs, 21 CFR 58 - Buone Pratiche di Laboratorio per i laboratori non clinici, 21 CFR 809 - Prodotti Diagnostici In Vitro e 21 CFR 812 - Esclusione per Dispositivi Sperimentali sono applicabili per l'Audit BIMO.
Quanti audit vengono condotti annualmente nell'ambito del Programma BIMO?
Il numero di audit BIMO condotti dalla US FDA varia ogni anno. Negli ultimi anni, il numero di ispezioni in loco è diminuito a causa dell'insorgenza della pandemia di COVID-19, e la FDA ha dovuto sospendere tutta la sorveglianza in loco degli studi clinici. Solo studi clinici specifici, critici e cruciali, venivano monitorati.
Le “Valutazioni Regolatorie a Distanza” (RRA) sono state introdotte durante la pandemia di COVID-19 per monitorare a distanza la ricerca regolamentata. Le RRA sono condotte tramite videoconferenze e sono un'iniziativa volontaria per la valutazione a distanza dei dati e dei processi. Tuttavia, è importante notare che le RRA non sono equivalenti o un'alternativa all'ispezione in loco, ma sono semplicemente una procedura che si è evoluta a causa della pandemia di COVID-19.
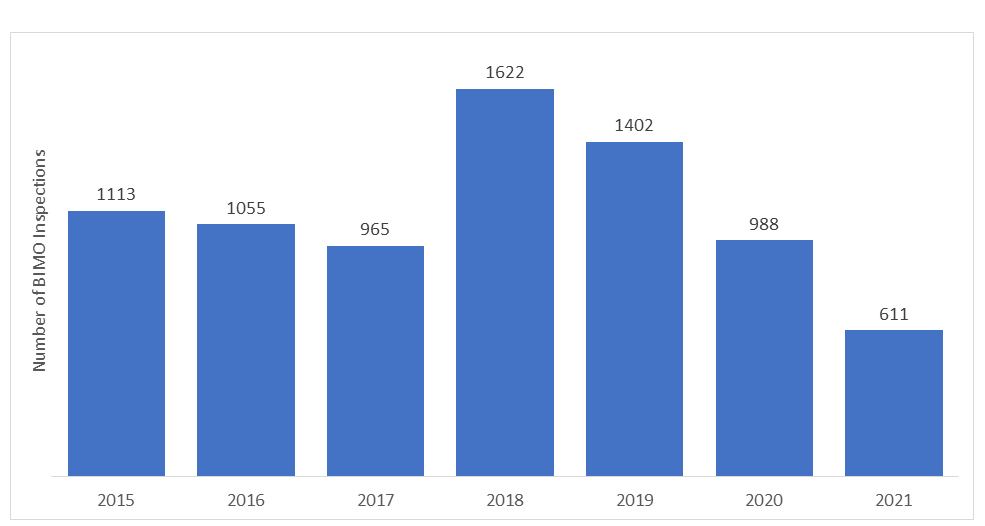
*I dati rappresentati per gli anni 2020 e 2021 non includono le ispezioni RRA
Quante Valutazioni Regolatorie Remote (RRA) sono state condotte durante la pandemia di COVID-19 nell'ambito del Programma BIMO?
Nel 2021, l'adozione dell'ispezione RRA è aumentata significativamente in tutti i programmi. Nell'aprile 2021, la FDA ha pubblicato un documento guida intitolato "Valutazioni Interattive Remote delle Strutture di Produzione di Farmaci e Monitoraggio della Bioricerca Durante l'Emergenza Sanitaria Pubblica COVID-19 - Guida per l'Industria", che fornisce informazioni esaustive sul processo della FDA per la conduzione delle RRA.
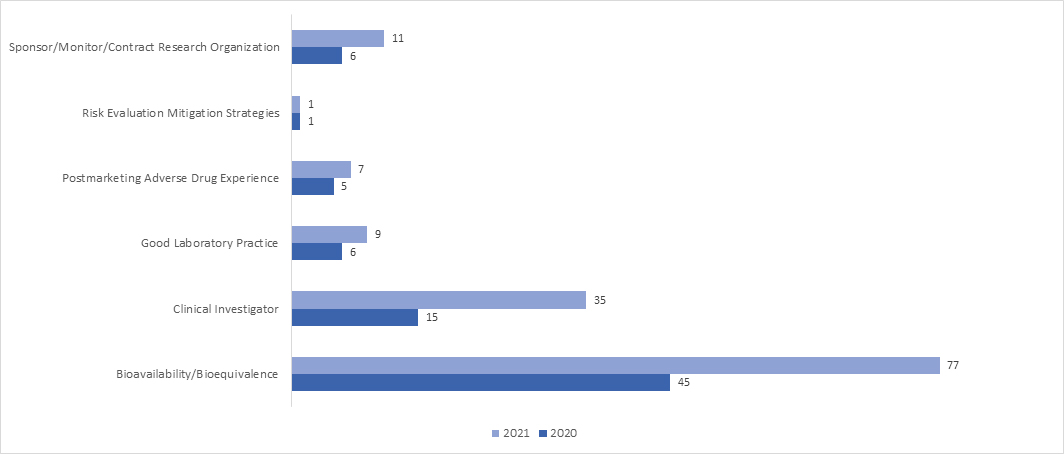
Quali sono i possibili esiti di un audit BIMO?
Durante l'audit BIMO, la US FDA può decidere di intraprendere una delle azioni elencate di seguito in base alla conformità –
1. Nessuna Azione Indicata (NAI)
NAI è applicabile quando l'ispettore sul campo della FDA non ha identificato alcuna pratica discutibile o solo problemi minori per i quali non è giustificabile alcuna ulteriore azione.
2. Azione volontaria indicata (VAI)
VAI è applicabile quando sono state identificate pratiche discutibili ma non sono significative.
3. Azione ufficiale indicata (OAI)
L'OAI è applicabile quando vengono identificate pratiche contestabili che compromettono l'integrità dei dati e/o i diritti dei soggetti umani.
Quali sono le non conformità più comuni riscontrate durante un audit BIMO?
Alcune delle non conformità più comuni osservate durante l'Audit BIMO sono –
- Mancanza di una corretta tenuta dei registri
- Mancato rispetto del piano investigativo
- Mancato rispetto delle normative
- Mancato monitoraggio dei protocolli
- Protezione inadeguata dei soggetti
- Tracciabilità inadeguata del prodotto oggetto di indagine
L'audit BIMO è cruciale per qualsiasi sviluppatore o produttore di nuovi dispositivi medici e tecnologie che intendono lanciare il loro dispositivo nel mercato US. Rispettare le normative e le linee guida per evitare qualsiasi delle insidie descritte è molto importante.
Hai bisogno di assistenza per le ispezioni di audit BIMO? Contatta Freyr. Rimani informato. Rimani conforme.