La redazione normativa svolge un ruolo cruciale nelle industrie farmaceutiche e sanitarie, collegando informazioni scientifiche complesse e vari stakeholder. L'arte di adattare la redazione normativa a diversi pubblici è essenziale per una comunicazione efficace e la conformità. Questo blog esplorerà come adattare la redazione normativa per tre pubblici chiave: pazienti, clinici e autorità di regolamentazione.
Comprendere l'importanza della scrittura specifica per il pubblico
La redazione normativa comprende vari documenti, ognuno con uno scopo specifico e destinato a lettori diversi. La capacità di adattare i contenuti a questi diversi pubblici è fondamentale per garantire che le informazioni siano accurate, ma anche accessibili e utilizzabili.
Punti chiave primari considerando l'approccio personalizzato:
Scrivere per i pazienti: semplificare informazioni complesse
Nella redazione di documenti normativi per i pazienti, l'obiettivo primario è trasmettere informazioni essenziali in modo chiaro e comprensibile senza sacrificare l'accuratezza.
- Utilizzo del linguaggio semplice
Usa parole di uso comune ed evita il gergo tecnico. Quando i termini medici sono necessari, fornisci spiegazioni chiare.
- Ausili Visivi e Formattazione
Incorporare diagrammi, grafici e infografiche per illustrare concetti complessi. Utilizzare elenchi puntati, titoli e paragrafi brevi per migliorare la leggibilità.
- Affrontare le preoccupazioni comuni
Anticipare e affrontare potenziali domande o preoccupazioni che i pazienti potrebbero avere riguardo al farmaco o al trattamento.
Esempio: Foglietti illustrativi per i pazienti
Questi documenti dovrebbero:

Scrivere per i clinici: bilanciare dettaglio e praticità
I clinici necessitano di informazioni complete ma concise per prendere decisioni informate sulla cura dei pazienti. La redazione regolatoria per questo pubblico deve bilanciare il dettaglio scientifico e l'applicabilità pratica.
- Enfasi sulla rilevanza clinica
Concentrarsi sulle informazioni che influenzano la cura del paziente, come le linee guida sul dosaggio, le controindicazioni e le interazioni farmacologiche.
- Presentazione Strutturata dei Dati
Organizzare i risultati degli studi clinici e i dati di sicurezza in un formato logico e facile da consultare. Utilizzare tabelle e grafici per riassumere i risultati chiave.
- Inclusione di Raccomandazioni Basate sull'Evidenza
Fornire indicazioni chiare e basate su prove sull'uso appropriato di farmaci o dispositivi medici in vari scenari clinici.
Esempio: Informazioni sulla prescrizione
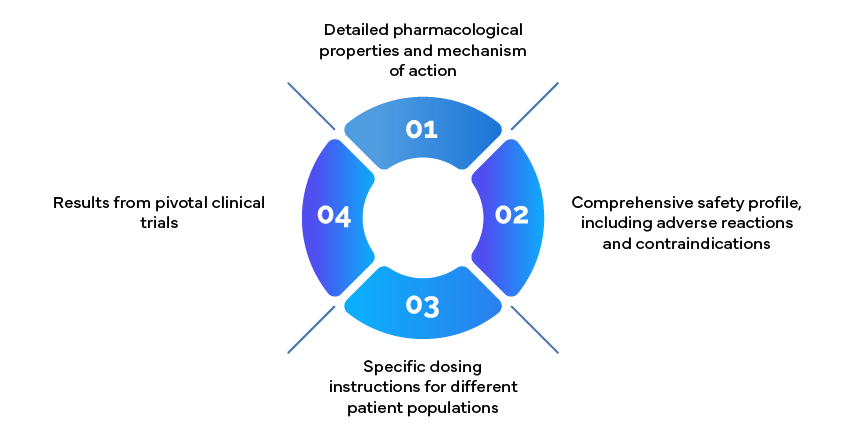
I documenti di informazione sulla prescrizione, noti anche come foglietti illustrativi, sono risorse fondamentali per i medici. Questi dovrebbero includere:
Scrivere per le autorità di regolamentazione: precisione e conformità
Le agenzie di regolamentazione richiedono una documentazione esaustiva e scientificamente rigorosa per valutare la sicurezza e l'efficacia dei nuovi prodotti. La redazione per questo pubblico richiede un'attenzione meticolosa ai dettagli e una rigorosa aderenza alle linee guida normative.
- Adesione alle linee guida normative
Assicurarsi che tutti i documenti siano conformi ai requisiti specifici di formato e contenuto degli organismi di regolamentazione come la FDA o l'EMA.
- Presentazione Completa dei Dati
Fornire un'analisi approfondita di tutti i dati pertinenti, incluse descrizioni dettagliate delle metodologie di studio, delle analisi statistiche e dell'interpretazione dei risultati.
- Trasparenza nella Segnalazione
Rivelare eventuali limitazioni o potenziali pregiudizi nella ricerca e affrontare come questi fattori possano influenzare le conclusioni.
Esempio: Rapporti di studi clinici
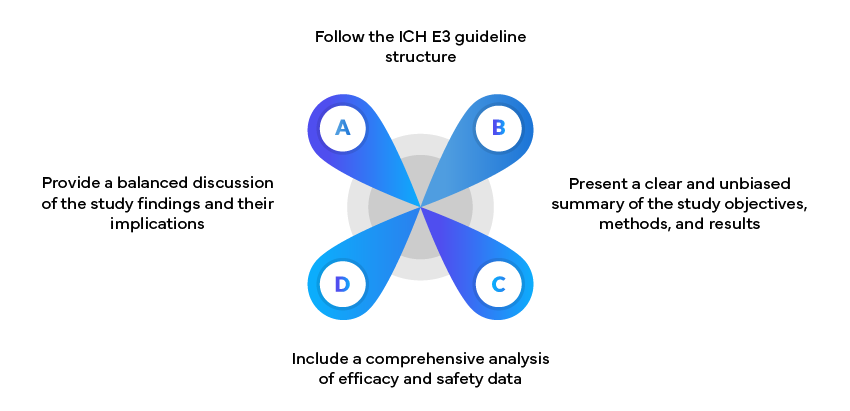
I Rapporti di Studi Clinici (CSR) sono documenti fondamentali nelle sottomissioni regolatorie. Essi dovrebbero:
Conclusione
Personalizzare la scrittura regolatoria per diversi pubblici è un compito complesso ma essenziale nelle industrie farmaceutica e sanitaria. Adattando i contenuti e gli stili di presentazione per soddisfare le esigenze specifiche di pazienti, clinici e autorità di regolamentazione, gli autori possono garantire che le informazioni critiche siano comunicate e comprese in modo efficace.
La capacità di redigere documenti normativi chiari, accurati e appropriati per il pubblico non è solo una questione di conformità; influisce direttamente sulla sicurezza dei pazienti, sul processo decisionale clinico e sullo sviluppo e la commercializzazione di successo di nuovi prodotti sanitari. Poiché il panorama normativo continua ad evolversi, l'importanza di una scrittura normativa qualificata in grado di colmare il divario tra dati scientifici complessi e le diverse esigenze degli stakeholder non farà che aumentare. I redattori normativi svolgono un ruolo cruciale nel promuovere la salute pubblica e favorire l'innovazione nel campo medico, concentrandosi sulla chiarezza per i pazienti, sulla rilevanza clinica per gli operatori sanitari e sulla precisione completa per le autorità di regolamentazione. Padroneggiare l'arte della scrittura normativa specifica per il pubblico è quindi una competenza inestimabile nell'ambiente sanitario in rapida evoluzione di oggi.










