Lorsque la pandémie de COVID-19 a été reconnue pour la première fois comme une crise sanitaire mondiale en 2020, les Autorités sanitaires (AS) mondiales ont pris des mesures innovantes pour y faire face de la meilleure manière possible. De même, les entreprises pharmaceutiques ont mis au point plusieurs vaccins/Produits médicaux au profit du public. Cependant, l'enregistrement des produits s'est avéré assez difficile. Pour simplifier l'enregistrement tout en maintenant leur sécurité, leur qualité et leur efficacité, les AS ont accordé des Autorisations d'utilisation d'urgence (AUU) à quelques vaccins et produits pertinents.
La question peut se poser de savoir comment les autorités sanitaires ont pu s'assurer que les bénéfices desdits produits l'emportaient sur les risques. La réponse réside dans l'adoption des meilleures pratiques de pharmacovigilance (PV).
Qu'est-ce que la pharmacovigilance ?
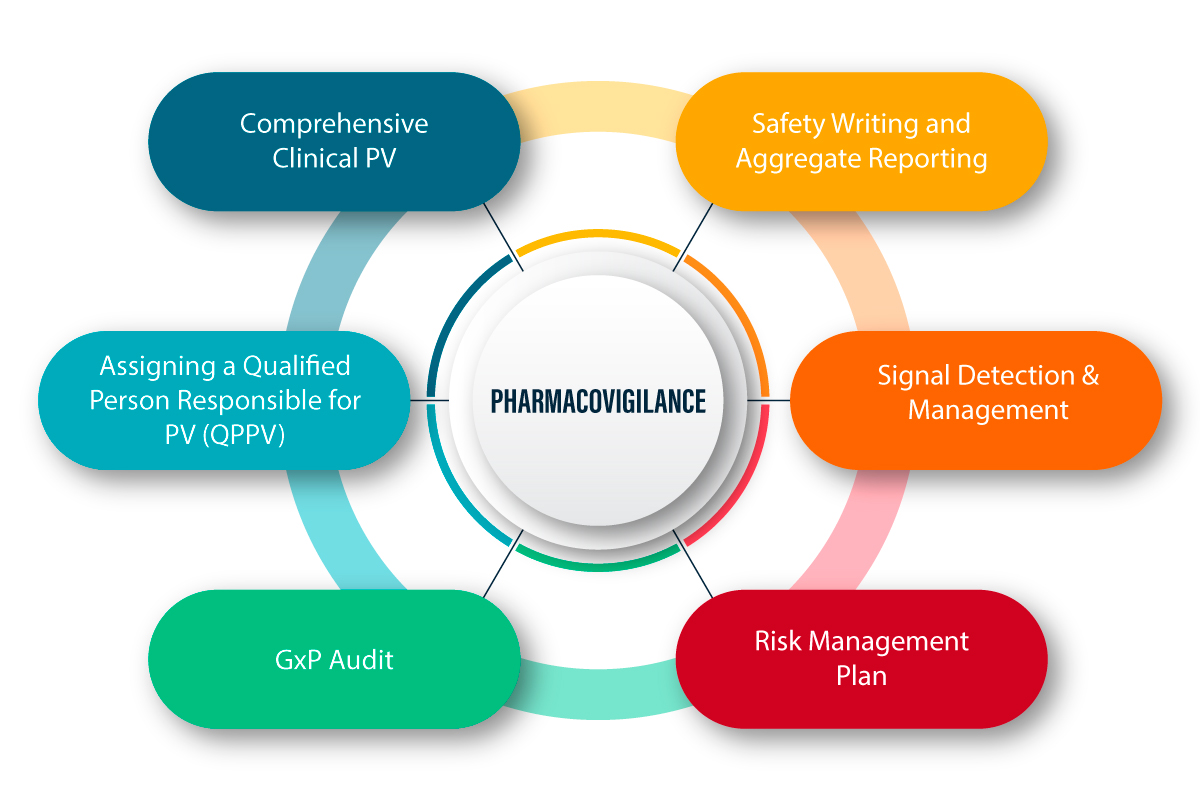
La PV est définie comme un ensemble d'activités scientifiques liées à la détection, à l'évaluation, à la compréhension et à la prévention des effets indésirables et de tout autre problème lié aux médicaments. Voici une explication imagée du fonctionnement de la PV et du processus qui y est associé.
La PV pendant la pandémie de COVID-19
Lorsque la pandémie de COVID-19 a commencé à se propager dans le monde, les vaccins et les produits médicaux pertinents ont dû être introduits sur le marché dans un délai limité tout en maintenant les normes de qualité requises. Dans de tels scénarios, il y avait moins de sujets disponibles pour les essais cliniques pendant la phase de développement des médicaments/vaccins, et le processus devait être achevé plus rapidement que la normale. Cela pouvait entraîner l'apparition de certains effets indésirables dans la phase post-approbation.
Par conséquent, l'équilibre bénéfice-risque des vaccins/produits médicaux était considéré comme primordial. Grâce à une communication rapide des réactions indésirables et des effets secondaires nocifs, l'efficacité des produits a été maintenue en temps réel.
Voici quelques-unes des activités clés de pharmacovigilance (PV) qui ont contribué à maintenir la sécurité, la qualité et l'efficacité desdits produits pendant la pandémie :
- L'adoption d'un bon plan de gestion des risques
- Évaluation des risques à l'aide des Rapports périodiques actualisés de sécurité (RPAS)
- Compilation des données d'exposition
- Études de sécurité post-autorisation (PASS).
- Déclaration spontanée des réactions indésirables suspectées
- Gestion efficace des signaux
PV en Affaires Réglementaires (RA)
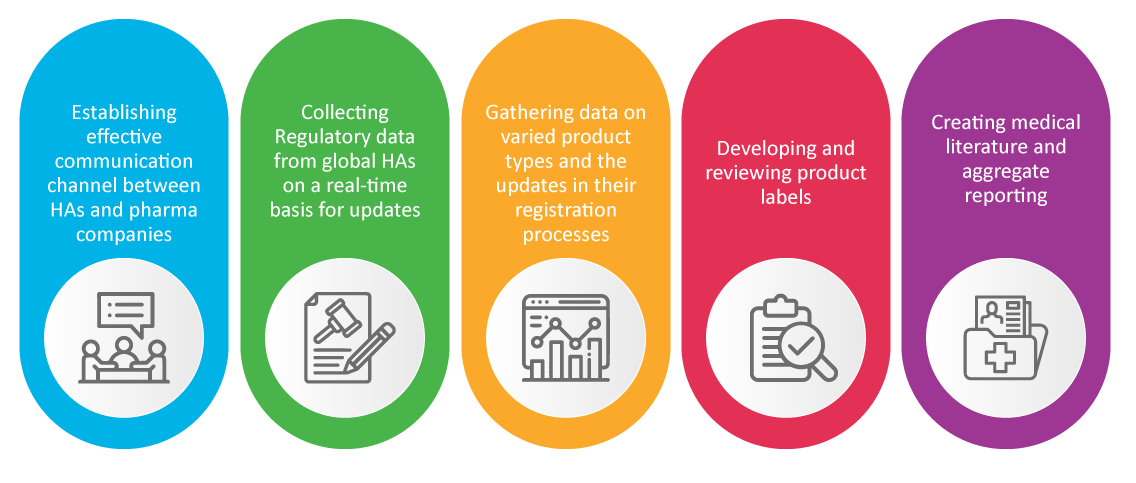
Il est bien connu que l'équipe des Affaires Réglementaires (RA) d'une entreprise pharmaceutique est responsable de la sécurité et de l'approbation des nouveaux produits. Les spécialistes RA s'occupent des activités de pharmacovigilance qui se sont avérées cruciales pendant la pandémie, telles que :
Conclusion
En conclusion, la PV aide à surveiller et à signaler la sécurité d'un produit pharmaceutique. Avec des rapports d'étude de cas individuels (ICSR) personnalisés, il devient plus facile pour les fabricants/promoteurs de se conformer aux réglementations respectives des autorités sanitaires mondiales. Cherchez-vous un soutien réglementaire pour la préparation des ICSR ? Consultez un expert réglementaire éprouvé pour la conformité. Contactez Freyr.










