
La publicité directe aux consommateurs (DTC) pour les médicaments est devenue un sujet de discussion privilégié ces dernières années. Ces publicités, destinées aux consommateurs plutôt qu'aux professionnels de la santé, ont été reconnues pour avoir accru la sensibilisation des patients et la demande pour certains médicaments. Cependant, elles ont également été critiquées pour pouvoir potentiellement entraîner un surdiagnostic et un surtraitement.
En observant les tendances actuelles au sein des entreprises pharmaceutiques, il est établi que les dépenses totales en marketing dépassent leur budget de recherche. À l'échelle mondiale, 1,42 billion de dollars ont été dépensés en marketing. Aux US, 486,62 milliards de dollars ont été consacrés en 2021 à la commercialisation de médicaments auprès des médecins ; au Canada, 29 305,1 millions de dollars ont été dépensés en 2022. En détaillant ces chiffres, 56 % concernent les échantillons gratuits, 25 % le « démarchage » des médecins par les représentants commerciaux pharmaceutiques (promotion directe de médicaments), 12,5 % la publicité directe auprès des utilisateurs, 4 % le démarchage auprès des hôpitaux, et 2 % les publicités dans les revues2. Parfois, des pratiques de marketing négatives peuvent avoir un impact sur les patients et les professionnels de la santé.
Types d'actions promotionnelles pour les médicaments
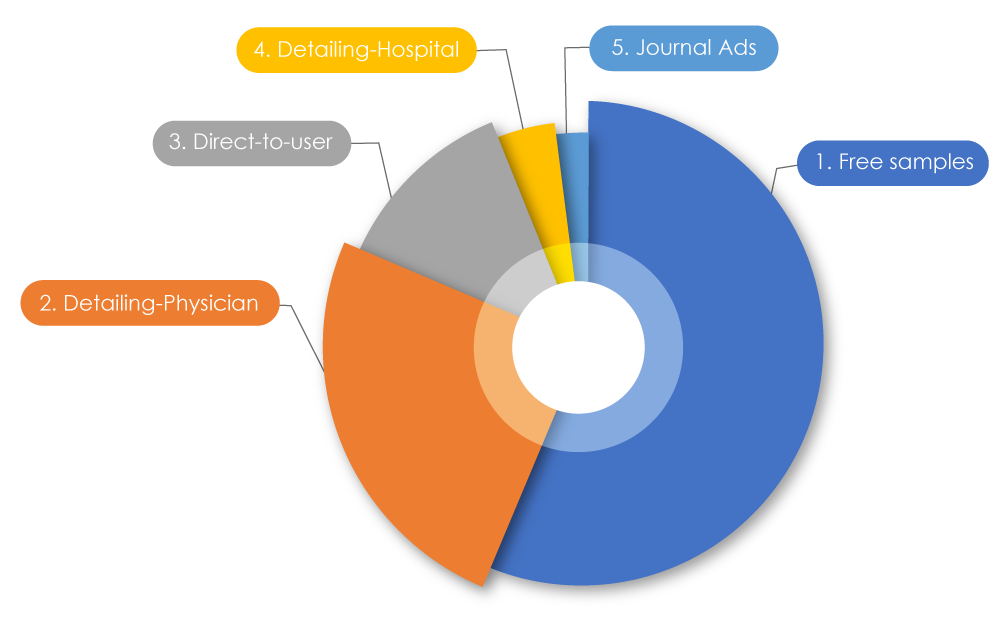
Source : Marketing pharmaceutique - Wikiwand
Publicité pharmaceutique destinée au grand public
Des restrictions sont imposées sur la publicité des médicaments sur ordonnance auprès du grand public, également appelée publicité directe auprès des consommateurs (DTC). Pour promouvoir les médicaments sur ordonnance auprès du public, la communication doit répondre à certaines exigences fondamentales :
- La conformité de la publicité et de la promotion des médicaments sur ordonnance aux indications autorisées repose sur l'usage prévu pour lequel le produit a été approuvé par la FDA l'étiquetage du médicament FDA). L'étiquetage fournit des informations sur la manière d'utiliser le produit de manière sûre et efficace pour l'indication approuvée. La publicité et la promotion qui ne sont pas conformes à l'étiquetage FDA sont considérées comme des promotions illégales « hors AMM ».
- La promotion et la publicité des médicaments sur ordonnance exigent un juste équilibre entre les bénéfices et les risques du produit, en veillant à ce que ces informations soient comparables en termes de profondeur, de détail et de contexte.
- Les allégations doivent être étayées par des preuves suffisamment solides ou une expérience clinique
- Véridique et non trompeur - Si la publicité et la promotion des médicaments sur ordonnance sont fausses ou trompeuses de quelque manière que ce soit, elles seront considérées comme mal étiquetées en vertu du Federal Food, Drug, and Cosmetic Act (FDCA) et sujettes à des mesures d'exécution.
- Utilisation d'un langage accessible aux consommateurs, en évitant le langage technique, les termes scientifiques et le jargon médical dans la publicité et la promotion destinées aux consommateurs. Cela doit être conforme à l'étiquetage ou à la monographie approuvée du produit.
Informations contenues dans la publicité pharmaceutique destinée au grand public.
La publicité et la promotion des médicaments sur ordonnance destinées aux consommateurs doivent comporter les éléments essentiels suivants, conformément aux dispositions de la FDCA et aux réglementations de la Food and Drug Administration (FDA).
- Les noms commerciaux et les noms établis doivent être conformes aux dispositions de FDA
- Il doit inclure la quantité des ingrédients du médicament annoncé.
- Il doit inclure un « bref résumé » qui divulgue chaque effet secondaire, avertissement, précaution et contre-indication. Il est principalement axé sur les informations importantes relatives aux risques plutôt que sur une liste exhaustive des risques liés au produit. La plupart des risques sont présentés de manière à être les plus facilement compréhensibles par les consommateurs.
- Les risques majeurs du produit doivent être présentés de manière claire, visible et neutre sous forme de « déclaration majeure »
- Les mentions d'information relatives aux effets indésirables figurant dans les publicités destinées directement au grand public doivent inclure la mention MedWatch suivante, imprimée en caractères bien visibles : « Nous vous encourageons à signaler les effets indésirables des médicaments sur ordonnance à la FDA. Rendez-vous fda ou appelez le +1–800-FDA-1088FDA
- Les mentions de rappel et la publicité sont exemptées des exigences générales. Il est important de noter que les mentions de rappel et la publicité ne sont pas autorisées pour un médicament soumis à prescription dont l'étiquetage FDA comporte une mise en garde encadrée.
Pour la publicité de médicaments DTC, contactez-nous.
Pour la publicité directe aux consommateurs (DTC) pour les médicaments
Restrictions concernant les interactions entre les patients ou les organisations de patients et l'industrie
Les interactions entre les entreprises pharmaceutiques et les patients/organisations de patients ne sont autorisées que dans quelques pays, tels que les US, mais avec des limitations, telles que :
- Doit être conforme à l'étiquetage/CFL
- Juste et équilibré
- Dûment étayé et
- Non fausse ou trompeuse par ailleurs
De plus, les interactions avec les clients ne doivent pas enfreindre la loi anti-rétrocommission en incitant les associations de patients ou les patients à recommander ou à utiliser le produit annoncé.
Au Royaume-Uni, la publicité directe aux consommateurs (DTC) est autorisée pour les produits pharmaceutiques, mais exclut les enfants. La publicité des médicaments sur ordonnance auprès du public est interdite. Les publicités doivent inclure le nom du produit et le nom de l'ingrédient actif. Les échantillons de produits ou les bons permettant aux consommateurs d'obtenir le produit gratuitement ou à un prix déraisonnablement bas ne sont pas autorisés.
En Allemagne, la publicité auprès du public est autorisée pour les Produits médicaux exclusivement destinés aux enfants de moins de 14 ans. La publicité des médicaments soumis à prescription auprès du public est interdite. Mais il existe également des règles spéciales pour la publicité des Produits médicaux en dehors des cercles professionnels. Ces règles spéciales sont principalement énoncées dans la loi sur la publicité des médicaments (Heilmittelwerbegesetz, « HWG ») et ont été modifiées par la loi allemande sur les Produits médicaux (Arzneimittelgesetz – « AMG ») pour être conformes à la directive 2001/83/CE4.
Débat sur la possibilité de la publicité pour les médicaments à l'ère numérique
Les défenseurs de la publicité directe aux consommateurs (DTC) pour les médicaments affirment qu'elle donne du pouvoir aux patients en leur fournissant des informations sur les options de traitement. Ils soulignent également que cela peut entraîner une augmentation de la demande de médicaments, ce qui peut être bénéfique pour les entreprises pharmaceutiques.
D'un autre côté, les détracteurs de la publicité directe aux consommateurs (DTC) pour les médicaments soutiennent qu'elle peut entraîner un surdiagnostic et un surtraitement. Ils affirment que ces publicités exagèrent souvent les avantages des médicaments tout en minimisant leurs risques, ce qui pousse les patients à demander à leurs médecins des médicaments dont ils n'ont peut-être pas besoin. De plus, ils déclarent que cela peut entraîner une augmentation des coûts des soins de santé, car les patients peuvent se voir prescrire des médicaments de marque plus chers plutôt que des alternatives génériques moins coûteuses.
Malgré le débat qui fait rage, la publicité directe auprès des consommateurs (DTC) pour les médicaments est là pour rester. La FDA publié des lignes directrices relatives à ce type de publicité, qui comprennent des exigences en matière de divulgation des risques et d'équilibre équitable entre les avantages et les risques. En conclusion, la publicité DTC pour les médicaments a le potentiel d'informer les patients et d'accroître la demande pour certains médicaments. Cependant, il est également important de prendre en compte les inconvénients potentiels et d'être conscient des limites des informations fournies dans ces publicités. Comme toujours, il est important de consulter votre professionnel de santé avant de prendre tout médicament. Reach les experts de Freyr pour end-to-end !










