Présentation et définition
Les fusions et acquisitions (F&A) dans le secteur des dispositifs médicaux s'accompagnent de défis réglementaires complexes dans plusieurs juridictions. L'intégration de deux entreprises nécessite d'harmoniser les systèmes de gestion de la qualité (SGQ), de gérer les demandes d'autorisation réglementaire et d'aligner les processus cliniques et post-commercialisation.
Les services de Freyr en matière de fusions-acquisitions et de réglementation des dispositifs médicaux offrent end-to-end pour aider votre organisation à relever ces défis en toute sérénité, tout en garantissant le respect constant de ISO 13485, du règlement MDR, FDA et d'autres normes internationales.
Processus de conformité en matière de fusions-acquisitions dans le secteur des dispositifs médicaux
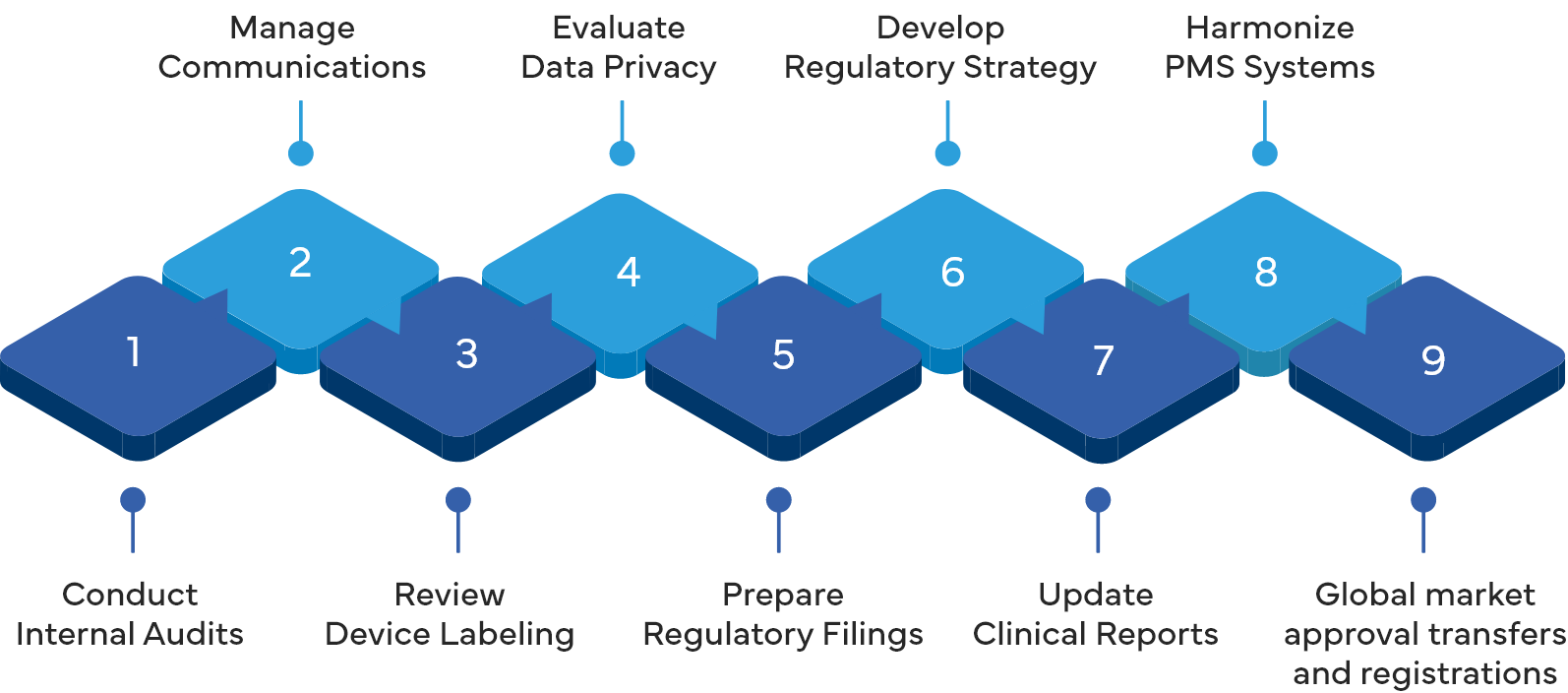
Les services de Freyr
INTÉGRATION DU PMS
- Fusionner les systèmes de gestion des stocks (PMS) des deux entreprises.
- Harmonisation des processus de notification des événements indésirables et d'analyse des tendances.
DILIGENCE RAISONNABLE EN MATIÈRE DE RÉGLEMENTATION
- Évaluation exhaustive de la conformité réglementaire de la société cible, notamment en ce qui concerne le système de gestion de la qualité (SGQ), les enregistrements de produits, les données cliniques et l'étiquetage.
- Identification des risques réglementaires et des responsabilités potentiels.
- Analyse des écarts et planification des mesures correctives.
STRATÉGIE ET PLANIFICATION RÉGLEMENTAIRES
- Élaborer une stratégie réglementaire globale visant à intégrer les gammes de produits des deux sociétés.
- Planification du transfert et de la mise à jour des enregistrements réglementaires et des licences sur l'ensemble des marchés concernés.
- Élaboration d'un calendrier pour les activités réglementaires.
INTÉGRATION DU SYSTÈME DE GESTION DE LA QUALITÉ ET DES ACTIONS CORRECTIVES ET PRÉVENTIVES
- Harmoniser les systèmes de gestion de la qualité des deux entreprises afin de garantir la conformité à ISO 13485 aux autres normes applicables.
- Élaborer et mettre en œuvre un système unifié de documentation du système de gestion de la qualité.
- Réalisation d'audits internes et d'analyses des écarts.
- Dossiers réglementaires et enregistrements :
- Préparer et soumettre tous les documents réglementaires nécessaires au transfert et à la mise à jour des enregistrements de produits.
- Gestion des relations avec les autorités de régulation.
INTÉGRATION DE LA PROTECTION DES DONNÉES ET DE LA CYBERSÉCURITÉ
- Réaliser une évaluation approfondie des risques liés à la confidentialité des données et à la cybersécurité.
- Élaborer et mettre en œuvre un plan visant à intégrer les systèmes de protection des données et de cybersécurité.
- Garantir le respect du RGPD et des autres réglementations applicables.
- Cartographie de toutes les données transférées.
MISE À JOUR DES FICHES TECHNIQUES
- Gestion des données cliniques et de l'évaluation :
- Évaluation de la validité et de la transférabilité des données cliniques.
- Mettre à jour les rapports d'évaluation clinique (REC) selon les besoins.
- Gestion des activités de suivi clinique après la mise sur le marché (PMCF).
CONFORMITÉ EN MATIÈRE D'ÉTIQUETAGE
- Révision et mise à jour des supports d'étiquetage afin de refléter le changement de propriétaire et de garantir le respect de la réglementation locale.
- Élaborer une stratégie d'étiquetage cohérente.
Défi
Les services de Freyr et notre accompagnement
Variations dans le niveau de maturité et l'état de conformité des systèmes de gestion de la qualité
Services d'harmonisation des systèmes de gestion de la qualité : notre équipe de consultants en fusions-acquisitions réalise des analyses des écarts et des audits internes afin d'harmoniser et d'aligner les systèmes de gestion de la qualité (SGQ) sur la norme ISO 13485 les exigences réglementaires, pour une intégration sans heurts.
Démarches réglementaires complexes et transferts d'enregistrement
Affaires réglementaires SoMAD (spin-off, fusions-acquisitions dans le secteur des dispositifs médicaux, cessions) Services : gestion des demandes d'autorisation, des transferts de licence et des communications avec les autorités réglementaires internationales afin de garantir l'obtention des autorisations dans les délais et le respect continu de la réglementation.
Garantir la conformité de l'étiquetage compte tenu du changement de propriétaire
Services de mise à jour et de conformité en matière d'étiquetage : Élaborer et mettre en œuvre des stratégies d'étiquetage harmonisées et conformes afin de refléter le changement de propriété et de respecter toutes les exigences réglementaires régionales.
Gestion des données d'évaluation clinique et PMCF
Gestion des données cliniques et des évaluations : évaluer la transférabilité des données cliniques, mettre à jour les rapports d'évaluation clinique (CER) et gérer les activités de suivi clinique post-commercialisation (PMCF).
Respecter les exigences en matière de protection des données et de cybersécurité
Évaluations en matière de protection des données et de cybersécurité : Évaluer et intégrer les systèmes de protection des données et de cybersécurité afin de garantir la conformité au RGPD et aux autres réglementations internationales.
Combiner les systèmes de surveillance post-commercialisation et les mécanismes de notification
Services SoMAD (Pharmacovigilance et Affaires médicales) : harmonisation des systèmes de surveillance post-commercialisation, de la notification des effets indésirables et de l'analyse des tendances, pour un suivi de la sécurité cohérent et conforme aux exigences réglementaires.
Nous ne proposons PAS
Conseil juridique en matière de fusions et acquisitions dans le secteur des dispositifs médicaux
Conseil financier ou transactionnel
Services d'intégration de la production ou des opérations
Remarque : bien que nous agissions en tant que consultants en matière de fusions-acquisitions sur le plan réglementaire, nous nous concentrons exclusivement sur la conformité réglementaire et ne fournissons pas de services juridiques, financiers ou opérationnels liés aux fusions-acquisitions.
Pourquoi collaborer avec Freyr ?

Histoire de succès avérée
Entrée simplifiée sur le marché mondial pour une organisation de diagnostics dentaires pilotée par l'IA.
Une entreprise de diagnostic dentaire en phase de démarrage, axée sur l'IA, s'est associée à Freyr pour naviguer dans le paysage réglementaire mondial complexe.