Qu'est-ce que le QMSR ?
FDA constitue une approche simplifiée visant à s'aligner sur les exigences ISO 13485:2016, qui remplace l'ancienne structure du QSR. Cet alignement est essentiel car il facilite la mise en conformité à l'échelle mondiale pour les fabricants, en particulier ceux qui exercent leurs activités à l'international. Cette harmonisation permettra aux entreprises de satisfaire aux exigences réglementaires tant aux US sur d'autres marchés de manière beaucoup plus cohérente.
Le QMSR impose des améliorations en matière de gestion des risques, de conception des dispositifs et de surveillance post-commercialisation. Cette mise à jour peut certes accroître la complexité, mais elle permet également aux fabricants d'harmoniser leurs procédures qualité, ce qui renforce la sécurité des dispositifs et améliore la documentation, un aspect qui peut s'avérer crucial lors USFDA .
Pourquoi le passage du QSR au QMSR est-il crucial ?

Conformité aux normes internationales
Cela aidera les fabricants à s'aligner sur le système de gestion de la qualité (SGQ) mondial applicable aux dispositifs médicaux en adoptant les QMSR, ce qui permettra de réduire les redondances réglementaires pour les fabricants de dispositifs médicaux opérant à l'échelle mondiale.
Amélioration de la qualité, de la sécurité et de l'efficacité
Cette intégration garantit que les dispositifs sont fabriqués conformément aux exigences mondiales du système de gestion de la qualité. Cela aide le fabricant à améliorer la qualité et la sécurité des dispositifs.
Conformité réglementaire
Cela aide les fabricants à s'adapter aux nouvelles exigences et réduit ainsi le risque de non-conformité lorsque le règlement entrera en vigueur le 2 février 2026.
Principaux changements liés au passage du QSR au QMSR :
Harmonisation avec la terminologie de ISO 13485:2016
Cela garantit que les fabricants adoptent des normes reconnues à l'échelle mondiale.
Gestion des risques :
Il met l'accent sur la gestion des risques tout au long du cycle de vie du dispositif médical.
Conception et commandes de l'appareil
Conformément aux FDA , les contrôles de conception ont été élargis afin de garantir que les fabricants tiennent pleinement compte des besoins des utilisateurs, de la sécurité du dispositif et des critères de performance, ce qui constitue un axe prioritaire lors USFDA
Surveillance post-commercialisation
Les entreprises doivent renforcer leur système de surveillance post-commercialisation. Cela impliquera que les fabricants recueillent des informations sur la sécurité et l'efficacité des dispositifs, ce qui permettra d'identifier et de résoudre rapidement les problèmes.
Documentation et tenue des registres
La réglementation finale met l'accent sur la documentation, soulignant qu'une tenue rigoureuse des registres est essentielle lors de l'inspection.
Dates importantes
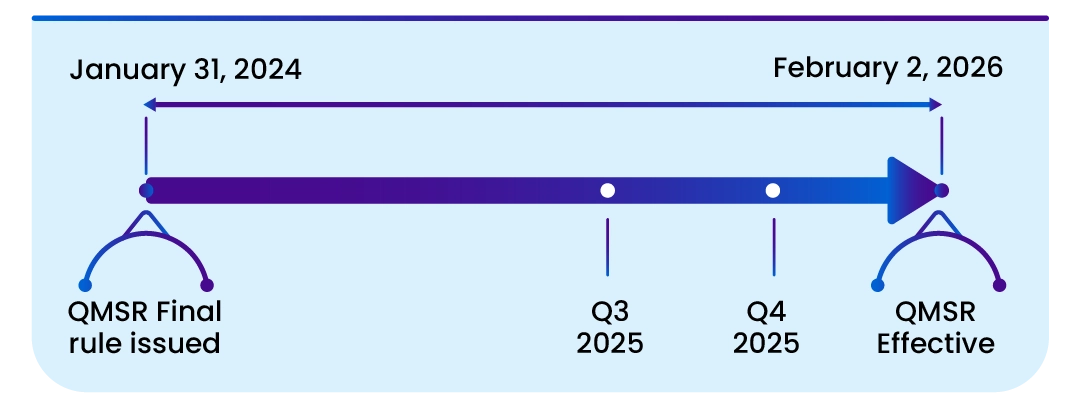
La présente règle entre en vigueur le 2 février 2026. L'incorporation par référence de certains documents mentionnés dans la présente règle a été approuvée par le directeur du Federal Register le 2 février 2024.
Bénéficiez des conseils d'experts pour assurer votre conformité à la norme QMSR
QMSR
- Classification des dispositifs médicaux selonFDA.
- Création de documents conformément à la norme 21 CFR 820.
- Analyse des écarts concernant les documents existants du système de gestion de la qualité (SGQ) conformément à la norme 21 CFR 820.
- Plan de remédiation pour la conformité au 21 CFR 820.
- Simulations d'audits.
- Une équipe dédiée d'assurance qualité (QA) d'experts en dispositifs médicaux.
- Expertise avérée dans la gestion de la conformité au 21 CFR 820.
- Modèles souples de réalisation de projets.




 La norme QMSR entrera en vigueur le 2 février 2026 ; les fabricants seront alors tenus de mettre à niveau leur système de gestion de la qualité.
La norme QMSR entrera en vigueur le 2 février 2026 ; les fabricants seront alors tenus de mettre à niveau leur système de gestion de la qualité. Une mise en œuvre dans les délais et une maintenance efficace peuvent réduire le risque de rappel de produits et de réclamations.
Une mise en œuvre dans les délais et une maintenance efficace peuvent réduire le risque de rappel de produits et de réclamations. Le respect des exigences du QMSR pourrait réduire le nombre de remarques formulées parFDA US ,FDA n'aura aucune incidence sur le statut du produit sur le marché réglementé.
Le respect des exigences du QMSR pourrait réduire le nombre de remarques formulées parFDA US ,FDA n'aura aucune incidence sur le statut du produit sur le marché réglementé.