
Les soumissions réglementaires et les tâches de publication ont toujours été laborieuses, nécessitant des heures d'efforts manuels pour le formatage des documents, la génération de PDF conformes aux exigences des agences, les contrôles qualité, l'assemblage des documents pour les soumissions, etc. Face aux délais serrés, les entreprises des sciences de la vie s'empressent toujours de soumettre leurs dossiers à temps. Partout dans le monde, les organismes de réglementation se préparent à adopter les développements récents tels que l'eCTD v4.0 pour les soumissions de dossiers, les modifications et autres rapports. L'eCTD v4.0 est une évolution progressive susceptible d'avoir un impact sur l'avenir des soumissions réglementaires, chaque pays se préparant à l'accepter et à le mettre en œuvre.
Compte tenu de tous les défis liés aux soumissions réglementaires, il est impératif de disposer d'une solution technologiquement avancée pour stimuler le processus de soumission et d'examen des médicaments. Étant donné que les organisations envisagent déjà l'automatisation comme partie intégrante du processus de soumission réglementaire, il est crucial d'examiner comment elle peut améliorer la productivité lors de la transition vers l'eCTD 4.0.
Comment l'automatisation aide à la transition vers l'eCTD 4.0 ?
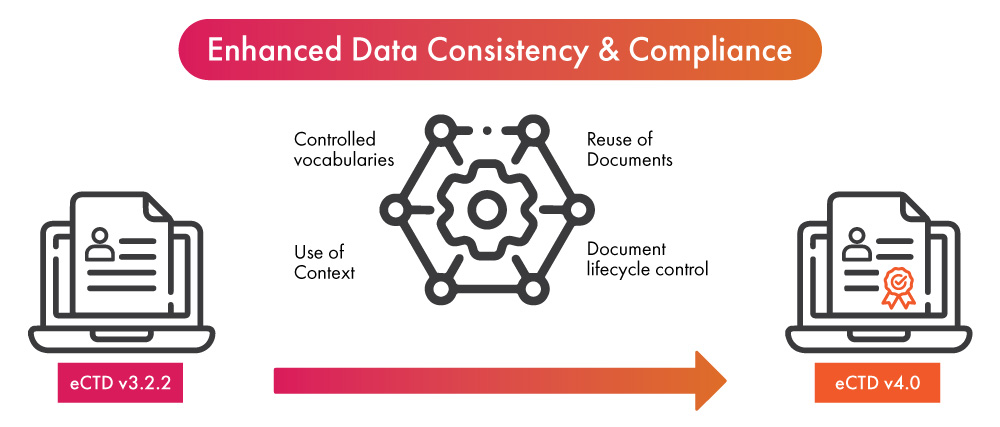
- À l'aube de l'adoption de la dernière version de l'eCTD, le déploiement de l'automatisation dans le processus de soumission réglementaire peut apporter de doubles avantages aux entreprises des sciences de la vie, notamment en assurant la conformité à l'eCTD v4.0 plus rapidement d'une part, et en améliorant la cohérence des données et la rationalisation du processus de soumission d'autre part.
- Une fois les données finalisées pour être utilisées dans un (01) dossier réglementaire, l'automatisation permet de les intégrer dans d'autres soumissions ou mises à jour. Cela tire parti de la nouvelle fonctionnalité de l'eCTD v4.0, qui permet désormais des remplacements de données de type plusieurs-à-un et plusieurs-à-plusieurs, facilitant ainsi la réutilisation des données de manière simplifiée.
- Les notifications automatisées éliminent le besoin de livrer des messages ou de passer des appels téléphoniques lorsque l'activité est requise. Elles permettent une communication plus rapide et plus claire, menant à des vocabulaires contrôlés, un composant essentiel de l'eCTD v4.0.
- L'automatisation de la soumission de documents contribuera à faciliter davantage le processus de mise à jour du contenu déjà soumis. Elle améliorera le contrôle du cycle de vie des documents soumis.
- L'automatisation dans les groupes de contexte peut accélérer le processus d'organisation de plusieurs fichiers destinés aux soumissions réglementaires.
Au milieu de la transition vers l'eCTD v4.0, il est crucial pour les organisations des sciences de la vie de s'associer à des fournisseurs qui sont prêts pour la nouvelle norme et comprennent comment automatiser et rationaliser le processus de publication réglementaire. Les entreprises doivent se préparer à adopter les dernières technologies rendues possibles par l'automatisation pour obtenir des avantages significatifs et un avantage concurrentiel sur le marché. L'eCTD v4.0 est un changement majeur qui intervient après une longue période. Les organisations doivent commencer leur preuve de concept pour tâter le terrain, car elle sera bientôt acceptée dans de nombreux pays du monde, en fonction des calendriers de chaque pays.
Chez Freyr, nous sommes à l'avant-garde de l'innovation technologique et nous sommes prêts à accompagner nos clients en rendant notre logiciel de soumission et de publication réglementaire – Freyr SUBMIT PRO compatible eCTD v4.0.
Pour en savoir plus sur la préparation de Freyr pour l'eCTD 4.0, veuillez cliquer ici pour télécharger la session de webinaire archivée.









