
Les Affaires Réglementaires (RA) jouent un rôle essentiel pour garantir la sécurité, l'efficacité et la qualité des produits pharmaceutiques dans le paysage pharmaceutique dynamique. Les Affaires Réglementaires (RA) relatives à la Chimie, la Fabrication et les Contrôles (CMC) sont essentielles pour la conformité. Elles visent à protéger la santé des patients et à promouvoir la confiance du public dans les produits pharmaceutiques en assurant la cohérence et la qualité tout au long du processus de fabrication des médicaments.
La CMC RA englobe les exigences en matière de documentation et de conformité liées à la fabrication, au contrôle qualité et à la stabilité des produits pharmaceutiques. Cela implique une attention particulière aux détails et le respect des directives réglementaires tout au long du cycle de vie du développement des médicaments. Pour en savoir plus sur l'importance de la CMC RA, consultez nos experts.
Dans ce blog, nous allons approfondir les fondamentaux de la CMC RA et explorer son importance pour atteindre la conformité et maintenir des normes de qualité élevées.
Le rôle du CMC dans le développement de médicaments
Les considérations CMC commencent tôt dans le processus de développement des médicaments et se poursuivent à toutes les étapes, de la recherche préclinique à la commercialisation. Les données et la documentation CMC sont des éléments essentiels des soumissions réglementaires, telles que les demandes d'autorisation de nouveau médicament expérimental (IND), les demandes d'autorisation de mise sur le marché (NDA) et les demandes d'autorisation de mise sur le marché (MAA). Les autorités réglementaires examinent les données CMC pour évaluer la sécurité, l'identité, la puissance et la qualité d'un produit médicamenteux, ainsi que la fiabilité et la cohérence du processus de fabrication.
Assurer la conformité avec CMC RA
Le respect des exigences réglementaires CMC est primordial pour une entrée réussie sur le marché. Les autorités réglementaires telles que la Food and Drug Administration des US (USFDA), l'Agence européenne des médicaments (EMA) et d'autres autorités sanitaires régionales (HA) sont chargées d'établir des lignes directrices et des normes qui doivent être respectées. Ces lignes directrices couvrent divers aspects, notamment les pratiques de fabrication, les systèmes qualité, les méthodes analytiques, les tests de stabilité et la validation. La conformité implique une documentation méticuleuse, le respect des bonnes pratiques de fabrication (BPF) et la mise en œuvre de systèmes de gestion de la qualité (QMS) efficaces.
Rôle de la conformité CMC dans le succès d'une entreprise pharmaceutique
Le maintien de normes élevées de conformité CMC offre plusieurs avantages aux entreprises pharmaceutiques. Certains des principaux avantages sont :
- Atténuation des risques réglementaires.
- Soutenir les approbations réglementaires réussies.
- Réduire la probabilité de rappels de produits.
- Favoriser une bonne réputation en matière de qualité et de fiabilité.
Points à considérer pour une fonction RA CMC réussie :
- Se tenir informé des connaissances réglementaires : Les exigences réglementaires évolutives des autorités sanitaires (HAs) nécessitent de se tenir au courant des dernières directives. Un suivi continu des mises à jour réglementaires et leur intégration dans les pratiques CMC sont cruciaux pour maintenir la conformité.
- Établir des systèmes qualité : Cela comprend l'élaboration et la maintenance de procédures opératoires standard (SOP) complètes, des procédures de contrôle des documents, des processus de contrôle des changements et des programmes de formation pour garantir que les employés comprennent et suivent les protocoles établis.
- Évaluation et atténuation des risques: Les entreprises doivent identifier les risques potentiels tout au long des processus de développement et de fabrication des médicaments et mettre en œuvre des stratégies d'atténuation des risques appropriées. Cela inclut l'évaluation des paramètres critiques du processus, de la variabilité des matières premières, des impuretés potentielles et des risques liés à la chaîne d'approvisionnement, ce qui garantit la conformité.
- Documentation et intégrité des données : Le maintien d'une documentation précise et complète est essentiel pour démontrer la conformité. Les entreprises doivent établir des pratiques de documentation robustes, y compris la tenue de dossiers de lots, de données analytiques, d'études de stabilité et de rapports de validation. Assurer l'intégrité, la traçabilité et la sécurité des données est essentiel pour éviter les problèmes de conformité.
- Gestion efficace des changements : Les entreprises doivent disposer de procédures de contrôle des changements bien définies pour évaluer et documenter les changements, évaluer leur impact sur la qualité des produits et la conformité réglementaire, et obtenir les approbations nécessaires avant de mettre en œuvre les changements.
- Partenariats et gestion solides des fournisseurs : Cela implique de sélectionner des fournisseurs qualifiés, de réaliser des audits et d'établir des accords de qualité qui définissent les responsabilités et les attentes. Il est essentiel de procéder à des évaluations régulières de la conformité des fournisseurs aux exigences des Bonnes Pratiques de Fabrication actuelles (BPFa).
- Préparation aux audits et inspections : Les entreprises devraient effectuer des auto-évaluations pour identifier les domaines à améliorer et assurer leur préparation aux audits réglementaires. En effet, traiter rapidement les conclusions d'audit et mettre en œuvre des actions correctives sont essentiels pour maintenir la conformité.
- Amélioration continue : Ceci peut être réalisé en encourageant l'engagement des employés, en offrant des formations et une éducation sur les exigences réglementaires, et en favorisant une mentalité axée sur la qualité à tous les niveaux de l'organisation.
- Traitement des Actions Correctives et Préventives (CAPA) : En traitant systématiquement les non-conformités à l'aide de la méthodologie CAPA, les entreprises pharmaceutiques peuvent démontrer leur engagement envers l'amélioration continue et la conformité.
- Connaissance des changements réglementaires post-approbation : Comprendre les exigences réglementaires pour les changements post-approbation est essentiel pour assurer la conformité. La mise en œuvre de processus de gestion du changement appropriés et une communication efficace avec les autorités de santé (HAs) peuvent aider à gérer ces changements tout en assurant la conformité.
Rôle d'un fournisseur de services réglementaires dans le processus de conformité CMC
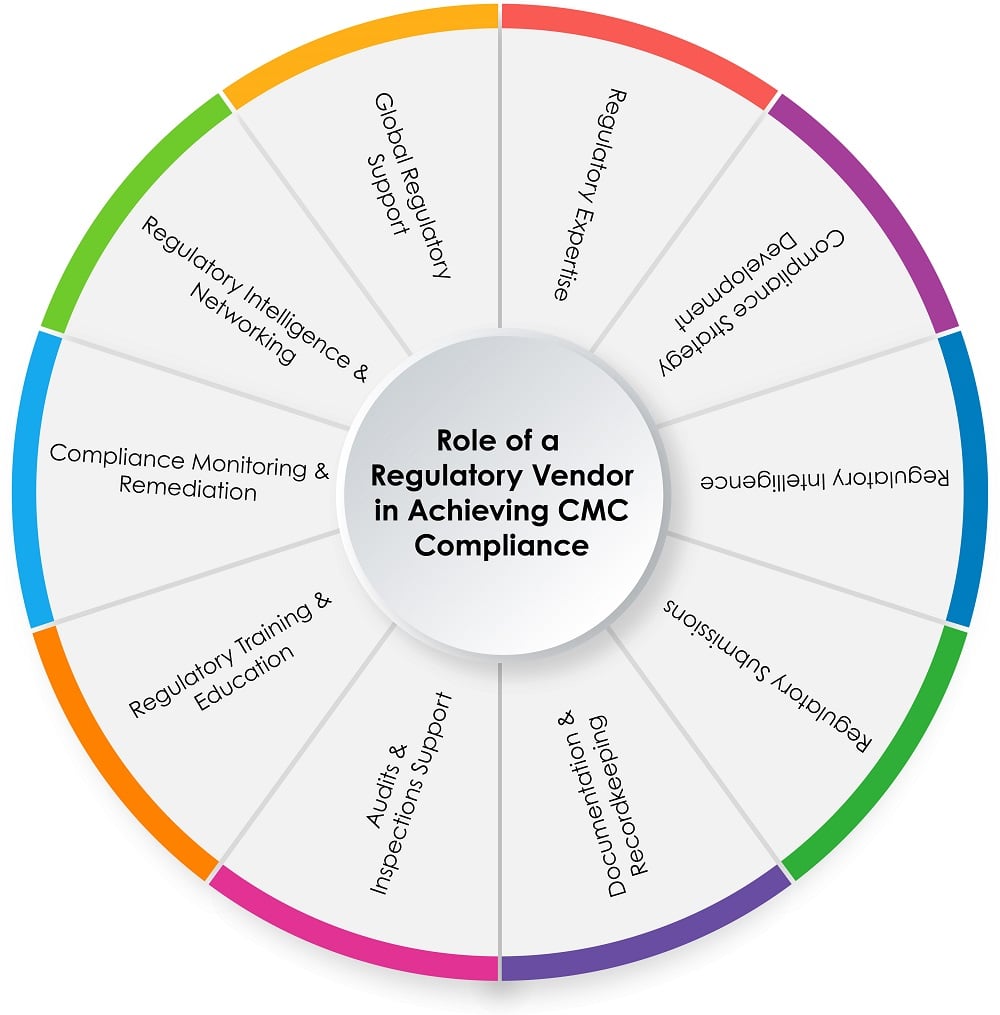
Le graphique circulaire ci-dessous (Figure 1) montre le rôle d'un fournisseur réglementaire dans le processus de conformité CMC :
Figure 1 : Rôle d'un fournisseur réglementaire dans l'atteinte de la conformité CMC
Conclusion
L'atteinte et le maintien de la conformité aux exigences CMC nécessitent une approche stratégique, qui implique une collaboration interfonctionnelle, des systèmes qualité robustes et une veille réglementaire (RI) continue. C'est également essentiel pour un accès réussi au marché et la disponibilité continue des produits. Une compréhension approfondie des fondamentaux de la RA CMC et la mise en œuvre de stratégies de conformité efficaces peuvent aider les entreprises pharmaceutiques à naviguer dans le paysage réglementaire, à obtenir les approbations et à maintenir les normes les plus élevées de qualité et de sécurité des patients. Des partenariats réglementaires stratégiques peuvent optimiser ces étapes cruciales en offrant une expertise de pointe pour rester conforme. Contactez-nous pour en savoir plus sur nos services !









