
En plus de compléter les soumissions de données xEVMPD requises, les organisations des sciences de la vie devront désormais utiliser un formulaire de demande basé sur le web appelé Digital Application Dataset Integration (DADI). L'Agence Européenne des Médicaments (EMA) a conçu DADI comme un remplacement à long terme du formulaire de demande électronique basé sur PDF (eAF), qui a été créé pour prendre en charge les soumissions eCTD.
Les délais pour cette transition ont été récemment publiés par l'EMA. DADI remplacera le formulaire pour les variations de Produits médicaux en 2022. D'autres formulaires de soumission pour les produits autorisés au niveau central (CAP) et les produits autorisés au niveau national (NAP) suivront bientôt d'ici 2023. Le projet remplacera également les formulaires utilisés pour les procédures clés de l'UE, y compris la procédure centralisée (CP), la procédure de reconnaissance mutuelle (MRP), la procédure décentralisée (DCP) et la procédure nationale (NP).
Les formulaires web (y compris le formulaire de variations humaines (HVF) pour les Produits médicaux destinés aux humains) uniformiseront les entrées pour les eAF afin de fournir des données de base standard pour les Produits médicaux. Ils permettront à la fois la sortie existante lisible par l'homme et la nouvelle sortie lisible par machine pour le traitement numérique, basée sur la norme d'échange de données Fast Healthcare Interoperability Resources (FHIR) pour les Produits médicaux. Ils utiliseront également les données de base existantes des services de gestion des produits (PMS) pour préremplir les champs du formulaire, le cas échéant.
Les formulaires web DADI visent à permettre un traitement plus méthodique des demandes, réduisant ainsi la charge de travail de l'organisation. Par exemple, les erreurs et les incohérences seront réduites grâce au soutien des formulaires pour l'examen minutieux des demandes soumises par les autorités sanitaires. Ces formulaires ouvriront également la voie à des données « justes du premier coup » alimentées dans les bases de données, rendant ainsi l'intégration des systèmes et le partage des données entre les autorités sanitaires plus fluides. De plus, les nouveaux formulaires remplaceront la technologie archaïque.
Avantages de DADI
L'objectif de DADI et de cette transformation axée sur les données des processus réglementaires peut se résumer comme suit :
- Pour améliorer l'efficacité dans les fonctions réglementaires, de R&D et de fabrication
- Pour communiquer plus rapidement avec les autorités sanitaires.
- Pour permettre une prise de décision basée sur les données pour les entreprises et les autorités
- Pour avoir de meilleurs aperçus et une meilleure anticipation des résultats commerciaux et de la performance globale
Globalement, cela vise à être bénéfique pour les patients, les régulateurs, ainsi que l'industrie.
Derniers changements de calendrier par l'EMA
- La date d'entrée en vigueur des HVF a été repoussée à octobre 2022, par rapport au calendrier initialement prévu d'avril 2022.
- Actuellement, le HVF est soumis à des tests d'acceptation utilisateur (UAT) fermés par un groupe d'experts en la matière sur DADI.
- Par la suite, une UAT intégrée aura lieu avec un groupe plus large de diverses parties prenantes au deuxième trimestre de 2022.
- Une fois mis en ligne, il y aura une phase de transition de six (06) mois durant laquelle les eAF (ancienne version PDF) et les formulaires web seront acceptés en parallèle. Après cette période, seul le HVF sera accepté.
Veuillez vous référer à l'infographie suivante pour prendre connaissance des délais de mise en œuvre du HVF (Mise à jour en février 2022, sous réserve de modifications par l'EMA) :
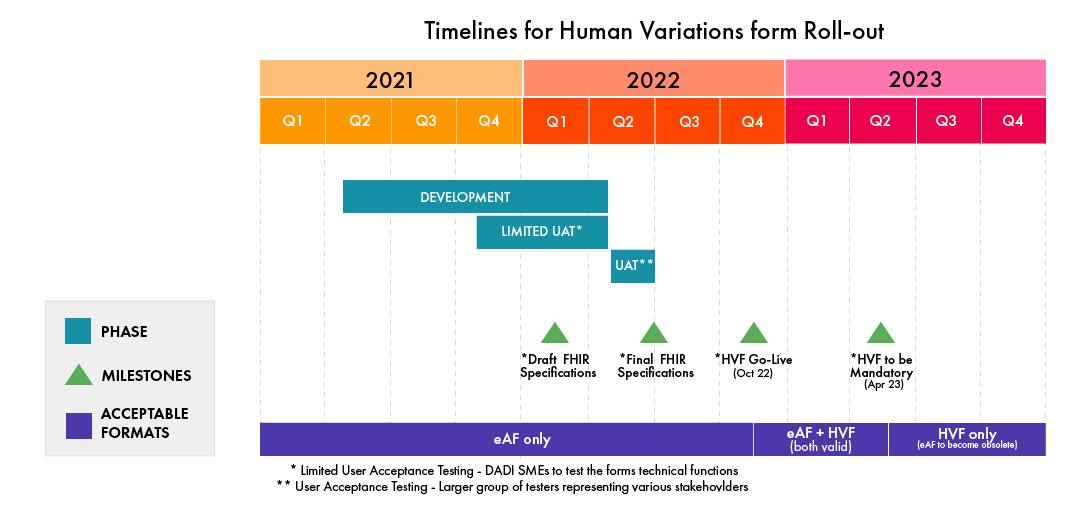
(source : EMA)
Assurer l'adaptabilité à l'environnement réglementaire dynamique.
Toutes les principales Autorités de Santé s'orientent désormais vers la soumission de jeux de données et de documents de haute qualité. Il est important pour les organisations de maintenir ces éléments dans un système unifié.
Il est également essentiel d'avoir une compréhension claire du cycle de vie complet de la soumission – ses exigences, les personnes et les processus qui y sont associés, ainsi que l'emplacement actuel des données sources, grâce à une évaluation approfondie des besoins. Le nettoyage et l'enrichissement des données doivent être traités en priorité si l'évaluation révèle un besoin.
Il est impératif de disposer d'un système de gestion de l'information réglementaire (RIMS) en place qui s'adapte aux réglementations et lignes directrices en constante évolution, et qui est également flexible pour remodeler les besoins actuels de l'organisation et se conforme à l'environnement réglementaire dynamique. Pour en savoir plus sur la suite de solutions réglementaires de Freyr, qui préparera votre organisation à DADI et à d'autres modifications de processus similaires, visitez-nous sur Freyr Digital.









