
Le 9 février 2022, l'Agence européenne des médicaments (EMA) a commencé la mise en place d'un Centre de coordination pour l'analyse des données et le réseau d'intégration en conditions réelles (DARWIN EU®). C'est la première étape vers l'intégration des preuves du monde réel (RWE) dans l'évaluation des médicaments à travers l'Union européenne (UE). Assurer la sécurité et l'efficacité des médicaments est l'activité principale de toute agence de réglementation, et le RWE s'avère être une source fiable pour recueillir des preuves en temps réel à partir des bases de données mondiales de soins de santé. Par conséquent, cette initiative de l'EMA vise à améliorer la qualité des médicaments dans la région de l'UE et à les rendre disponibles plus rapidement.
Activités majeures prévues pour le Centre de coordination de DARWIN EU®
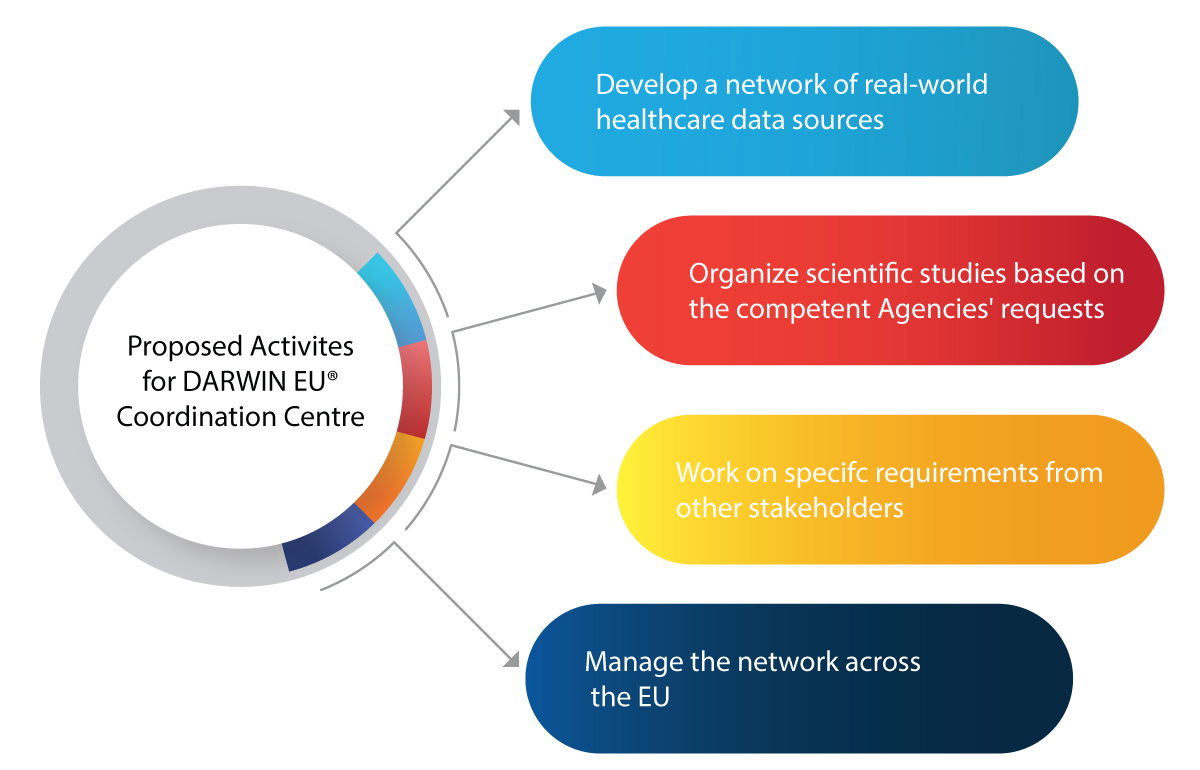
Comment le DARWIN EU® va-t-il aider l'EMA et les autorités compétentes dans le domaine de la réglementation ?
Des médicaments innovants, facilement accessibles aux patients, sont une nécessité urgente. Les processus réglementaires de développement, d'approbation, de commercialisation et de surveillance post-commercialisation prennent un temps considérable, ce qui rend la demande de nouveaux médicaments insatisfaite. Réduire le délai de mise sur le marché tout en garantissant la sécurité, l'efficacité et la qualité des médicaments innovants est la voie à suivre. Plusieurs autorités sanitaires mondiales reconnaissent les avantages d'intégrer les RWE dans leurs approbations réglementaires, et DARWIN EU® est l'initiative de l'EMA.
L'EMA prévoit de connecter le réseau européen de réglementation des médicaments à l'Espace européen des données de santé (EHDS) afin d'améliorer l'échange de données et l'accès à divers types de données de santé dans le cadre de ce programme. Elle établira également des normes pour les évaluations scientifiques et la prise de décision réglementaire.
Voici quelques activités que DARWIN EU® vise à réaliser :
- Utilisation des RWE dans les activités de prise de décision pour la réglementation des nouveaux médicaments, vaccins, etc.
- Intégrer les données du monde réel (RWE) dans l'ensemble du cycle de vie d'un médicament, tels que le développement, l'autorisation et la surveillance post-commercialisation
- Se préparer à toute future urgence médicale, telle que les pandémies
- Bénéficier à l'industrie pharmaceutique avec des données probantes du monde réel (RWE) pertinentes et fiables concernant les patients, les maladies et l'utilisation des médicaments.
- Prendre des décisions réglementaires éclairées basées sur les RWE pour l'utilisation sûre et efficace des médicaments
- Accessibilité améliorée des médicaments vitaux aux patients dans le besoin grâce à une analyse de données précise et opportune
Calendrier proposé pour que DARWIN EU® devienne un réseau pleinement fonctionnel dans l'UE
L'EMA précise également les délais pour que DARWIN EU® soit pleinement opérationnel, et ils se présentent comme suit :
- 2021 – Lancement du projet
- 2022 – Établissement de DARWIN EU®
- 2023 – Développement de DARWIN EU® et définition de ses usages
- 2024 – Rendre DARWIN EU® pleinement opérationnel
- 2025 – Améliorer les utilisations réglementaires des données de santé en élargissant les portées en termes de médicaments, de géographie, etc.
L'EMA collabore avec le Centre médical universitaire Erasmus de Rotterdam pour la mise en place de DARWIN EU®. L'objectif de ce partenariat est la création du Centre de coordination pour établir un réseau de données distribué. Ils ont également entrepris les tâches de mener des études scientifiques, de soutenir les processus de prise de décision réglementaire et de gérer un catalogue de sources de données du monde réel.
Que signifie le lancement de DARWIN EU® pour l'avenir ?
L'EMA et les Chefs des Agences des Médicaments (HMA) ont toujours collaboré pour identifier les défis, fixer des objectifs limités dans le temps et définir les priorités dans leurs documents de stratégie quinquennale (05 ans). Il vise à donner une orientation stratégique aux activités menées par le réseau réglementaire européen des médicaments.
L'initiation de DARWIN EU® est une étape majeure vers la mise en œuvre de la stratégie de réseau de l'EMA. Mener des études scientifiques pour répondre à des questions de recherche, soutenir l'évaluation des médicaments dans l'UE et maintenir les Metadata pour les activités réglementaires des médicaments sont les principaux objectifs. DARWIN EU® est envisagé comme un acteur majeur de la réglementation des médicaments en Europe, et les études pilotes devraient être prêtes d'ici la fin de 2022.
Si vous êtes un fabricant de médicaments et souhaitez en savoir plus sur les RWE et la manière dont ils façonnent l'avenir de la prise de décision réglementaire, contactez les experts en affaires réglementaires de Freyr.









