
L'Administration des produits thérapeutiques (TGA) en Australie a des règles strictes pour l'enregistrement de nouveaux médicaments sur ordonnance contenant de nouveaux principes actifs. Récemment, la TGA a élaboré un processus révisé pour améliorer l'efficacité des médicaments vitaux sur ordonnance et les rendre plus rapidement accessibles aux patients. Ces changements sont pertinents pour les demandes qui doivent être étayées par des données non cliniques, cliniques et/ou de bioéquivalence (catégorie 1 et catégorie 2). La TGA a publié un document en août détaillant les exigences réglementaires y afférentes.
Caractéristiques importantes du nouveau processus d'enregistrement des médicaments sur ordonnance
- La TGA a élaboré un processus d'enregistrement par phases et a désigné les étapes comme des jalons. Chacune d'elles suit une voie distincte.
- Le nouveau processus vise à améliorer la qualité des dossiers. Les dossiers sont préparés selon un format de document technique commun (CTD) et respectent toutes les exigences réglementaires.
- La phase de planification de la pré-soumission est importante car les demandeurs déposent les détails de la demande prospective. Ceci est fait au moins deux mois et quart (02 ¼) avant la soumission du dossier complet. Cette étape vise à aider la TGA à établir les dates des jalons ultérieurs et à préparer les ressources pour gérer le CTD.
- La prochaine phase est la soumission. Une fois celle-ci effectuée, la TGA ne permet pas au demandeur de fournir des données ou informations supplémentaires après la date de soumission. Il est obligatoire de soumettre un dossier complet, correct et de haute qualité.
- En vertu de l'article 31 de la loi de 1989 sur les produits thérapeutiques, la TGA demande des informations supplémentaires au stade de l'évaluation. Après l'évaluation initiale, toutes les demandes sont regroupées et envoyées au demandeur.
Pour comprendre les étapes clés du processus renouvelé, veuillez vous référer aux organigrammes suivants.
Jalon 1
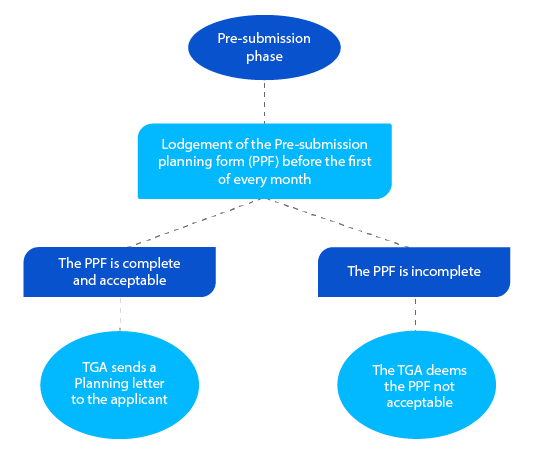
La lettre de planification contient la date prévue à laquelle la TGA s'attend au dépôt du dossier et d'autres dates clés cibles pour la demande de médicament sur ordonnance.
Jalon 2
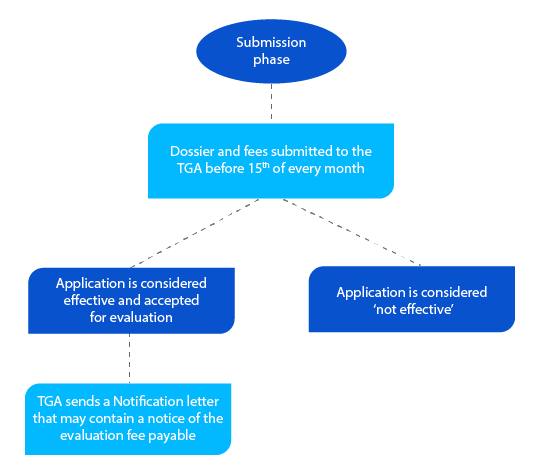
Le dossier contient des informations qui aident la TGA à évaluer la demande, et si tout est acceptable, une lettre de notification est envoyée avant la fin du mois au cours duquel le demandeur a soumis le dossier.
Jalon 3
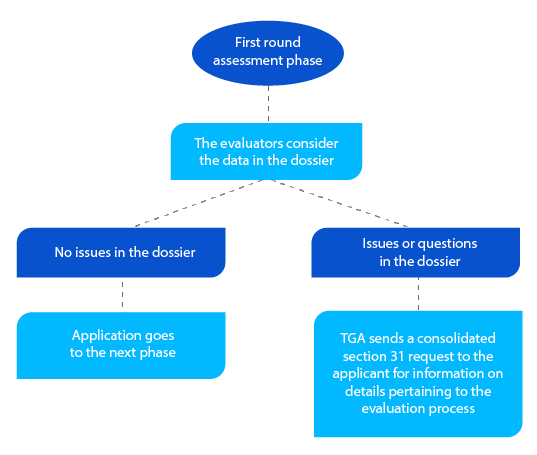
En plus de la section 31 consolidée, demandée le cas échéant, la TGA envoie des copies des rapports d'évaluation préparés par les évaluateurs de la qualité, des études non cliniques, des études cliniques et des plans de gestion des risques (PGR).
Jalon 4
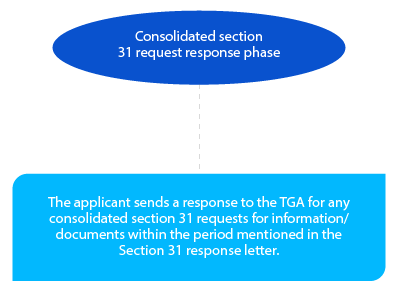
Le demandeur peut proposer le délai de réponse de la section 31. Il peut être de trente (30) ou soixante (60) jours et doit être mis en évidence dans le PPF. Cette période doit être confirmée par la TGA dans la lettre de planification. Le format acceptable de la réponse est le CTD, et celle-ci doit être envoyée sous forme de copies papier et électroniques.
Puisqu'il s'agit de la dernière occasion pour le demandeur de fournir toute information manquante à la TGA, cela doit être fait de manière conforme.
Jalon 5
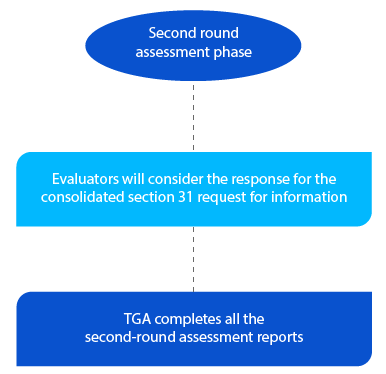
La TGA dispose de deux (02) mois pour les demandes de nouveaux médicaments génériques concernant la deuxième série de rapports d'évaluation et d'un (01) mois pour tous les autres types de demandes. Les rapports sont envoyés aux demandeurs respectifs après l'achèvement de la deuxième évaluation.
Jalon 6
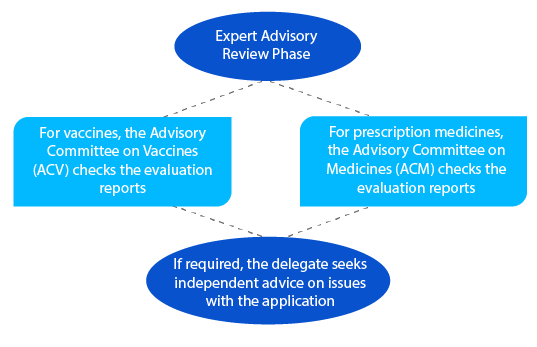
Après l'examen consultatif, la TGA envoie une notification avec les détails de l'avis qu'elle reçoit de l'ACV ou de l'ACM.
Jalon 7
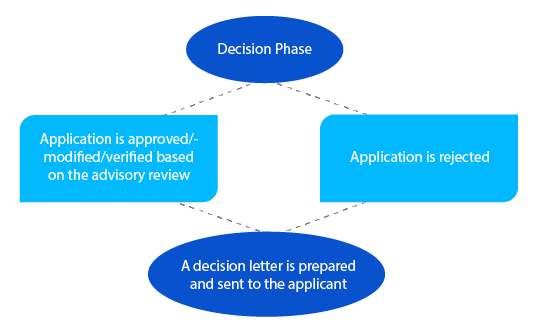
En cas de problèmes en suspens, le délégué peut prendre contact avec le demandeur à ce stade avant de prendre une décision. Pour les demandes relevant de la section 23 de la loi de 1989 sur les produits thérapeutiques (médicaments inscrits nouvellement évalués dans le Registre australien des produits thérapeutiques (ARTG)), une notification est envoyée au demandeur dans les vingt-huit (28) jours suivant la prise de décision.
Jalon 8
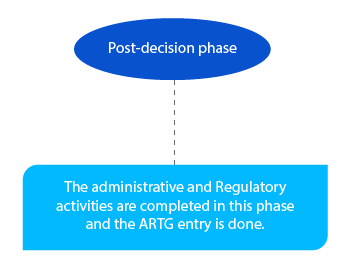
Les paiements en suspens sont traités à ce stade. Et cela doit être finalisé avant la fin du mois suivant la décision du délégué.
La TGA prenant toutes les précautions pour assurer la sécurité, l'efficacité et la qualité des médicaments sur ordonnance tout en réduisant leur délai de mise sur le marché, il incombe au demandeur de faire les soumissions pertinentes pour un processus d'enregistrement fluide. À n'importe quelle étape, collaborer avec un fournisseur de services réglementaires End-to-End expert en enregistrement de médicaments sur ordonnance est la situation idéale. Contactez une entité réglementaire expérimentée pour une voie conforme ; restez informé et restez conforme.










