
Les essais en aveugle constituent la pierre angulaire de l'intégrité des essais cliniques, car ils éliminent les biais et garantissent une évaluation objective des produits à l'étude. Cependant, derrière cette rigueur scientifique se cache un élément créatif essentiel : les étiquettes des emballages destinés aux essais cliniques. Pour artwork réglementaire, la conception pour les essais en aveugle est un exercice d'équilibre entre conformité, confidentialité et clarté.
Chez Freyr Solutions, nous sommes spécialisés dans artwork conforme à la réglementation et prête pour l'audit, artwork essais cliniques internationaux. Dans cet article, nous examinons comment artwork des emballages destinés aux essais cliniques artwork être adaptée pour répondre aux exigences spécifiques des études en aveugle.
Pourquoi Artwork dans les études en aveugle
La conception d'étiquettes d'emballage pour les études en aveugle (généralement dans le cadre d'essais cliniques) implique des processus spécifiques visant à préserver l'aveugle et à garantir le respect des exigences réglementaires et des spécificités de l'essai.
Contrairement aux produits commerciaux, les artwork études en aveugle doivent dissimuler l'identité du produit, tout en fournissant des informations claires et conformes à la réglementation aux utilisateurs finaux, tels que les investigateurs, les pharmaciens et les patients. Toute divergence — qu'elle concerne la couleur, la forme, la typographie ou le contenu de l'étiquetage — peut involontairement lever l'aveugle de l'étude.
Artwork des études Artwork aveugle doivent donc comporter des objectifs clés :
- Garantir l'intégrité de l'aveugle: l'étiquette ne doit comporter aucune information susceptible de révéler l'identité du traitement. La cohérence visuelle doit être préservée dans tous les groupes de l'étude.
- Facilité d'utilisation: garantir une utilisation sûre et correcte (par exemple, une mise en œuvre adéquate par le personnel sur place). Éviter toute différenciation du produit par le biais d'éléments de conception.
- Gérer les données variables : les éléments de données variables essentiels — tels que les codes de randomisation, les dates d'expiration, les numéros de kit, les identifiants des patients et les informations spécifiques à chaque visite — doivent être disponibles.
- Conformité réglementaire: respecter les réglementations mondiales et régionales en matière d'essais cliniques
- Traçabilité : garantir un lien clair avec l'essai clinique et le patient sans révéler le type de produit. Le système doit être soumis à un contrôle de version et permettre la vérifiabilité.
Procédure de création d'étiquettes d'emballage pour les essais cliniques en aveugle
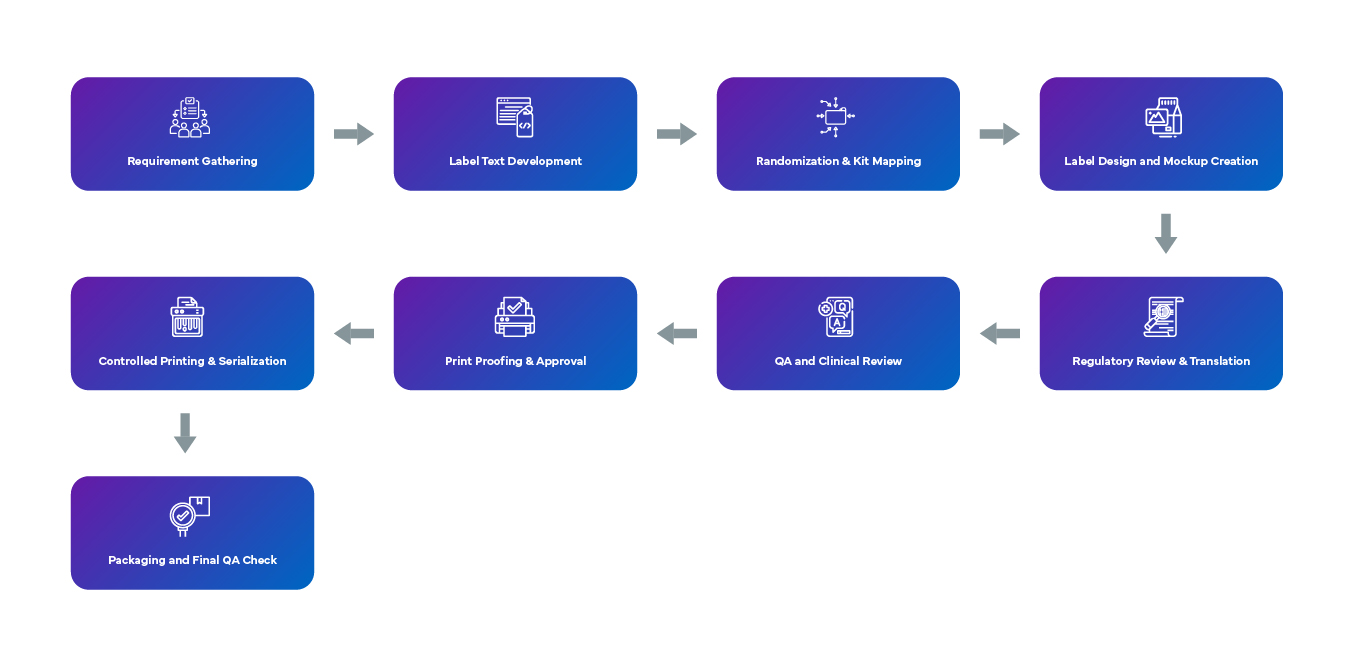
Le processus de conception de l'étiquetage en aveugle commence par la collecte des exigences via l'examen du protocole et les contributions des parties prenantes, afin de garantir la conformité avec les réglementations spécifiques à chaque pays. Le texte neutre des étiquettes est rédigé à l'aide de termes tels que « Médicament de l'étude » et comprend des informations essentielles telles que les numéros d'essai, les dates de péremption et les mises en garde, tout en évitant les identifiants susceptibles de révéler le traitement. La randomisation et le mappage des kits sont gérés de manière sécurisée, les étiquettes étant conçues pour préserver l'aveuglement, souvent à l'aide de codes-barres. Des maquettes de conception sont créées en tenant compte de la taille des contenants, des besoins multilingues et des exigences en matière de superposition. Les examens réglementaires et de traduction garantissent la conformité mondiale. Les équipes QA cliniques vérifient la conformité au protocole, tandis que les épreuves d'étiquettes font l'objet de contrôles électroniques et d'approbations formelles. La stratégie d'application des étiquettes — qu'il s'agisse d'étiquetage primaire, secondaire ou superposé — tient compte des contraintes environnementales. L'impression contrôlée, souvent en flux tendu, garantit la traçabilité sérialisée et l'emballage final est réalisé sous QA afin de confirmer l'exactitude de l'étiquette, son adhérence et l'intégrité de l'aveuglement.
Artwork clés Artwork pour Artwork des étiquettes dans le cadre d'études en aveugle
| Artwork | Exigences relatives à la conception des études en aveugle | Artwork de Freyr |
| Palette de couleurs | Évite toute distinction par couleur qui pourrait indiquer les groupes de traitement | Des palettes de couleurs uniformes pour toutes les branches ; les nuances de gris ou les tons neutres sont privilégiés |
| Polices et typographie | Une police et une taille de caractères uniformes pour toutes les variantes afin d'éviter tout indice visible | Les directives typographiques prédéfinies sont appliquées de manière uniforme à l'ensemble des maquettes d'étiquettes |
| Mise en page et hiérarchie des étiquettes | Positionnement du texte et des éléments graphiques conformément aux directives techniques | Mises en page basées sur des modèles pour garantir l'uniformité |
| Étiquetage « placebo » vs « actif » | Il ne doit présenter aucune différence visuelle | Utilisez des modèles d'étiquettes identiques ; seuls les champs variables diffèrent en fonction des données encodées. |
| Codes de randomisation/suivi | Doit être présent mais ne doit pas être interprétable par l'utilisateur final | Possibilité de générer n'importe quel code-barres. |
| Gestion linguistique | Le contenu multilingue ne doit pas entraîner de biais de mise en page | Les blocs de texte sont conçus selon une disposition symétrique. |
| Champs de données dynamiques | Les données telles que le numéro de lot, la date de péremption et l'identifiant du composant varient d'un emballage à l'autre | Champs réservés ou emplacements convenus par le service d'emballage |
| Matériau et format de l'étiquette | Il faut permettre la mise en aveugle et la levée de l'aveugle en fonction des besoins de l'étude | Utilisation d'étiquettes en livret, d'étiquettes autocollantes ou d'étiquettes de recouvrement, selon les besoins |
| Contrôle des versions et validation | Les étiquettes sont fréquemment mises à jour en raison des modifications apportées aux protocoles | artwork centralisée artwork avec contrôle des versions des étiquettes et gestion des validations |
Références des autorités réglementaires concernant l'étiquetage des essais cliniques
Région | Organisme de réglementation. | Référence de la directive |
| UE | EMA | Annexe VI du règlement (UE) n° 536/2014 |
| US | FDA | 21 CFR, partie 312.6 |
| Royaume-Uni | MHRA | Guide des bonnes pratiques cliniques |
| Canada | Santé Canada | Document d'orientation à l'intention des promoteurs d'essais cliniques |
Erreurs courantes dans Artwork des études en aveugle Artwork et comment les éviter)
✗ Utilisation d'étiquettes de dimensions différentes pour l'
du groupe actif et du groupe placebo ✓ Uniformisation de la taille et de la forme pour tous les groupes
✗ L'emplacement des langues varie d'un pays à l'autre
✓ Utilisez des blocs de texte en miroir avec une mise en forme cohérente
✗ Numéros de lot/de produit visibles sur artwork des produits
✓ Utiliser des données codées et des codes-barres pour masquer les identifiants visibles
Pourquoi faire appel à Freyr pour Artwork d'études en aveugle ?
- Expertise en conception d'étiquettes en aveugle pour les essais cliniques internationaux
- Disponibilité des informations réglementaires aux US, dans l'Union européenne, au Royaume-Uni, au Canada et dans la région Asie-Pacifique
- Utilisation d'un outil Artwork , si nécessaire. Cet outil peut être personnalisé pour répondre aux exigences des essais cliniques.
- Fichiers soumis à un contrôle de version, conformes et prêts pour un audit
- Prise en charge multilingue et relecture technique d'étiquettes pour n'importe quel pays ou région










