
Le besoin médical non satisfait (UMN) est l'une des priorités les plus urgentes des systèmes de santé. L'évolution constante de la science et de la technologie dans le domaine de la santé a permis d'explorer diverses options thérapeutiques. Les autorités sanitaires encouragent les thérapies innovantes qui promettent des avantages significatifs pour la qualité de vie des patients. S'appuyant sur la priorité donnée à l'innovation et à la satisfaction des besoins non couverts des patients pour le développement de médicaments, l'Agence européenne des médicaments (EMA) a introduit le programme PRIority MEdicines (PRIME) en 2016. Depuis lors, le programme PRIME est une méthode permettant d'accorder des approbations pour des thérapies innovantes selon un calendrier accéléré. Ce type de voie facilitée peut être exploré par toute entreprise, des start-ups aux biotechnologies de taille moyenne en passant par les grandes organisations multinationales. Cependant, la qualification pour ce programme est limitée aux produits en développement et n'ayant pas encore demandé d'autorisation de mise sur le marché via la procédure centralisée. Les critères de qualification sont appliqués rigoureusement. Entre mars 2016 et avril 2022, seulement 24 % des demandes ont reçu l'approbation, tandis que 72 % des demandes PRIME ont été rejetées. Parmi les 24 % sélectionnés pour le programme PRIME, la majorité appartenait au domaine thérapeutique de l'oncologie.
Les innovateurs qui recherchent des autorisations de mise sur le marché pour des maladies rares ou des médicaments orphelins peuvent souvent disposer de jeux de données limités comme preuves pour étayer leurs demandes de nouveaux médicaments, comme l'exigent les régulateurs. Les demandes de produits médicaux de thérapie innovante (ATMPs) et de médicaments orphelins sont généralement confrontées à de tels défis. En raison des données limitées sur la population de patients, une interaction constante avec les régulateurs est encouragée afin d'obtenir de meilleures informations pour l'examen scientifique et les exigences d'approbation. La voie PRIME peut être utile pour de telles thérapies grâce à l'implication précoce des régulateurs qui fournissent un soutien proactif et des conseils pour la collecte de données et l'évaluation bénéfice-risque.
Avantages de la voie PRIME
- Aide les innovateurs à élaborer un plan de développement bien rédigé.
- Bénéficie aux innovateurs en impliquant les Autorités de Santé dès le début du développement, ce qui contribue à la rédaction de demandes d'autorisation de mise sur le marché de haute qualité.
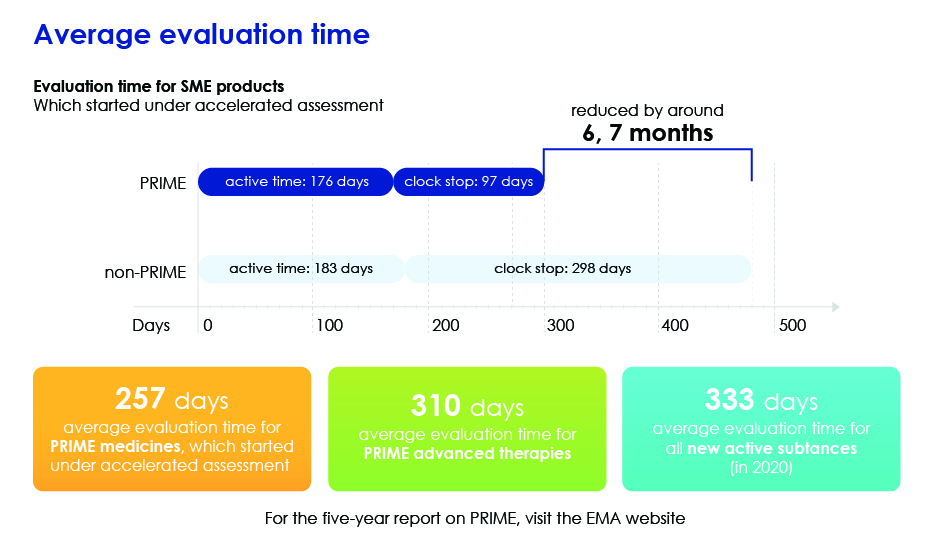
- Accélère l'évaluation globale en réduisant le temps d'évaluation moyen afin que les médicaments puissent atteindre les patients plus rapidement.
- Soutient les innovateurs à concentrer leur attention sur le développement de médicaments pour améliorer les résultats pour les patients et répondre aux besoins non satisfaits des patients.
Détail du temps d'évaluation.
Demandes pour la voie PRIME
La procédure PRIME priorise les besoins médicaux non satisfaits. Sur les 384 demandes PRIME reçues depuis mars 2016, seules 18 ont abouti à une autorisation de mise sur le marché en juin 2021.

Êtes-vous prêt(e) pour PRIME ?
L'existence de la voie PRIME est due à des besoins médicaux non satisfaits importants et à l'accent mis sur la réduction des lacunes par le Réseau Réglementaire Européen des Médicaments (EMRN). Pour évaluer l'adéquation d'un produit à la voie PRIME, il faut prendre en compte les éléments suivants :
- Constatations : Les demandeurs doivent exposer le besoin médical non satisfait et fournir un argument convaincant sur la manière dont leur produit résoudra le problème.
- Potentiel : Les demandeurs doivent démontrer le potentiel bénéfique de la thérapie au regard des critères de besoin médical non satisfait.
- Données précliniques : Les demandeurs doivent présenter des données sur l'efficacité ou la performance de la thérapie dans le système biologique humain. Les modèles non cliniques, aussi précis soient-ils, ne fournissent pas un aperçu exact de son comportement dans le système biologique humain.
- Stade de développement : Le demandeur doit identifier le bon stade pour s'engager dans la voie PRIME afin d'obtenir des conseils optimaux de la part des régulateurs et de poursuivre la procédure de demande.
Après l'octroi PRIME
Une fois qu'un demandeur a obtenu la possibilité d'emprunter la voie facilitée, l'EMA :
- Désigner un rapporteur du Comité des Produits médicaux à Usage Humain (CHMP) ou du Comité des thérapies avancées (CAT) dans le cas des thérapies avancées.
- Organiser une réunion de lancement avec le rapporteur du CHMP/CAT et un groupe multidisciplinaire d'experts afin de fournir des orientations sur le plan de développement global et la stratégie réglementaire.
- Désigner un point de contact unique pour le demandeur.
- Fournir des conseils scientifiques à chaque étape clé du développement, impliquant un ensemble supplémentaire de parties prenantes telles que les organismes d'évaluation des technologies de la santé, afin d'accélérer l'accès des patients au nouveau médicament.
- Confirmer la possibilité d'une évaluation accélérée lors du dépôt d'une demande, tout en tenant compte de l'autorisation de mise sur le marché.
Votre demande pour la voie des médicaments prioritaires (PRIME-ready) est-elle prête ? Contactez Freyr dès aujourd'hui pour une évaluation. Découvrez comment nous pouvons vous aider avec votre stratégie réglementaire et la désignation au programme PRIME. Restez informé. Restez conforme.









