
Les innovations en matière de combinaisons médicament-dispositif ont conduit à des avancées significatives dans les soins aux patients. Les produits médicamenteux associés à des dispositifs médicaux permettent une administration ciblée des médicaments, des résultats thérapeutiques améliorés et une meilleure observance des patients. Cependant, naviguer dans le paysage réglementaire des combinaisons médicament-dispositif peut être complexe.
Ce blog explorera les considérations et les défis associés aux opérations réglementaires pour les produits combinés médicament-dispositif, offrant des perspectives pour la rationalisation des processus.
Aperçu et cadre réglementaire des combinaisons médicament-dispositif
Les produits de combinaison médicament-dispositif médical associent les effets thérapeutiques des médicaments pharmaceutiques aux capacités de délivrance des dispositifs médicaux. Ces combinaisons incluent les stents à élution médicamenteuse, les inhalateurs et dispositifs respiratoires, les patchs transdermiques, les systèmes d'administration d'insuline, les systèmes de perfusion médicamenteuse et les ballons recouverts de médicaments. L'administration ciblée, l'efficacité accrue, l'amélioration de l'observance du patient et un contrôle précis du traitement sont quelques-uns des attributs notables de ces produits.
Les autorités de réglementation telles que la Food and Drug Administration (FDAUS , l'Agence européenne des médicaments (EMA) et d'autres ont établi des lignes directrices relatives aux combinaisons de médicaments et de dispositifs médicaux. Ces dernières années ont été marquées par des évolutions notables dans le paysage réglementaire, avec une attention accrue portée à l'harmonisation, aux évaluations fondées sur les risques et à la surveillance post-commercialisation.
Considérations clés pour les opérations réglementaires
Lors de la gestion des opérations réglementaires pour les combinaisons médicament-dispositif, voici quelques-unes des considérations à prendre en compte :
Comprendre la classification des produits et les parcours réglementaires
Comprendre la classification des produits combinés médicament-dispositif et choisir la voie réglementaire appropriée est crucial. Les fabricants doivent déterminer s'il s'agit d'une combinaison médicament-dispositif, d'un dispositif revêtu de médicament ou d'un produit co-conditionné. Le choix de la bonne voie pour le type de produit spécifique est essentiel pour un accès réussi au marché.
Répondre aux exigences scientifiques et techniques.
Cela inclut d'assurer la compatibilité entre les composants du médicament et du dispositif, de réaliser des études de stabilité pour évaluer la durée de conservation du produit, de valider les processus de fabrication et de mettre en œuvre des évaluations des risques pour identifier et atténuer les dangers potentiels.
Soins aux patients et tests d'utilisabilité
Les soins aux patients et l'ingénierie de l'utilisabilité jouent un rôle important dans le développement de ces produits combinés. Prendre en compte des facteurs tels que l'interface utilisateur, l'ergonomie, la manipulation du dispositif et l'observance du patient pendant le développement du produit contribue à garantir leur utilisation sûre et efficace par les patients et les professionnels de la santé avec un minimum d'erreurs.
Considérations après commercialisation
Les obligations post-commercialisation sont un aspect essentiel de la conformité réglementaire pour les combinaisons médicament-dispositif. Les fabricants doivent établir des processus pour la déclaration des événements indésirables, la surveillance après commercialisation et la déclaration de vigilance afin de surveiller la sécurité et la performance de leurs produits.
Se tenir informé des récentes directives et mises à jour réglementaires
Il est essentiel de se tenir informé des dernières directives et mises à jour afin de garantir la conformité et d'aligner les stratégies réglementaires sur les attentes actuelles. Le paysage réglementaire applicable aux combinaisons de médicaments et de dispositifs médicaux est en constante évolution. Se conformer aux directives FDA, du règlement européen sur les dispositifs médicaux (MDR) et du Conseil international d'harmonisation des exigences techniques pour les produits pharmaceutiques à usage humain (ICH) peut aider les fabricants à rester en conformité.
Meilleures pratiques pour l'optimisation des opérations réglementaires
Pour optimiser les opérations réglementaires pour les combinaisons médicament-dispositif, les entreprises pharmaceutiques peuvent suivre les meilleures pratiques illustrées dans le graphique circulaire ci-dessous :
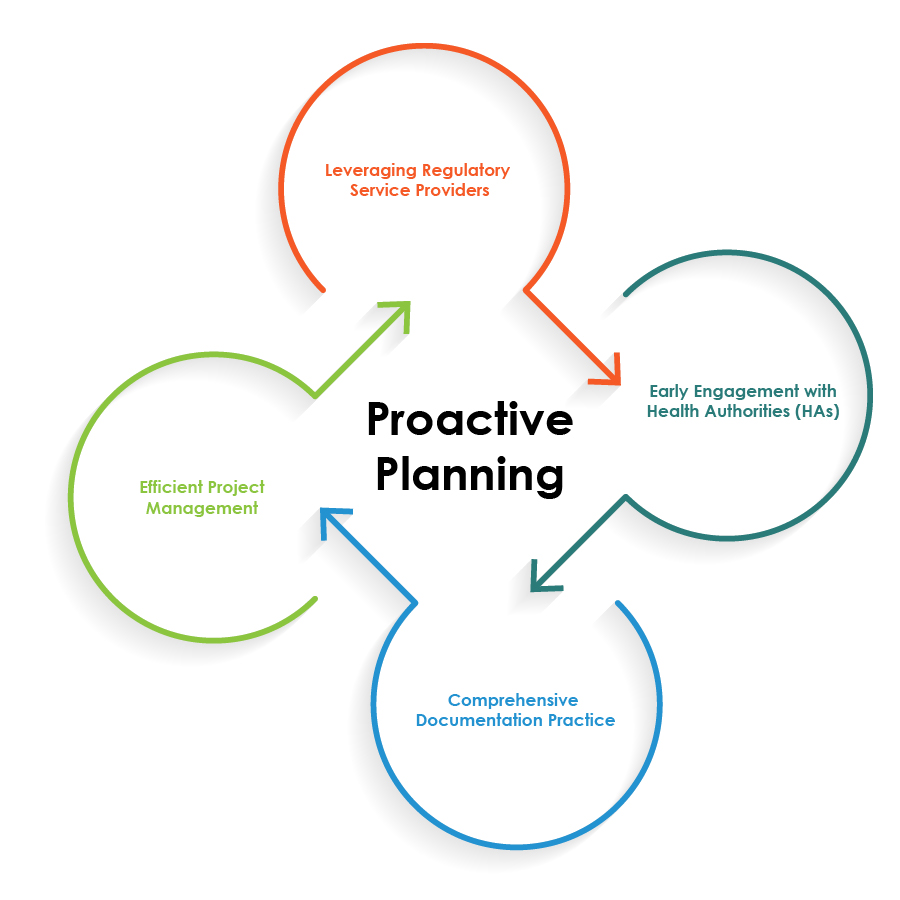
Une planification proactive est la pierre angulaire pour des opérations réglementaires fluides concernant les combinaisons médicament-dispositif.
Tendances futures et défis
Il est crucial de surveiller les tendances futures et les lacunes pour les entreprises pharmaceutiques et les professionnels de la réglementation impliqués dans les opérations réglementaires de ces produits. Voici quelques tendances et défis à surveiller :
- Technologies émergentes : La nanotechnologie, l'impression 3D et les applications connexes influencent le développement de combinaisons innovantes de médicaments et de dispositifs. Ces tendances technologiques offrent une administration ciblée de médicaments, une médecine personnalisée et une surveillance améliorée des patients. Cependant, elles présentent également des défis réglementaires uniques liés à la sécurité, à l'efficacité et au contrôle qualité.
- Cybersécurité : Avec la connectivité croissante des dispositifs médicaux, assurer la sécurité des données et se protéger contre les cybermenaces devient primordial. L'intégration de mesures de cybersécurité robustes et la mise à jour des meilleures pratiques en matière de sécurité des dispositifs sont des considérations essentielles pour les opérations réglementaires.
- Défis divers : Ceux-ci incluent les complexités de la chaîne d'approvisionnement mondiale, telles que l'approvisionnement en matières premières, la disponibilité des composants et les processus de fabrication, qui posent des défis pour maintenir la conformité réglementaire et garantir la qualité des produits. Des pratiques robustes de gestion de la chaîne d'approvisionnement, des évaluations des risques et une surveillance des fournisseurs sont essentielles pour relever ces défis et atténuer les risques associés.
Naviguer dans le paysage réglementaire des produits combinés médicament-dispositif exige une compréhension approfondie du cadre réglementaire, des directives récentes et des meilleures pratiques. Prendre en compte les considérations clés, se tenir informé des changements et mettre en œuvre les meilleures pratiques aidera les entreprises pharmaceutiques à rationaliser leurs opérations réglementaires. Collaborer avec des fournisseurs réglementaires permet aux entreprises de tirer parti de connaissances et d'expériences spécialisées et d'optimiser leurs chances de succès réglementaire dans ce domaine en évolution et exigeant. Grâce à notre expertise avérée en matière de respect des normes réglementaires mondiales, Freyr peut vous aider à assurer un parcours produit conforme. Pour en savoir plus, contactez-nous.









