
Une multitude de défis sont rencontrés par les départements réglementaires avec le passage des soumissions papier aux soumissions eCTD, une transition qui se poursuit dans le monde entier. La plupart des entreprises des sciences de la vie peinent à se conformer à la norme USFDA pour l'utilisation du format eCTD et à respecter les délais impartis. L'obligation du format eCTD aux US et au Canada a amélioré la procédure de soumission et l'a simplifiée en réduisant le délai entre le temps et le marché, ce qui contribue à minimiser les dépenses liées aux soumissions électroniques pour les industries pharmaceutiques. Bien que les avantages offerts par ce type de soumission soient nombreux, cela reste un défi considérable pour les entreprises des sciences de la vie. Certains des inconvénients rencontrés lors de la publication des soumissions eCTD auprès de la USFDA sont abordés ci-dessous :
- Rapports annuels - L'eCTD ne permet pas facilement de rédiger le rapport annuel comme un seul document pour cette approche, ce qui peut entraîner des erreurs et des problèmes de validation et potentiellement un rejet de la demande.
- Rapports d'études cliniques (CSRs) - La préparation d'un CSR permet aux évaluateurs de naviguer et de suivre facilement les informations, de sorte que même si une section est mise à jour, le rapport n'a pas besoin d'être remplacé.
- Création d'hyperliens - L'un des problèmes les plus courants rencontrés par les éditeurs en raison d'erreurs typographiques lors de la rédaction de documents est la tentative de créer un hyperlien vers une section qui pourrait ne pas exister du tout.
- Numérotation des rapports – Le principal enjeu, lorsqu'une analyse de données d'étude s'étend sur plusieurs rapports, est d'insérer un identifiant d'étude unique afin de garantir que toute référence croisée dans les sections récapitulatives soit claire et facilement identifiable.
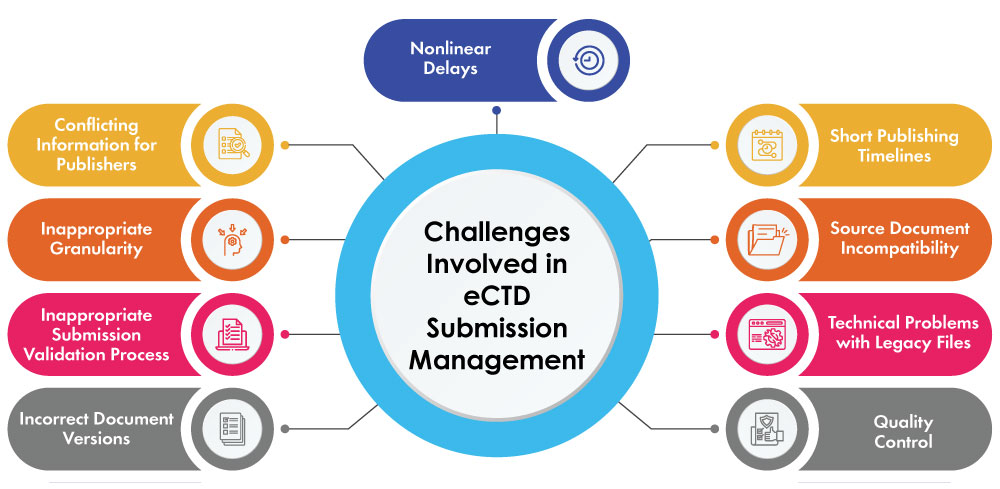
Défis liés à la gestion des soumissions eCTD
Les entreprises pharmaceutiques subissent une pression considérable pour gérer les défis logistiques liés à la gestion des applications et systèmes informatiques afin de soumettre des documents sans erreur dans des délais stricts. Ce défi s'amplifie lorsque les coûts augmentent ou entraînent des retards dans l'approbation du dossier, et, dans le pire des cas, un refus d'enregistrement. Même si les éditeurs peuvent être très expérimentés, les équipes de publication réglementaire rencontrent généralement les problèmes suivants :
- Informations contradictoires pour les éditeurs : Selon l'expérience de l'équipe réglementaire, les informations critiques requises dans le processus de publication sont nécessaires pour être présentées aux éditeurs, mais peuvent également être ambiguës même si elles sont incluses dans le contenu de la soumission. Par exemple, les soumissions eCTD reposent fortement sur l'utilisation de Metadata qui sont incluses dans des capacités critiques telles que les chemins de dossiers dans l'eCTD final, ce qui fournit des informations supplémentaires sur les éléments. Un moyen facile de prévenir les retouches potentielles est d'utiliser des procédures et des formulaires bien conçus, en fournissant ces informations aux éditeurs en même temps que les fichiers source.
- Granularité inappropriée : Un document de publication eCTD produit à l'aide d'un modèle de qualité avec le niveau de granularité approprié a un effet considérable sur la publication. Lorsqu'il est prévu de soumettre une section sous forme de plusieurs feuilles, celles-ci doivent être fournies sous forme du nombre correspondant de documents sources plutôt que d'être compilées en un seul fichier pour être séparées au moment de la publication. Chaque document source qui doit être renvoyé pour reformatage représente une nouvelle petite opportunité de retarder le projet.
- Processus de validation de soumission inapproprié : Une validation inappropriée peut survenir en cas d'erreurs de système ou d'éditeur lors du téléchargement des fichiers. Le principal avantage de l'eCTD est la possibilité de vérifier sa conformité technique lors de la soumission par le demandeur ou l'agence.
- Versions de documents incorrectes : L'objectif est de finaliser la publication d'une soumission avec le bon document ou la bonne version de document, après des contrôles qualité (QC) plus approfondis. Des procédures rigoureuses sont nécessaires pour les groupes qui utilisent des partages de fichiers comme référentiels de publication. Les équipes de publication qui utilisent un système de gestion documentaire (DMS) fermé dans leurs flux de travail de publication évitent généralement ce problème, car seules les versions approuvées peuvent être publiées.
- Retards non linéaires : Non seulement les retards sont parfois inévitables, mais ils peuvent également avoir des effets néfastes sur les délais de soumission. Dans une situation donnée, si la période de publication du projet ne peut être reportée d'un jour ou deux en raison du retard d'autres projets, cela ne fera qu'aggraver le retard.
- Délais de Publication Courts : En raison d'un processus de soumission excessivement long, le temps perdu lors des étapes précédentes du processus est souvent censé être récupéré pendant la publication. L'une des techniques les plus efficaces pour gagner du temps et gérer les risques dans le processus de soumission consiste à publier indépendamment les modules ou les sections de la soumission.
- Incompatibilité des Documents Source : Lors du processus de numérisation des documents source pour extraire automatiquement des informations (provenant de types de fichiers autres que Word/PDF et d'outils de différents fournisseurs), les fichiers source sont numérisés et des éléments tels que les liens internes aux documents, les signets existants et les styles de titres/plans sont traités et collectés dans la base de données du logiciel afin de créer des signets et des hyperliens dans la sortie publiée. Si les fichiers source ne sont pas configurés selon les attentes du logiciel de publication, ce processus peut prendre plus de temps et nécessiter un ajout manuel d'éléments de navigation après la publication.
- Problèmes techniques avec les fichiers hérités : Bien que, dans les moments les plus critiques, les fichiers hérités aient pu être imprimés sans problème par le passé, l'édition électronique est extrêmement efficace pour mettre en évidence les problèmes techniques. Les problèmes ne sont généralement pas difficiles à résoudre, mais ils prennent du temps et entraînent des retards, sachant que l'outil le plus important dans la boîte à outils de l'éditeur est le temps. Une telle situation peut être résolue bien à l'avance par les équipes de soumission en utilisant des versions incrémentielles pour rattraper le temps perdu en raison des problèmes dans le processus.
- Contrôle Qualité: Au moment où la publication commence, le contenu du fichier source doit être finalisé et approuvé, car la modification d'un document pendant le processus de publication peut prolonger encore davantage le calendrier du projet. Voici quelques-uns des points de contrôle qualité qui doivent être clairement définis tout au long du projet pour s'assurer qu'ils sont appropriés à la tâche de soumission eCTD :
- Tous les documents sources doivent obligatoirement faire l'objet d'un contrôle qualité avant d'entrer dans le flux de travail de publication.
- La structure de la soumission (l'assemblage/le plan) au sein du logiciel de publication doit être examinée de manière indépendante avant toute publication.
- Tous les fichiers PDF publiés doivent être examinés à l'écran
- Vérifier les signets et les liens dans les fichiers PDF publiés.
- Toujours valider les soumissions eCTD avant toute soumission.
(Cliquez ici pour votre information)
Freyr Digital propose une solution à tous les défis énumérés ci-dessus pour les activités de publication et de soumission de votre organisation. Freyr SUBMIT PRO, un logiciel eCTD hébergé dans le cloud, facilite le travail de notre équipe des opérations réglementaires et de nos spécialistes de la publication eCTD pour fournir un soutien supplémentaire lorsque vous en avez le plus besoin. Freyr assure des soumissions efficaces et en temps voulu grâce à son logiciel eCTD, soutenu par une visionneuse et un validateur eCTD intégrés.
Souhaitez-vous en savoir plus ? Demandez une démonstration.









