
L'adoption de l'eCTD 4.0 représente une étape cruciale vers la modernisation des soumissions réglementaires à l'échelle mondiale. Avec des avantages tels qu'un suivi amélioré des documents et des efficacités basées sur les Metadata, il n'est pas surprenant que les agences mondiales adoptent ce changement.
Mais où en est l'EMA ? Contrairement à la FDA, qui a défini des phases de mise en œuvre claires, l'EMA adopte une approche plus mesurée, en commençant par des programmes pilotes et des évaluations techniques. Dans ce blog, nous détaillons les plans de l'EMA pour l'eCTD 4.0, son impact potentiel sur les dépôts réglementaires et la manière dont votre entreprise peut garder une longueur d'avance.
Plus important encore, l'EMA a-t-elle déjà rendu obligatoire l'eCTD 4.0 ? Plongeons-nous dans le sujet.
Qu'est-ce que l'eCTD 4.0 et en quoi est-il différent de l'eCTD 3.2.2 ?
Le Document Technique Commun Électronique (eCTD) est le format internationalement accepté pour les soumissions réglementaires. Il uniformise la manière dont les entreprises pharmaceutiques soumettent les demandes d'autorisation de médicaments et gèrent les mises à jour du cycle de vie sur les différents marchés.
La version actuelle, eCTD 3.2.2, est utilisée depuis des années. Cependant, les organismes de réglementation, y compris l'EMA, travaillent sur l'eCTD 4.0, qui est basé sur la norme Health Level 7 (HL7) Regulated Product Submission (RPS). Cette mise à jour améliore l'efficacité des soumissions et la gestion du cycle de vie réglementaire.
Différences clés entre l'eCTD 3.2.2 et l'eCTD 4.0 :
- Meilleure gestion du cycle de vie : Suivi amélioré des versions de documents, réduisant la duplication.
- Granularité plus flexible : Permet la réutilisation de documents structurés pour différentes soumissions.
- Gestion Améliorée des Metadata : Des Metadata plus structurées, rendant les interactions réglementaires plus fluides.
- Meilleure interopérabilité : Conçu pour mieux fonctionner avec les systèmes réglementaires numériques en évolution à l'échelle mondiale.
- Bien que ces changements offrent de nombreux avantages, la transition vers l'eCTD 4.0 exige une préparation, un investissement et une compréhension des attentes réglementaires.
La position de l'EMA sur l'adoption de l'eCTD 4.0
La grande question que tout le monde se pose est : L'EMA a-t-elle rendu l'eCTD 4.0 obligatoire ? La réponse est non, pas encore, mais la transition est en cours.
État actuel de l'eCTD 4.0 dans l'UE :
- À l'heure actuelle, l'eCTD 3.2.2 reste la norme obligatoire pour les soumissions dans l'UE.
- L'EMA a activement évalué l'eCTD 4.0 mais n'a pas encore officiellement rendu son utilisation obligatoire.
- L'agence travaille aux côtés d'autres organismes de réglementation, tels que la FDA et la PMDA du Japon, pour harmoniser les normes mondiales.
- Aucun délai de transition officiel n'a été fixé, mais l'EMA a indiqué que l'eCTD 4.0 deviendra à terme obligatoire.
L'approche de l'EMA : un déploiement progressif avec un programme pilote
Contrairement à la USFDA, qui a défini un plan de mise en œuvre échelonné, l'EMA adopte une approche structurée. L'agence a lancé un programme pilote technique pour tester la mise en œuvre de l'eCTD 4.0 avec les parties prenantes de l'industrie.
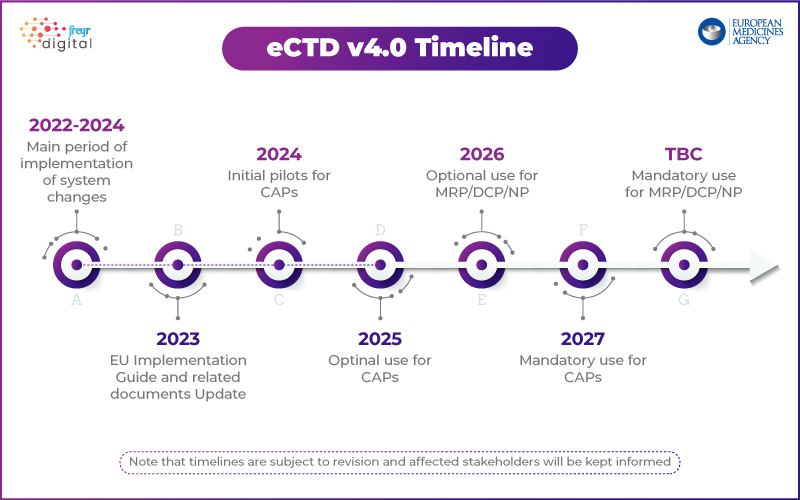
Principaux points saillants de la stratégie eCTD 4.0 de l'EMA :
- Étape 1 : Mettre l'accent sur l'interopérabilité technique avec les outils réglementaires.
- Phases futures : Soumissions d'essai, gestion du cycle de vie et soumissions groupées.
- Projet d'ensemble de mise en œuvre disponible avec des vocabulaires contrôlés et des critères de validation.
L'EMA s'engage à assurer une transition en douceur, et les entreprises des sciences de la vie devraient suivre les mises à jour sur la page officielle eCTD de l'EMA.
Défis et considérations pour les entreprises des sciences de la vie
Bien que l'eCTD 4.0 offre des avantages clairs, son adoption ne va pas sans défis. Voici quelques considérations clés pour les entreprises pharmaceutiques et biotechnologiques :
- Complexités réglementaires
- La transition progressive de l'EMA signifie que les entreprises doivent se préparer à des processus de soumission doubles (eCTD 3.2.2 et eCTD 4.0).
- Différentes régions auront des calendriers d'adoption différents, ce qui exigera des entreprises qu'elles restent agiles.
- Défis techniques
- La migration des données de l'eCTD 3.2.2 vers la version 4.0 nécessite une planification minutieuse.
- Les règles de validation changeront considérablement, exigeant des logiciels et des outils mis à jour.
- Les entreprises doivent investir dans des solutions d'automatisation et basées sur l'IA pour assurer la conformité.
- Risques de conformité.
- Un mappage Metadata incorrect ou le non-respect des nouvelles exigences de granularité des documents pourrait entraîner le rejet de la soumission.
- Les équipes réglementaires ont besoin d'une formation adéquate pour comprendre les nouvelles règles de validation.
- Impact sur les flux de travail existants
- Les entreprises devront adapter leurs processus internes pour s'adapter à l'eCTD 4.0.
- Une collaboration accrue entre les équipes réglementaires, informatiques et de soumission sera nécessaire.
Ce qu'il faut retenir ? Les entreprises doivent commencer à se préparer dès maintenant, même si l'EMA n'a pas encore rendu obligatoire l'eCTD 4.0.
Comment les entreprises peuvent se préparer à la transition vers l'eCTD 4.0 de l'EMA
Bien que l'EMA n'ait pas fixé de date limite officielle, les entreprises proactives bénéficieront d'une préparation anticipée. Voici comment :
- Évaluer les processus de soumission actuels
- Identifier les lacunes dans les flux de travail eCTD 3.2.2 existants.
- Évaluer l'impact des nouvelles règles de gestion du cycle de vie sur les soumissions en cours.
- Investissez dans les bons outils eCTD 4.0
- Sélectionnez un logiciel de soumission réglementaire conforme à l'eCTD 4.0.
- S'assurer que le logiciel prend en charge les normes HL7 RPS et l'automatisation des Metadata.
- Former les équipes réglementaires et informatiques.
- Animer des ateliers et des sessions de formation sur les changements de l'eCTD 4.0.
- Fournir des lignes directrices pour le balisage des Metadata et le suivi du cycle de vie.
- Collaborer avec l'EMA et les pairs de l'industrie
- Participez aux programmes pilotes et aux consultations réglementaires de l'EMA.
- Tenez-vous informé des dernières directives et mises à jour réglementaires de l'EMA.
- Effectuer des tests et la validation
- Effectuer des soumissions de test internes en utilisant les structures eCTD 4.0.
- Identifier les problèmes potentiels dans la granularité des documents et le mappage des Metadata avant le mandat final de l'EMA.
En commençant dès maintenant, les entreprises peuvent assurer une transition en douceur sans perturbations des dépôts réglementaires.
Et ensuite ? L'avenir de l'eCTD 4.0 en Europe
Bien que le calendrier complet de la transition reste incertain, la stratégie à long terme de l'EMA comprend :
- Standardiser les dossiers de soumission sur les marchés mondiaux, améliorant ainsi la cohérence et l'efficacité.
- Réduire les délais d'approbation grâce à un meilleur suivi du cycle de vie des soumissions.
- Intégrer l'IA et l'automatisation dans les processus réglementaires pour améliorer la conformité.
Dans les prochaines années, nous pouvons nous attendre à plus de clarté de la part de l'EMA, y compris des calendriers de transition officiels et de nouveaux critères de validation.
Conclusion
Bien que l'EMA n'ait pas encore rendu obligatoire l'eCTD 4.0, ce n'est qu'une question de temps avant qu'il ne devienne la norme pour les soumissions réglementaires dans l'UE. Les entreprises qui se préparent de manière proactive obtiendront un avantage concurrentiel, assurant leur conformité et évitant les obstacles réglementaires de dernière minute.
Points clés à retenir
- L'eCTD 3.2.2 reste la norme actuelle, mais l'eCTD 4.0 se profile à l'horizon.
- L'EMA adopte une approche progressive, sans mandat officiel à ce jour.
- Les entreprises devraient commencer à se préparer dès maintenant pour assurer une transition en douceur.
- Investir dans les nouvelles technologies, la formation des équipes et le test des soumissions sera essentiel.
Appel à l'action
Tenez-vous informé des annonces réglementaires de l'EMA et commencez à évaluer votre préparation à l'eCTD 4.0. Plus tôt vous vous préparez, plus la transition sera facile lorsque l'obligation entrera en vigueur.
Souhaitez-vous de l'aide pour choisir un logiciel conforme à l'eCTD 4.0 ou pour comprendre comment cette transition affecte votre entreprise ? N'hésitez pas à nous contacter.









