
Pour améliorer l'accès des patients aux médicaments innovants au Royaume-Uni après le Brexit, une nouvelle voie d'approbation accélérée, connue sous le nom de « Innovative Licensing and Access Pathway » (ILAP), a été lancée en janvier 2021. Son objectif principal était de fournir une feuille de route intégrée à toutes les parties prenantes, améliorant ainsi le processus de développement de produits. L'ILAP soutient en outre les développeurs commerciaux et non commerciaux en facilitant l'accès des médicaments innovants à la population de patients, réduisant ainsi le délai de mise sur le marché. Les entreprises pharmaceutiques peuvent envisager l'ILAP comme une voie une fois que les données non cliniques sont consolidées. Elle est applicable aux nouvelles entités chimiques (NCE), aux médicaments biologiques, aux nouvelles indications et aux médicaments repositionnés.
L'ILAP est une initiative développée conjointement par la Medicines and Healthcare products Regulatory Agency (MHRA) en association avec l'All-Wales Therapeutics and Toxicology Centre (AWTTC), le National Institute of Health and Care Excellence (NICE) et le Scottish Medicines Consortium (SMC) en tant que partenaires permanents. Les partenaires de soutien de l'ILAP incluent le National Health Service England (NHS), la Health Research Authority (HRA) et le National Institute for Health Research (NIHR). Ensemble, les parties prenantes apportent des contributions réglementaires, scientifiques, éthiques et commerciales améliorées au stade précoce du développement des médicaments pendant les essais cliniques.
Selon l'avis de Freyr, l'ILAP offre de grandes opportunités aux développeurs de traitements innovants, en particulier à ceux qui répondent à des besoins non satisfaits des patients. Pour un coût relativement modeste (environ 8 000 £), une entreprise pourrait obtenir des conseils précoces, obtenir une désignation pour son produit et convenir d'un profil de développement cible. Cela a le potentiel d'économiser une quantité significative de temps sur le cycle de vie global du développement du produit. Il y a également des avantages à regarder au-delà de l'autorisation de mise sur le marché et à préparer tôt les négociations de remboursement.
L'ILAP se compare favorablement aux dispositifs similaires proposés au sein du réseau européen des médicaments (tel que le PRIME). Bien que différents dans leur concept et leur mise en œuvre, l'ILAP a des critères d'acceptation plus larges et un taux d'acceptation plus élevé. L'ILAP offre également une voie d'intégration avec le Project Orbis de la Food and Drug Administration des États-Unis (USFDA) pour les produits oncologiques émergents.
Comment demander l'ILAP ?
Pour accéder à l'ILAP, les demandeurs doivent demander un Passeport Innovation (PI). L'obtention d'une désignation PI permet aux développeurs de médicaments d'accéder à la voie sur la base des preuves requises pour qu'un produit soit conforme aux critères d'éligibilité définis par le NICE, le SMC, l'AWTTC et la MHRA.
Cette désignation agit comme un catalyseur pour les produits innovants, de la phase préclinique à la phase intermédiaire de développement. L'IP peut mener à la définition d'un document de Profil de Développement Cible (PDC). Le PDC est une feuille de route qui facilite l'accès aux partenaires de l'ILAP dès les premières étapes du cycle de vie du développement des médicaments, afin d'accélérer et de faciliter l'accès des patients à des traitements nouveaux et innovants. Les patients font partie intégrante de ce processus. Plusieurs outils fournis par l'ILAP soutiennent les demandeurs à toutes les étapes du processus de conception, de développement et d'approbation.
Critères de désignation du passeport innovant
Les lignes directrices de la MHRA clarifient les critères pour une désignation IP. Ceci est particulièrement pertinent pour les produits innovants et se compare favorablement aux dispositifs équivalents proposés en Europe.
À l'avenir, l'applicabilité spécifique de la PI pour les dispositifs médicaux et les produits combinés, des domaines où l'innovation est toujours significative, peut s'avérer bénéfique.
La désignation de la propriété intellectuelle (PI) est évaluée par les partenaires permanents et de soutien selon les critères suivants :
- Critère 1 : Détails de la condition, du patient ou du domaine de santé publique
- Pour les affections potentiellement mortelles et graves
- Dans une situation où le besoin est crucial pour les patients
- Critère 2 : Le produit médicinal répond à un ou plusieurs domaines spécifiques qui incluent
- Médicament innovant
- Médicament associé à une nouvelle indication
- Médicament destiné aux maladies rares
- Médicament en développement pour l'objectif de santé publique du Royaume-Uni
- Critère 3 : Le médicament a le potentiel d'offrir
- Un aperçu des avantages que le médicament ou l'indication proposé(e) apportera aux patients.
- Les avis des patients ou des associations de patients sont encouragés.
Lors de la soumission de la demande de PI, une réunion entre les demandeurs et la MHRA a lieu pour déterminer si le produit remplit les trois (03) critères.
Selon les dernières informations de janvier 2022, la MHRA a reçu soixante et onze (71) demandes, dont quarante et une (41) ont abouti à la désignation IP, vingt-deux (22) sont en cours de traitement et sept (07) demandes ont été refusées.
Le moment opportun pour s'engager dans l'ILAP est mentionné ci-dessous.
- Au stade de développement précoce à intermédiaire du produit
- Lorsque des données pertinentes sont disponibles
- Lorsque les demandeurs ressentent le besoin d'obtenir des avis des parties prenantes
- Les demandeurs aspirent à adopter de nouvelles approches innovantes.
- Pas lorsque le produit est vers la fin de la phase de développement
Aperçu du développement de médicaments
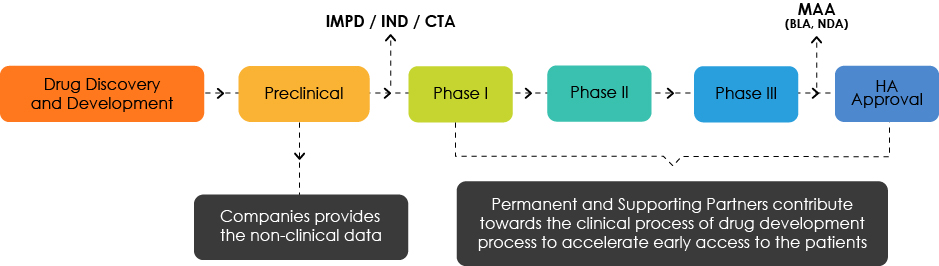
Comprendre le profil de développement cible (TDP)
Les experts TDP analysent les caractéristiques des produits et mettent en évidence les lacunes d'un point de vue réglementaire. Ils sont chargés d'orienter les développeurs de médicaments vers une feuille de route qui permet un accès rapide des patients à leurs produits.
Le TDP est un document mis à jour en temps réel selon les exigences alignées sur le développement du produit. Par conséquent, un produit subit de multiples modifications du TDP à mesure que de nouvelles données sont générées.
L'accès des patients aux médicaments essentiels peut être compromis par les retards de mise sur le marché. Pour éviter de tels scénarios, les voies d'autorisation accélérées agissent comme un catalyseur. L'ILAP est un exemple de voie d'autorisation flexible, bien acceptée dans l'industrie, qui peut accélérer le calendrier de développement des médicaments innovants. Les critères détaillés définis par le système de santé du Royaume-Uni permettent aux demandeurs d'évaluer leur éligibilité à la désignation de passeport innovant (IP). Encourager la satisfaction des besoins cliniques et des patients non satisfaits grâce à des voies accélérées comme l'ILAP facilite l'entrée sur le marché et peut apporter un soulagement aux populations de patients à risque. Pour protéger l'intérêt des patients, les autorités sanitaires ne transigent pas sur la sécurité, l'efficacité ou la qualité du produit tout en garantissant un processus d'approbation accéléré. Les services réglementaires End-to-End de Freyr facilitent le processus de documentation pour soutenir la désignation de passeport innovant dans un délai accéléré, aidant ainsi vos produits à atteindre les patients plus tôt. Contactez Freyr.










