
À compter du 31 janvier 2022, le nouveau règlement pharmaceutique de l'Union européenne (UE) relatif aux essais cliniques (Règlement sur les essais cliniques - CTR) est devenu obligatoire, abrogeant la Directive sur les essais cliniques 2001/20/CE. Ce règlement harmonise les protocoles d'évaluation et de supervision des essais cliniques dans toute l'UE. Les lignes directrices ont été révisées afin de promouvoir une approche uniforme de la recherche clinique, tout en mettant l'accent sur la sécurité des participants aux essais cliniques et une divulgation publique accrue.
La réglementation établit un nouveau système d'évaluation en deux parties pour tous les essais cliniques de l'UE. La première partie consiste en une évaluation scientifique des documents essentiels de l'essai clinique, et la deuxième partie en une évaluation éthique de la documentation au niveau national. Suite à cette évaluation en deux parties, chaque État membre prendra une décision unifiée concernant l'essai et en informera le promoteur via le système d'information sur les essais cliniques.
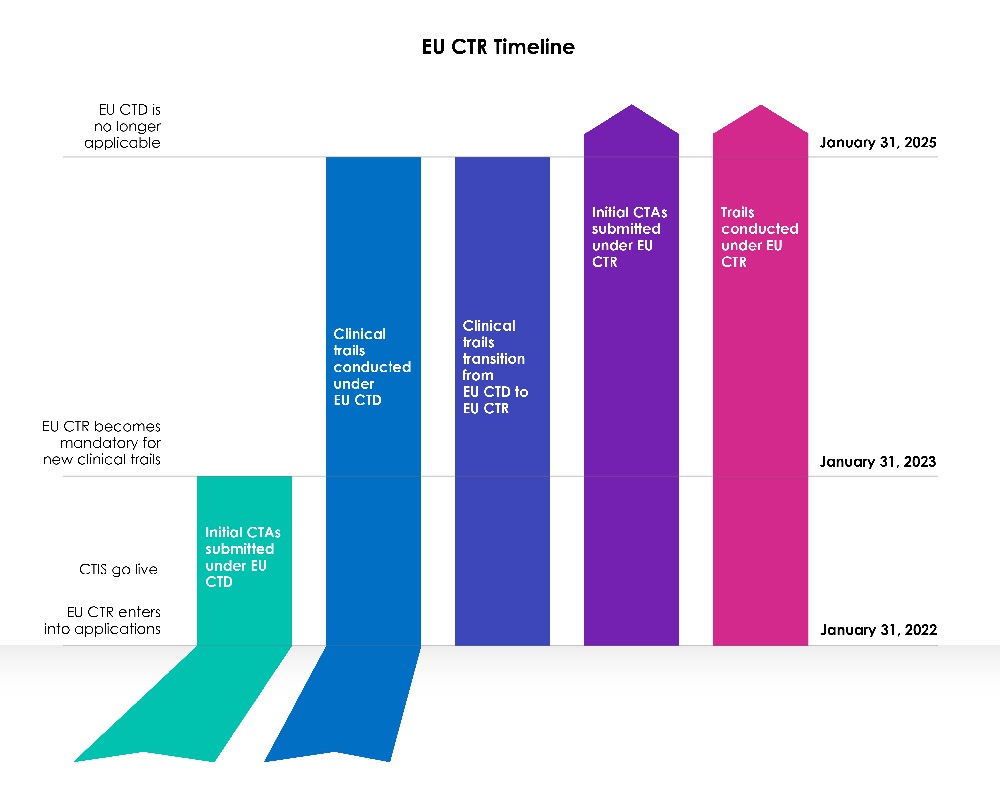
Calendrier de transition pour les nouveaux demandeurs
Une phase de transition de trois (03) ans a débuté avec la date de mise en service du CTIS de l'UE.
Année 1 (31 janvier 2022 au 30 janvier 2023) :
La Directive 2001/20/CE de l'Union européenne (UE) sur les essais cliniques (EU-CTD) a régi les essais cliniques dans l'UE depuis 2004. Elle visait à uniformiser les règles et a considérablement amélioré la sécurité des patients dans les essais cliniques. Cependant, en pratique, elle a créé des conséquences imprévues. Au cours de la première année suivant la mise en œuvre du CTIS, les promoteurs ont été autorisés à choisir de soumettre une nouvelle demande d'essai clinique (CTA) dans le cadre du système d'information sur les essais cliniques (CTIS) en vertu de la directive sur les essais cliniques (CTD : Directive 2001/20/CE), ou d'utiliser le CTIS conformément à la législation actuelle, le Règlement sur les essais cliniques (UE) n° 536/2014.
Les deux idées étaient viables, et les promoteurs ont eu la possibilité de choisir quelle législation suivre.
Les membres étaient prêts à utiliser le Système d'information sur les essais cliniques (CTIS) et ont accepté les demandes en vertu de la nouvelle législation, le Règlement sur les essais cliniques (EU CTR), dès le premier jour de fonctionnement du CTIS.
Années 2 et 3 (31 janvier 2023 au 31 janvier 2025) :
À partir du 31 janvier 2023, toutes les nouvelles demandes d'essais cliniques (CT) doivent être soumises via le CTIS en vertu de la nouvelle législation (CTR).
Les nouvelles demandes d'essais cliniques (CT) ne peuvent pas être soumises dans EudraCT en vertu de la Directive sur les essais cliniques (CTD). La Directive européenne sur les essais cliniques n'autorise plus l'admission de nouveaux Member States après le 31 janvier 2023. Les essais menés en vertu de la CTD doivent d'abord être transférés, après quoi une demande supplémentaire concernant un Member State peut être soumise via EU CTIS.
Pour les candidats existants
Les demandes d'essais cliniques soumises avant le 30 janvier 2023, en vertu de l'ancienne législation (CTD) et utilisant EudraCT, seront autorisées à se poursuivre jusqu'à leur achèvement en vertu de cette directive ((CTD : Directive 2001/20/CE), jusqu'au 30 janvier 2025. Les procédures resteront inchangées et les promoteurs pourront soumettre des modifications importantes et des notifications de fin d'essai comme l'exige la réglementation. EudraCT restera actif pendant la période de transition pour permettre la poursuite de ces essais.
Il est cependant important de noter que les demandes de transition peuvent être soumises à tout moment au cours de la période de transition de trois (03) ans, et les promoteurs sont encouragés à achever le processus suffisamment tôt pendant cette période afin d'assurer la continuité des essais cliniques dans l'UE au-delà du 30 janvier 2025, compte tenu des jours fériés et de l'arrêt de deux (02) semaines en hiver.
Essais non transférables
- Les essais qui sont terminés ou qui se termineront juste avant la fin de la période de transition EU/EEA ne doivent pas faire l'objet d'une transition.
- Si une notification de fin d'essai a été complétée dans tous les Member States de l'EU/EEA, mais que la fin globale de l'essai n'a pas encore été notifiée, l'étude ne doit pas être transférée. En vertu de la Directive, la fin globale de l'essai et les résultats sommaires de l'essai doivent être publiés via EudraCT.
- Les essais qui ont débuté avant la mise en œuvre de la Directive 2001/20/CE ne bénéficient pas d'une telle procédure de transition. S'ils sont interventionnels et doivent continuer à être menés après la fin de la phase de transition du CTR, une nouvelle demande d'essai clinique doit être soumise en vertu du CTR.
- Les essais pédiatriques menés en dehors de l'UE/EEA mais pour lesquels un numéro EudraCT a été attribué ne devraient pas non plus être convertis.
- Les essais qui sont en suspens après la fin de la période de transition ne peuvent pas être transférés. Le redémarrage de l'essai dans ces circonstances nécessiterait la soumission d'une nouvelle demande d'essai clinique en vertu du CTR.
CTIS de l'UE CTIS EMA des mises à jour techniques de EMA afin d'améliorer ses fonctionnalités. Lorsque des modifications importantes sont apportées au CTIS, EMA des notes de mise à jour décrivant les changements intervenus dans le système. Ces mises à jour peuvent inclure des améliorations des fonctionnalités existantes, l'ajout de nouvelles fonctionnalités, ainsi que des perfectionnements techniques et fonctionnels. Un partenaire expérimenté en matière de réglementation peut aider à surmonter les difficultés potentielles et accompagner les promoteurs dans la transition vers le CTIS pour les essais existants et à venir, dans le cadre de leurs stratégies de développement clinique. Cliquez ici pour en savoir plus sur le CTIS l'expertise de Freyr dans ce domaine : https://www.freyrsolutions.com/medical-devices/regulatory-affairs.










