
La Food and Drug Administration (FDAUS a publié en décembre 2022 des lignes directrices révisées, intitulées « Lignes directrices à l'intention de l'industrie concernant l'absence de réponse à une lettre de réponse ANDA (CRL) relative à ANDA demande ANDA d'autorisation ANDA dans les délais réglementaires », qui remplaçaient celles de juillet 2022. Ces lignes directrices ont pour but de guider les demandeurs de demandes abrégées de mise sur le marché de nouveaux médicaments (ANDA) soumises en vertu de la section 505(j) de la loi fédérale sur les aliments, les médicaments et les cosmétiques (FD&C Act) (21 U.S.C. 355(j)). Une réponse complète et pertinente à une CRL est essentielle pour l'autorisation du médicament générique. Le document d'orientation propose des recommandations concernant les conséquences de la réception d'une CRL et les mesures FDA prendre si la réponse à la CRL n'est pas fournie dans le délai imparti.
La FDA s'assurer que les médicaments génériques autorisés répondent aux normes en matière de sécurité, de qualité, d'efficacité et d'accessibilité financière. Si la demande ANDA aux exigences FDA , une lettre de refus (CRL) est envoyée au demandeur, dans laquelle sont énumérées les lacunes identifiées lors de l'évaluation.
Voici une description figurative de ce qu'un demandeur peut faire dans l'année suivant la réception de la CRL :
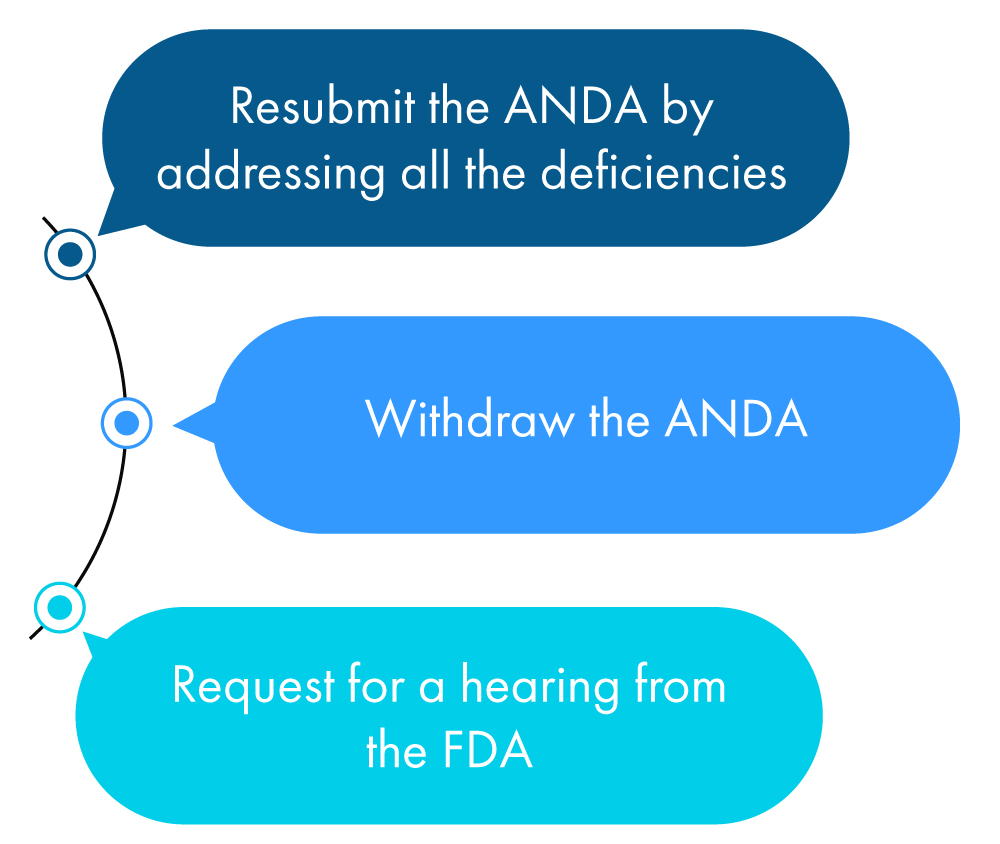
Si le demandeur ne prend aucune des mesures susmentionnées, la FDA cela comme une demande de retrait de la ANDA le demandeur n'ait sollicité un délai supplémentaire pour corriger toutes les anomalies mentionnées dans la lettre de refus (CRL).
Que se passe-t-il après un (01) an de la délivrance de la CRL ?
La FDA une notification écrite indiquant que le demandeur dispose d'un délai de trente (30) jours à compter de la date de cette notification pour :
- Donner les raisons pour lesquelles l'ANDA ne devrait pas être retirée.
- Demande de prolongation de délai pour traiter toutes les lacunes mentionnées dans le CRL
Une fois que la FDA une demande de prolongation de la part du demandeur, elle examine les différents facteurs mentionnés ci-dessous avant de se prononcer sur cette demande :
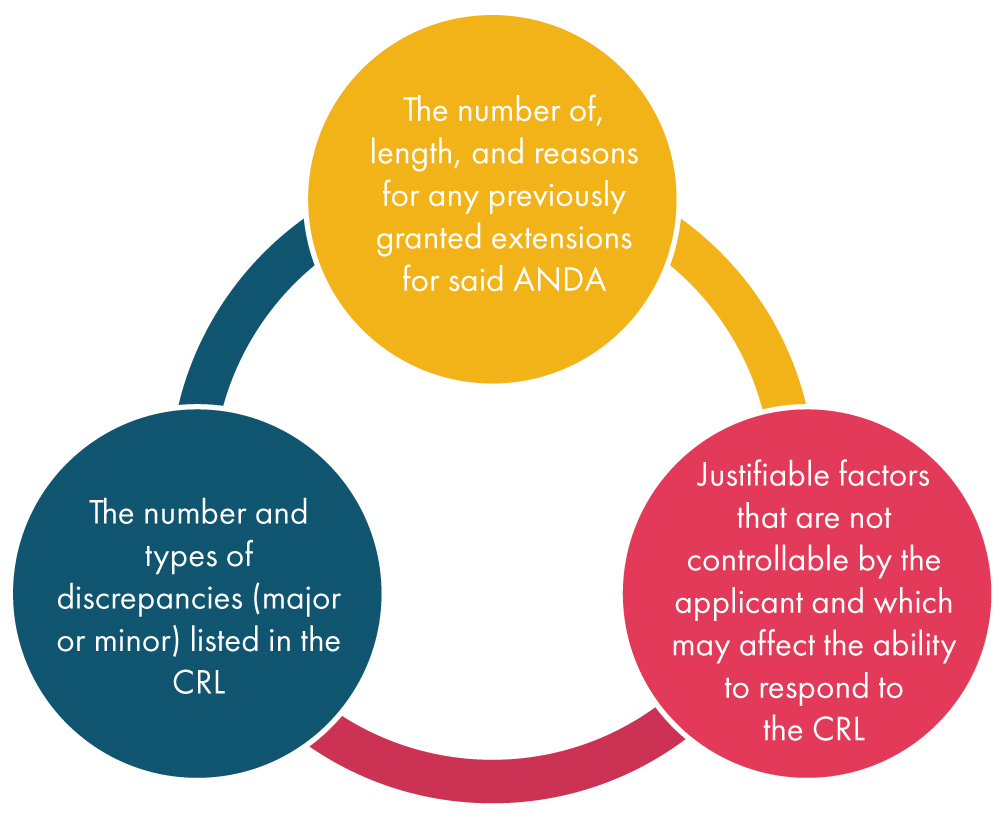
Qu'est-ce qu'un amendement ?
Le demandeur doit présenter une demande de prolongation du délai de réponse à une lettre de refus (CRL) par le biais d'un amendement. La FDA les amendements en deux catégories, majeurs ou mineurs, en fonction de leur incidence sur la procédure d'autorisation.
FDA essentielles FDA que les demandeurs doivent connaître :
- La FDA une modification mineure en modification majeure si celle-ci est soumise plus d'un an après la lettre de refus (CRL), sauf si la ANDA un produit figurant sur la liste des pénuries de médicaments au titre de l'article 506E de la loi FD&C (21 U.S.C. 356e), ou s'il fait l'objet d'une réponse à une urgence de santé publique déclarée par le secrétaire du US de la Santé et des Services sociaux en vertu de l'article 319 de la loi sur les services de santé publique (42 U.S.C. 247d), ou s'il est prévu qu'il soit soumis aux mêmes critères que ceux applicables à une telle déclaration, au moment de la soumission.
- Si le demandeur ne parvient pas à résoudre les divergences constatées dans le CRL dans le délai supplémentaire accordé par la FDA, celle-ci peut envisager de rejeter la demande d'autorisation de mise sur le marché ANDA.
- Si le demandeur a besoin d'un délai supplémentaire supérieur à trente (30) jours, il peut demander une nouvelle prolongation. La demande de modification doit alors contenir de nouvelles informations permettant à la FDA déterminer si la prolongation peut être accordée ou non.
Obtenir une lettre de refus (CRL) de la FDA s'avérer particulièrement intimidant pour ANDA . Qu'il s'agisse de corriger les divergences ou de fournir les motifs et informations appropriés pour justifier une prolongation, toutes les exigences pertinentes doivent être respectées afin d'accélérer le processus d'autorisation du médicament. Freyr est un expert reconnu en matière de réglementation, doté d'une vaste expertise dans le traitement des lettres de refus (CRL) et la mise en conformité avec FDA . Contactez-nous dès maintenant pour bénéficier d'un accompagnement end-to-end dans le cadre de ANDA .










