
Le monde de la réglementation pharmaceutique est sur le point de connaître une mise à niveau majeure avec la mise en œuvre de l'eCTD 4.0. Ce format standardisé promet un parcours plus fluide pour les demandes d'autorisation de nouveaux médicaments soumises aux organismes de réglementation. Mais pour les entreprises qui convoitent une part du marché pharmaceutique japonais de 141,5 milliards de dollars, il y a un rebondissement crucial : le Japon accélère le calendrier d'adoption !
Voici une analyse de ces points saillants :
- Adoption obligatoire : Contrairement à d'autres domaines qui connaissent des phases volontaires avant l'adoption obligatoire, le Japon vise à rendre l'utilisation de l'eCTD 4.0 obligatoire d'ici 2026.
- La préparation est essentielle: La préparation est essentielle en raison des contraintes de temps et de l'absence de chemin de migration direct du format PMDA JP1.0 du Japon vers l'eCTD 4.0. Se concentrer sur un meilleur système aidera les entreprises pharmaceutiques au Japon pendant le processus de transition. Ces étapes incluent la mise à jour des logiciels, la formation du personnel et la préparation des PDF pour le nouveau format.
- Ressources disponibles : L'Agence japonaise des produits pharmaceutiques et des dispositifs médicaux (PMDA) a publié des ressources qui peuvent guider les entreprises à travers ce changement, telles que le « Guide de mise en œuvre du document technique commun électronique ICH eCTD 4.0 », avec des explications sur les changements apportés et les meilleures pratiques disponibles.
Voici quelques raisons pour lesquelles vous ne devriez pas manquer cette opportunité liée aux chiffres :
- Voie rapide vers l'eCTD 4.0 : Contrairement à d'autres régions où le processus est progressif, le Japon vise une adoption obligatoire de l'eCTD 4.0 dès 2026. C'est trois ans avant la date limite fixée par la FDA US pour 2029 ! Avec un calendrier aussi ambitieux, cela signifie que le Japon a pris les devants en matière d'intégration mondiale de l'eCTD.
- Pas de place à l'erreur : JP n'a pas pu être directement converti en eCTD 4.0 contrairement à ses versions précédentes. Cela signifie que les entreprises pharmaceutiques doivent être particulièrement préparées pour éviter tout retard de soumission qui pourrait leur coûter des millions de revenus.
- Un soutien pour une entrée réussie sur le marché : L'Agence japonaise des produits pharmaceutiques et des dispositifs médicaux (PMDA) comprend les défis. Elle a élaboré des ressources, telles que des guides de mise en œuvre, conçues pour accompagner facilement les entreprises à travers ces modifications et assurer leur bonne implantation sur le marché japonais. (https://www.pmda.go.jp/english/).
Si vous développez des médicaments pour l'énorme marché japonais, il est temps de se préparer sérieusement ! Voici votre liste de contrôle avant le décollage :
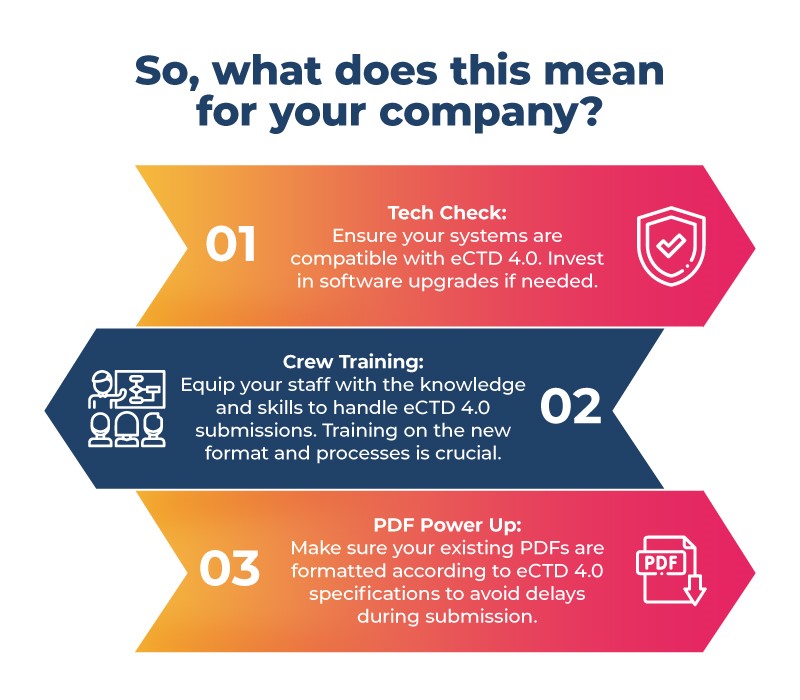
La transition vers l'eCTD 4.0 promet une efficacité accrue et une standardisation mondiale tout au long du processus d'approbation des médicaments. Votre entreprise peut anticiper ce changement au Japon pour une transition en douceur et profiter des innombrables opportunités offertes par cette nouvelle ère. N'oubliez pas que ne pas se préparer, c'est se préparer à échouer – alors, soyez prêt à prendre votre envol avec l'eCTD 4.0 au Japon.
Les avantages et les opportunités acquis sont attractifs pour l'industrie pharmaceutique. Cependant, il comporte son lot de difficultés en cours de route qui doivent être résolues. Afin de naviguer en toute fluidité dans un environnement réglementaire en constante évolution, les entreprises peuvent rechercher des partenariats avec des consultants fiables tels que Freyr. Adoptez l'avenir des soumissions réglementaires au Japon avec notre logiciel eCTD inégalé, Freyr SUBMIT PRO, qui est conforme aux normes 21 CFR Part 11 et dispose d'un modèle de déploiement flexible. Contactez-nous dès aujourd'hui pour en savoir plus et vous engager sur la voie d'une efficacité et d'un succès accrus. Demandez une démo dès aujourd'hui.









