
Bonjour, chers professionnels de la réglementation ! En tant que membre de l'industrie des sciences de la vie, vous êtes probablement familiarisé avec le format de soumission du Document Technique Commun électronique (eCTD) qui révolutionne le secteur de la réglementation des sciences de la vie. Sa structure standardisée change véritablement la donne. Avec ce blog, nous visons à fournir des informations précieuses sur les meilleures pratiques pour les soumissions eCTD. Alors, préparons-nous à devenir ensemble des experts en soumissions eCTD !
Soumissions eCTD et meilleures pratiques
Pour garantir une soumission eCTD réussie, il est essentiel de respecter les exigences réglementaires et de suivre les meilleures pratiques comme illustré dans l'image ci-dessous :
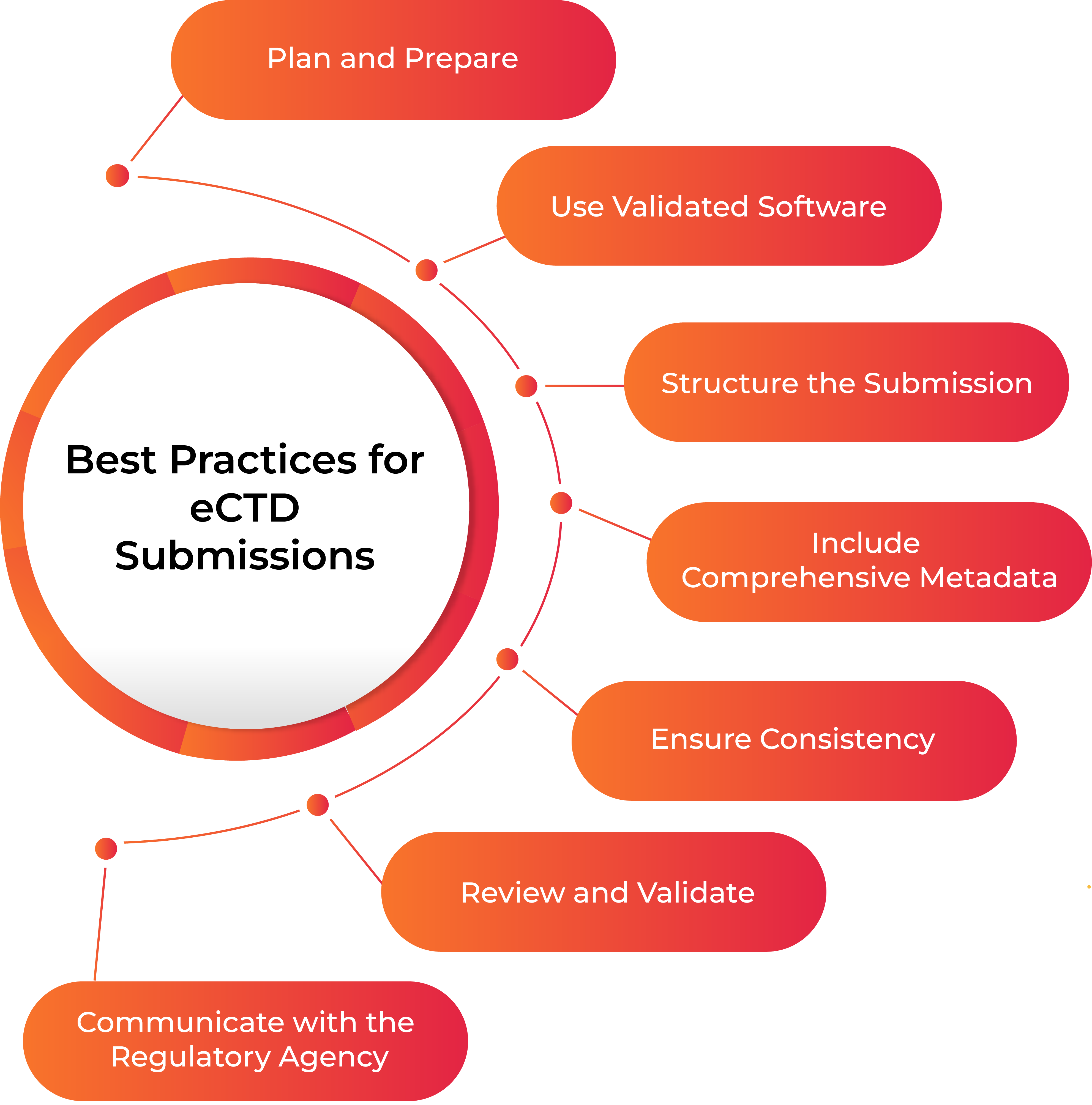
Planifier et Préparer
L'élaboration d'un plan détaillé est la première étape vers une soumission eCTD réussie. Ce plan doit inclure un calendrier, des étapes clés et les responsabilités de chaque membre de l'équipe impliqué dans le processus de soumission. Un temps suffisant doit être alloué à l'examen et à l'approbation du dossier de soumission. Tous les documents requis doivent être préparés et organisés conformément aux directives réglementaires applicables.
Utilisation de logiciels validés
Le logiciel de soumission eCTD doit être validé pour s'assurer qu'il est conforme aux exigences réglementaires. Le logiciel doit être capable de générer des soumissions eCTD sans erreur et bien structurées. De plus, le logiciel doit être fréquemment mis à jour pour s'aligner sur les dernières exigences réglementaires.
Structurer la soumission
Une soumission eCTD bien structurée facilite un examen réglementaire efficace. Elle doit être conforme aux spécifications eCTD du Conseil international d'harmonisation (ICH) et aux spécifications régionales du Module 1. Chaque soumission doit présenter une structure de dossiers clairement définie et cohérente pour l'ensemble du dossier.
Inclure des Metadata complètes
Les Metadata fournissent des informations supplémentaires sur les documents du dossier de soumission, telles que l'auteur, le numéro de version et la date de soumission. Des Metadata complètes facilitent la gestion des documents et permettent aux agences réglementaires de suivre les modifications et d'assurer l'intégrité des données.
Assurer la cohérence
La cohérence est essentielle pour une soumission eCTD réussie. Tous les documents doivent être cohérents en termes de contenu, de formatage et de Metadata. Cette cohérence garantit une navigation aisée dans la soumission et minimise les risques d'erreurs lors de l'examen réglementaire.
Examiner et valider
Avant de soumettre le dossier eCTD, il est essentiel d'examiner et de valider la soumission pour s'assurer de son exhaustivité et de son exactitude. Un examen approfondi garantit que tous les documents requis sont inclus et qu'il n'y a pas d'erreurs ou de divergences. La validation garantit que la soumission est conforme aux spécifications eCTD et aux exigences réglementaires.
Communiquer avec l'Agence de réglementation
Les agences de réglementation fournissent des lignes directrices et des retours sur les soumissions eCTD. Il est important de clarifier les doutes ou les préoccupations soulevés par les autorités de santé avant de soumettre le dossier. Il est également essentiel de répondre rapidement aux questions que l'agence de réglementation soulève pendant le processus d'examen.
En conclusion, suivre les meilleures pratiques est crucial pour les soumissions eCTD. Ce faisant, vous pouvez garantir un processus de soumission fluide, rationalisé et réussi qui répond à toutes les exigences réglementaires et accélère le processus d'examen.
Intégrez Freyr SUBMIT PRO pour répondre à toutes vos exigences de soumission eCTD. Cet outil eCTD est entièrement équipé de fonctionnalités uniques et personnalisées qui rendent le processus plus fluide et plus efficace.
Dites adieu aux soumissions stressantes et bonjour aux soumissions réglementaires sereines avec Freyr SUBMIT PRO !
Demandez une démo dès aujourd'hui !









