
Le marché pharmaceutique malaisien est un pôle en pleine expansion en Asie du Sud-Est, offrant d'importantes opportunités aux entreprises internationales. Avec une demande croissante en soins de santé de qualité et un cadre réglementaire de plus en plus structuré, le marché pharmaceutique malaisien devient une destination attractive tant pour les fabricants de médicaments génériques que pour ceux de médicaments innovants.
Aperçu du marché malaisien : un panorama prometteur pour le secteur pharmaceutique en Malaisie
Les médicaments génériques et les nouvelles entités chimiques (NEC) ont tous deux de solides perspectives sur le marché pharmaceutique malaisien, un secteur en plein essor en Asie du Sud-Est. Le pays offre un environnement dynamique aux entreprises pharmaceutiques grâce à sa population croissante et à des besoins de plus en plus importants en matière de soins de santé. Le secteur de la santé constitue un marché lucratif pour les produits pharmaceutiques, car il est bien établi et dispose d’infrastructures médicales de premier ordre.
Le marché pharmaceutique malaisien se caractérise par une demande croissante de nouveaux médicaments, en particulier dans des domaines thérapeutiques tels que le diabète, les maladies cardiovasculaires et l’oncologie. Le cadre réglementaire s'est structuré davantage, avec des règles précises pour l'autorisation des produits et l'entrée sur le marché, tandis que le gouvernement continue de se concentrer sur l'amélioration des soins de santé publics et de l'accès aux médicaments.
Procédure d'enregistrement en Malaisie :
La procédure d'enregistrement des produits pharmaceutiques en Malaisie est régie par l'Agence nationale de réglementation pharmaceutique ( NPRA), qui est chargée de garantir la sécurité, l'efficacité et la qualité des produits pharmaceutiques.
NPRA en matière d'enregistrement des produits pharmaceutiques sont conformes aux lignes directrices et recommandations de l'Organisation mondiale de la santé (WHO) en matière de qualité, de sécurité et d'efficacité, ainsi qu'à d'autres normes internationalement reconnues telles que celles de la Conférence internationale sur l'harmonisation (ICH). Les principales étapes du processus d'enregistrement sont les suivantes :
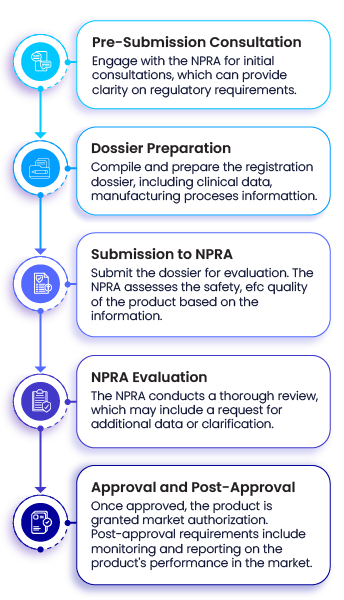
Exigences réglementaires de base :
Pour être homologué en Malaisie, un produit pharmaceutique doit remplir plusieurs conditions réglementaires importantes :
- Bonnes pratiques de fabrication (BPF): Afin de garantir que le produit répond aux exigences de qualité, les sites de fabrication doivent être agréés par les autorités PIC/S .
- Données cliniques: pour prouver leur innocuité et leur efficacité, les nouvelles entités chimiques (NEC) doivent s'appuyer sur des données issues d'essais cliniques. La bioéquivalence doit être démontrée pour les produits génériques.
- Étiquetage et conditionnement: il convient de respecter la législation locale lors de l'étiquetage des produits, en particulier en ce qui concerne la langue et les consignes de sécurité.
- Fiche technique du produit: une description détaillée des ingrédients, du dosage et des consignes d'utilisation du produit est nécessaire.
- Représentation locale: En règle générale, un agent ou un représentant local doit servir de point de contact NPRA. Le demandeur de l'enregistrement du produit, appelé « titulaire de l'enregistrement du produit » (PRH), doit être une société, une entreprise ou une personne morale constituée localement, disposant d'une adresse permanente et enregistrée auprès de la Commission des sociétés de Malaisie (SSM) (dont l'objet social porte sur les produits de santé ou pharmaceutiques).
Étude de cas Freyr : accompagnement d'une entreprise pharmaceutique taïwanaise dans son entrée sur le marché :
Présentation du client : Une société pharmaceutique de premier plan basée à Taïwan a sollicité l'aide de Freyr pour end-to-end en vue du lancementProduits médicaux génériques etProduits médicaux NCE Produits médicaux le marché pharmaceutique malaisien. Son objectif était de garantir une mise sur le marché dans les délais tout en surmontant les complexités réglementaires.
Détails du projet : La mission de Freyr couvre l'ensemble des services réglementaires :
- Stratégie et approche réglementaires: une stratégie conforme à NPRA et adaptée aux besoins du client a été élaborée en vue du lancement du produit en Malaisie.
- Examen technique et analyse des lacunes: un examen approfondi des documents d'enregistrement a été réalisé afin d'identifier d'éventuelles lacunes et de s'assurer de leur conformité avec les exigences NPRA.
- Compilation et soumission: s'est assuré que tous les documents requis étaient complets et conformes aux normes réglementaires avant de compiler et de soumettre le dossier d'enregistrement à NPRA.
- Suivi auprès de NPRA: j'ai supervisé la correspondance avec NPRA répondre à toutes les questions ou demandes supplémentaires, ce qui a permis d'accélérer la procédure d'approbation.
Résultat : Grâce à l'aide de Freyr, le client a pu mener à bien la procédure d'enregistrement en Malaisie. Les produits ont été approuvés rapidement, ce qui a permis une entrée sur le marché sans heurts, en comblant les lacunes techniques et en veillant à ce que les documents requis soient bien fournis. Ce cas a mis en évidence l'expertise de Freyr en matière d'affaires réglementaires et son rôle dans la navigation efficace sur le marché pharmaceutique malaisien.
Grâce à end-to-end offert par Freyr, qui a veillé à ce que l'ensemble du processus réglementaire — de la préparation du dossier à l'autorisation finale — se déroule sans encombre, le client a pu se concentrer sur ses activités principales.
Prêt à vous lancer sur le marché pharmaceutique florissant de la Malaisie ?
Le marché pharmaceutique malaisien offre un immense potentiel de croissance. Cependant, pour s'y retrouver dans le cadre réglementaire, il faut une stratégie bien structurée, une documentation précise et une bonne connaissance du contexte local.
En s'associant à des prestataires de services réglementaires expérimentés tels que Freyr, les laboratoires pharmaceutiques peuvent faciliter leur entrée sur le marché pharmaceutique malaisien, combler leurs lacunes techniques et obtenir des autorisations plus rapidement, ouvrant ainsi de nouvelles perspectives dans cette région en plein essor.










