Les coûts de conformité pour les entreprises pharmaceutiques peuvent représenter jusqu'à 25 % de leurs dépenses opérationnelles totales. Les entreprises pharmaceutiques disposant de multiples portefeuilles de produits sont confrontées à des défis uniques pour gérer la conformité mondiale, suivre les soumissions de dossiers et superviser les variations d'étiquetage. La complexité des exigences réglementaires dans différentes régions, associée à la gestion manuelle de grandes quantités de données, peut entraîner des non-conformités, des retards dans les approbations de mise sur le marché et des inefficacités opérationnelles.
Ce blog explore les défis majeurs rencontrés par les entreprises pharmaceutiques lors de la gestion de portefeuilles de produits multiples et démontre comment les logiciels réglementaires, étayés par des études de cas réelles, offrent une solution stratégique à ces problèmes.
Principaux défis dans la gestion de portefeuilles de produits multiples
- Exigences mondiales complexes en matière de conformité : chaque pays dispose de son propre organisme de réglementation, et les exigences peuvent varier considérablement d'un pays à l'autre. Par exemple, laFDA US , EMA et PMDA japonaise PMDA des formats de dépôt, des délais et des normes de conformité différents. Les laboratoires pharmaceutiques doivent gérer des dossiers variés dans plusieurs régions tout en veillant à respecter scrupuleusement les réglementations locales.
- Suivi des variations d'étiquetage selon les régions : Gérer les variations d'étiquetage pour différentes régions et assurer des mises à jour en temps opportun est l'un des aspects les plus difficiles de la gestion de portefeuille. Une mauvaise gestion des changements d'étiquetage peut entraîner des non-conformités, des rappels de produits et d'importants revers financiers.
- Surcharge liée à la soumission des dossiers : La soumission et la gestion de dossiers pour de multiples gammes de produits, chacune à des stades de développement différents, peuvent rapidement submerger les équipes internes. La gestion manuelle des mises à jour du cycle de vie des produits entraîne souvent des erreurs et des retards d'approbation.
- Mauvaise gestion des ressources : Les équipes ont souvent du mal à allouer efficacement les bonnes ressources. Sans un système de gestion robuste, les entreprises peuvent surcharger leur personnel de tâches administratives, limitant ainsi leur capacité à se concentrer sur les activités stratégiques essentielles.
- Silos de données : Le manque de centralisation signifie que les données relatives aux soumissions, aux approbations et aux mises à jour des produits sont stockées dans des systèmes disparates, ce qui entraîne des inefficacités, des problèmes de communication et des difficultés à maintenir une vue d'ensemble du cycle de vie du produit.
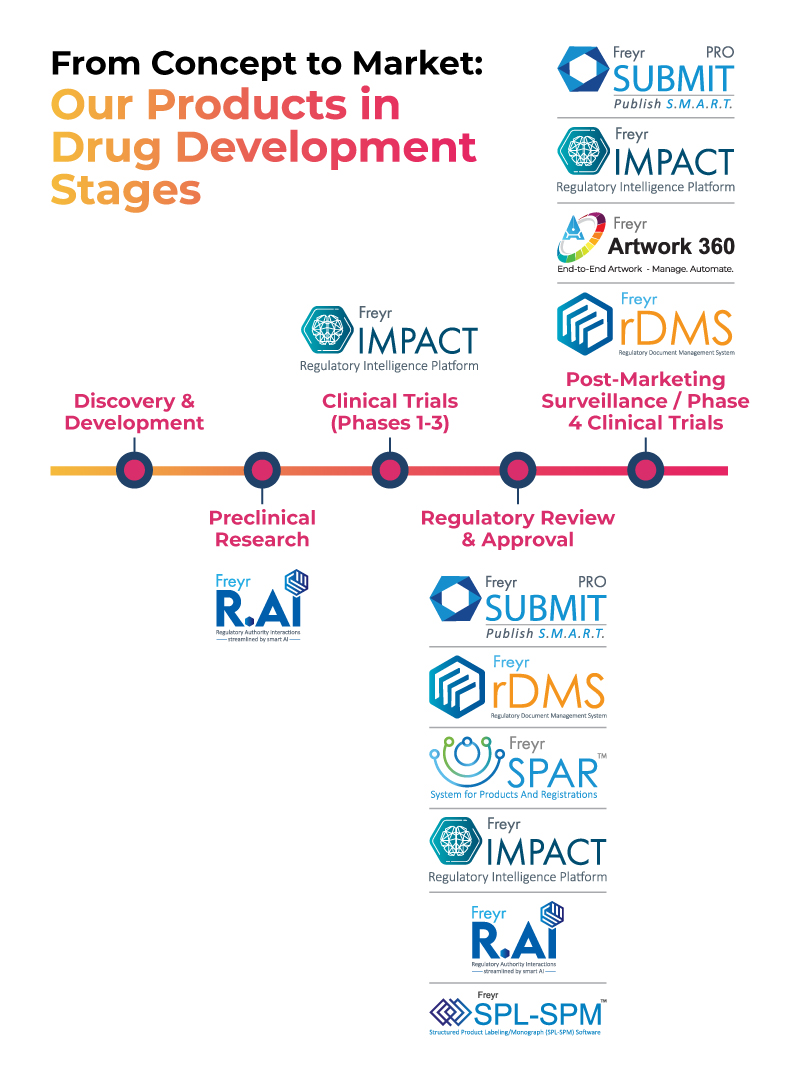
La suite de produits technologiques de Freyr Digital accompagne les entreprises pharmaceutiques du concept à la commercialisation, comme illustré dans l'image ci-dessous.
Études de cas : Comment les logiciels réglementaires offrent un avantage stratégique
En adoptant un logiciel de réglementation, les entreprises pharmaceutiques peuvent automatiser les processus, assurer la conformité et, au final, obtenir un avantage stratégique sur leurs concurrents. Les études de cas suivantes mettent en évidence des exemples concrets de la manière dont nos solutions logicielles de réglementation ont aidé les entreprises pharmaceutiques à relever ces défis.
Cas avéré
Défi du client
Une entreprise pharmaceutique générique basée aux US avait du mal à gérer efficacement ses soumissions réglementaires End-to-End et la gestion de ses documents. Elle était confrontée à des défis liés à des référentiels de documents dispersés, rendant difficile l'accès fluide aux documents réglementaires pour les parties prenantes internes et externes. De plus, le processus de création et de gestion de Structured Product Labeling (SPL) était lourd, entraînant des retards dans les délais de soumission et une augmentation des cycles d'examen.
La solution de Freyr Digital
Freyr Digital est intervenu en tant que fournisseur de solutions virtuelles en affaires réglementaires, en déployant ces trois produits clés comme solutions pour relever les défis du client :
- Freyr rDMS: Un système centralisé de gestion des documents servant de source unique de vérité pour toutes les soumissions et tous les documents réglementaires, garantissant un accès en temps réel et un contrôle des versions pour les équipes internes et les partenaires externes.
- Freyr SUBMIT PRO: Un outil puissant pour la publication et la soumission eCTD, qui simplifie le processus de soumission, réduit le temps de préparation et assure la conformité aux normes réglementaires en constante évolution.
- Freyr SPL-SPM: Une solution efficace pour gérer toutes les activités liées au SPL, améliorant considérablement les processus de création, de gestion et de soumission de documents.
Résultats
En mettant en œuvre ces solutions, Freyr Digital a aidé le client à atteindre :
- Une réduction de 30 % du temps de préparation des soumissions
- Conformité totale à toutes les exigences réglementaires
- Une amélioration de 40 % de l'efficacité du traitement des documents
- Une réduction de 25 % des cycles d'examen
Conclusion : Adopter la transformation numérique pour un succès stratégique
Gérer plusieurs portefeuilles de produits sur les marchés mondiaux n'est pas une mince affaire. Cependant, avec le bon logiciel de réglementation, les entreprises pharmaceutiques peuvent rationaliser les processus, assurer la conformité et obtenir un avantage stratégique dans l'industrie.
La suite d'outils réglementaires de Freyr Digital – comprenant Freyr SUBMIT PRO, Freyr rDMS et Freyr SPL-SPM – a constamment aidé les entreprises pharmaceutiques à réduire les délais de soumission, à améliorer la conformité et à optimiser les ressources. En automatisant les processus manuels, en offrant une gestion centralisée des données et en fournissant des informations en temps réel, nos solutions permettent aux entreprises pharmaceutiques de garder une longueur d'avance sur un marché concurrentiel. Contactez-nous.









