
Dans le paysage fortement réglementé de l'industrie des sciences de la vie, le respect des Lignes directrices spécifiques aux produits (PSG) est primordial pour le développement et l'approbation réussis des médicaments. Les PSG sont des documents complets émis par les autorités sanitaires mondiales (AS) pour fournir des orientations pour l'approbation des produits pharmaceutiques dans des catégories thérapeutiques spécifiques.
Ce blog détaille l'objectif, la pertinence et le point de vue de l'autorité compétente (HA) concernant l'émission des PSGs. Cet article explique en détail la logique et les attentes définies dans les PSGs, qui sont essentielles au succès stratégique des entreprises des sciences de la vie.
Comprendre les lignes directrices spécifiques aux produits et leurs types
Les PSGs jouent un rôle central dans la définition du parcours réglementaire pour les produits pharmaceutiques. En fournissant des orientations ciblées, les HAs garantissent la cohérence et des évaluations solides des demandes de produits au sein de catégories thérapeutiques spécifiques. En adhérant aux PSGs, les entreprises pharmaceutiques peuvent naviguer dans le paysage réglementaire complexe, en s'assurant que leurs produits répondent aux normes de sécurité et d'efficacité requises.
Les PSGs ne se limitent pas au développement de médicaments génériques. Ils couvrent également une large gamme de produits pharmaceutiques, tels que les suivants :
- Pour les médicaments innovants : Les PSG fournissent des orientations spécifiques sur les études précliniques, la conception des essais cliniques, l'évaluation de la sécurité, la pharmacocinétique et les critères d'évaluation de l'efficacité. Elles guident les entreprises sur le type et la quantité de données requises pour démontrer la sécurité et l'efficacité de leurs médicaments innovants.
- Pour les biosimilaires : Les PSG décrivent les exigences en matière de données, les méthodes analytiques et les considérations relatives à la conception des études cliniques pour les produits biosimilaires. En les suivant, les entreprises de biosimilaires peuvent démontrer la similarité de leurs produits avec le produit biologique de référence, ouvrant ainsi la voie à l'approbation et à l'accès au marché.
- Pour les produits biologiques : Ces lignes directrices abordent des aspects cruciaux, tels que la fabrication, la caractérisation et les études de comparabilité, garantissant que les produits biologiques respectent les normes approuvées.
Développement de lignes directrices et de processus spécifiques aux produits
L'élaboration des PSG est un effort collaboratif impliquant les autorités sanitaires, les experts scientifiques et les parties prenantes de l'industrie. Voici les étapes de développement des PSG :
Étape 1 - Évaluation complète du domaine thérapeutique : Les autorités sanitaires (HA) identifient les lacunes dans les lignes directrices existantes et initient le développement de PSG pour combler ces lacunes. Des experts scientifiques et des parties prenantes de l'industrie sont ensuite sollicités pour apporter leur expertise, garantissant que les projets de lignes directrices sont fondés sur des preuves et pratiques à mettre en œuvre.
Étape 2 - Consultation publique: Les projets de PSG sont maintenant disponibles pour examen public et commentaires. Cette approche ouverte et transparente permet aux parties prenantes, y compris les professionnels de la santé (HCP), les groupes de patients et les représentants de l'industrie, de fournir des contributions précieuses et d'améliorer la qualité et la pertinence globales des lignes directrices.
Étape 3: Étape d'examen interne: Pendant que les projets de PSG sont en consultation publique, l'équipe de développement des PSG au sein des autorités sanitaires procède à un examen interne rigoureux, s'assurant que les lignes directrices répondent aux exigences réglementaires nécessaires et s'alignent sur le cadre réglementaire plus large.
Étape 4 - Finalisation: Une fois finalisés, les PSG sont publiés et mis à la disposition de l'industrie, offrant des orientations claires et exploitables pour le développement et la soumission des produits.
Composants des PSG
Les entreprises des sciences de la vie doivent bien comprendre les composants des PSG. Le diagramme circulaire suivant les illustre en détail :
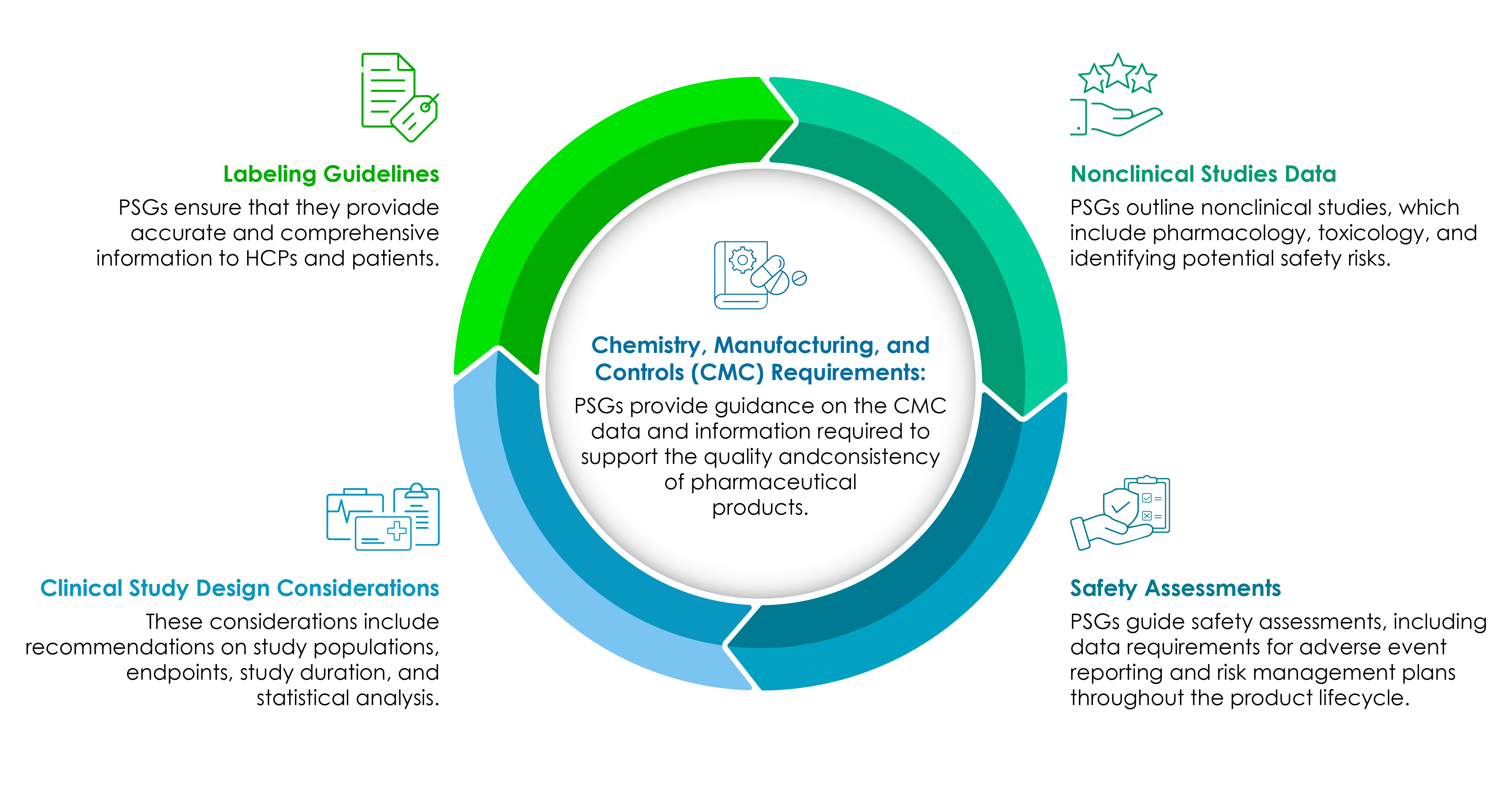
La CMC reste le cœur de chaque développement de produit pharmaceutique axé sur la réglementation.
Gérer les PSG
Naviguer dans les PSG de manière conforme à la réglementation peut être réalisé grâce aux points/stratégies suivants :
- Engagement précoce avec les autorités sanitaires: Un tel engagement favorise une approche collaborative et aide à relever les défis potentiels de manière proactive.
- Expertise scientifique: L'exploitation des contributions d'experts garantit que les conceptions d'études, les méthodes analytiques et les évaluations de sécurité sont conformes aux normes scientifiques les plus élevées.
- Consultants en réglementation: Les consultants offrent des conseils d'experts, assurant le succès des plans de développement et des soumissions réglementaires.
- Examen complet des PSG: Les entreprises doivent identifier les sections spécifiques des PSG applicables à leur produit et aligner leurs plans de développement en conséquence.
- Surveillance continue: Les PSG sont des documents dynamiques qui peuvent faire l'objet de mises à jour ou de révisions fréquentes. Les entreprises doivent surveiller les changements dans les PSG pour assurer la conformité réglementaire avec les dernières exigences des PSG.
Conclusion
Les lignes directrices spécifiques aux produits (PSG) constituent la base des soumissions réglementaires pour les produits pharmaceutiques au sein de catégories thérapeutiques spécifiques. Comprendre les perspectives des autorités de santé (AS) derrière l'émission des PSG est essentiel pour les entreprises des sciences de la vie qui cherchent à accélérer les approbations, à garantir la qualité des produits et à naviguer sans encombre dans le paysage réglementaire mondial.
En tant que fournisseur de services réglementaires de premier plan, Freyr reconnaît l'importance d'adhérer aux meilleures pratiques et de tirer parti de l'expertise qui guidera les entreprises des sciences de la vie à aligner leurs stratégies de développement de produits conformément aux exigences du PSG. Contactez-nous dès aujourd'hui pour en savoir plus sur nos services et comment nous pouvons vous aider à atteindre vos objectifs.









