
Les produits combinés, qui intègrent des médicaments, des dispositifs et/ou des produits biologiques, ont révolutionné les soins de santé en offrant des solutions thérapeutiques innovantes. Cependant, leur nature unique présente des défis réglementaires importants. Ce guide complet explore le paysage complexe de la réglementation des produits combinés et fournit des stratégies pour naviguer avec succès dans ces parcours complexes.
Comprendre les produits combinés et leur cadre réglementaire
Les produits combinés sont des dispositifs médicaux qui associent au moins deux (2) composants réglementés – médicaments, dispositifs médicaux ou produits biologiques – en une seule entité. Ces produits innovants peuvent prendre diverses formes, telles que les stents à élution médicamenteuse, les seringues préremplies ou les patchs transdermiques. Le cadre réglementaire applicable aux produits combinés est principalement défini par la Food and Drug Administration (FDA) aux États-Unis, et des approches similaires sont adoptées par les autorités réglementaires du monde entier.
Le Bureau des produits combinés (OCP) FDA joue un rôle crucial dans la détermination du mode d'action principal (PMOA) d'un produit combiné, qui détermine la voie réglementaire à suivre et le FDA principal FDA chargé de l'examen. Le Centre d'évaluation et de recherche sur les médicaments (CDER), le Centre pour les dispositifs médicaux et la santé radiologique (CDRH) et le Centre d'évaluation et de recherche sur les produits biologiques (CBER) collaborent au processus d'examen, soulignant la nécessité d'une approche intégrée pour garantir la sécurité et l'efficacité des produits combinés.
Déterminer la voie réglementaire
L'une des étapes les plus critiques dans l'élaboration d'une stratégie réglementaire pour les produits combinés est de déterminer la voie réglementaire appropriée. Cette décision est principalement basée sur le PMOA du produit. Voici les considérations clés :
- Mode d'action principal (PMOA) : Identifier le mode d'action unique qui assure l'action thérapeutique la plus importante du produit combiné.
- Affectation au centre principal : En fonction du PMOA, le produit sera attribué au CDER, au CDRH ou au CBER pour examen principal.
- Type de soumission réglementaire : Selon le centre pilote, la soumission peut prendre la forme d'une demande d'autorisation de mise sur le marché d'un nouveau médicament (NDA), d'une demande de licence pour produits biologiques (BLA) ou d'une autorisation de mise sur le marché (PMA).
- Demande de désignation (RFD) : Si le PMOA n'est pas clair, les promoteurs peuvent soumettre une RFD à l'OCP pour une détermination formelle.
- Demande préalable de désignation (Pre-RFD) : L'OCP peut recevoir une demande préalable de désignation (Pre-RFD) pour obtenir des commentaires informels et non contraignants sur les questions de classification et de compétence.
Comprendre ces facteurs est essentiel pour élaborer une stratégie réglementaire efficace adaptée à votre produit combiné spécifique.
Naviguer dans les processus d'examen préalable à la mise sur le marché
Le processus d'examen pré-commercialisation des produits combinés peut être complexe, nécessitant une planification et une exécution minutieuses. Voici les stratégies clés pour naviguer efficacement dans ce processus :
- Collaboration précoce avec les autorités réglementaires : entamer des discussions avec la FDA du processus de développement, dans le cadre de réunions préalables au dépôt de la demande. Ces échanges peuvent fournir des conseils précieux sur les exigences réglementaires, la conception des études et les difficultés potentielles.
- Plan de développement complet : Élaborez un plan solide qui tient compte des aspects uniques de votre produit combiné, y compris la manière dont les composants interagissent et leurs effets combinés sur la sécurité et l'efficacité.
- Approche de test intégrée : Concevoir des études précliniques et cliniques qui évaluent les composants individuels et le produit combiné complet. Cette approche doit évaluer les interactions potentielles et les effets cumulatifs.
- Considérations relatives au système qualité : Mettez en œuvre un système qualité conforme aux réglementations sur les médicaments (21 CFR 210/211) et les dispositifs (21 CFR 820), selon ce qui est approprié pour votre produit.
- Ingénierie des facteurs humains : Intégrer des études sur les facteurs humains pour évaluer les interactions des utilisateurs avec le produit combiné, garantissant une utilisation sûre et efficace.
- Gestion des risques : Élaborer un plan complet de gestion des risques qui aborde les risques potentiels liés à chaque composant et à leur combinaison.
En adoptant ces stratégies, les promoteurs peuvent rationaliser le processus d'examen préalable à la mise sur le marché et augmenter la probabilité de succès réglementaire.
Relever les défis post-commercialisation
Les responsabilités réglementaires pour les produits combinés s'étendent au-delà de l'approbation de mise sur le marché. Une surveillance post-commercialisation et une conformité efficaces sont cruciales pour le succès à long terme. Considérez les stratégies suivantes :
- Pharmacovigilance intégrée : Mettre en œuvre un système de pharmacovigilance robuste qui recueille les événements indésirables liés aux composants médicamenteux et dispositifs du produit combiné.
- Études après commercialisation : Planifier et mener des études après commercialisation pour recueillir des données supplémentaires sur la sécurité et l'efficacité, en particulier pour les nouveaux produits combinés.
- Maintenance du système qualité : Mettre à jour et maintenir continuellement votre système qualité pour assurer la conformité aux réglementations pertinentes concernant les composants de médicaments et de dispositifs.
- Gestion des modifications : Établir un processus simple pour gérer les modifications post-approbation, en tenant compte de l'impact potentiel sur les aspects médicamenteux et de dispositif du produit.
- Intelligence réglementaire : Restez informé des évolutions réglementaires et des documents d'orientation relatifs aux produits combinés afin d'assurer une conformité continue.
En s'attaquant de manière proactive à ces défis post-commercialisation, les fabricants peuvent maintenir la conformité réglementaire et la sécurité des produits tout au long du cycle de vie du produit.
Considérations réglementaires mondiales
À mesure que le marché des produits combinés se développe à l'échelle mondiale, la compréhension des exigences réglementaires internationales devient de plus en plus cruciale. Voici quelques stratégies pour réussir sur le plan réglementaire à l'échelle mondiale :
- Harmonisation réglementaire : Tirez parti des efforts d'harmonisation internationale, tels que ceux du Forum international des régulateurs de dispositifs médicaux (IMDRF), pour simplifier les soumissions réglementaires mondiales.
- Exigences spécifiques au marché : Rechercher et comprendre les exigences spécifiques pour les produits combinés sur les marchés cibles, car les réglementations varient considérablement d'un pays à l'autre.
- Soumissions simultanées : Envisagez des soumissions simultanées à plusieurs agences de réglementation pour accélérer l'accès au marché mondial, le cas échéant.
- Essais cliniques mondiaux : Concevoir des essais cliniques qui répondent aux exigences de plusieurs agences de réglementation pour soutenir les demandes d'autorisation de mise sur le marché mondiales.
- Partenariats internationaux : Collaborez avec des experts réglementaires locaux ou des partenaires sur les marchés cibles pour gérer les réglementations spécifiques à chaque pays et les considérations culturelles.
En adoptant une perspective mondiale dans l'élaboration de la stratégie réglementaire, les fabricants peuvent étendre plus efficacement leur portée commerciale pour les produits combinés.
Conclusion
Naviguer dans les parcours réglementaires des produits combinés nécessite une compréhension approfondie des cadres réglementaires complexes et une planification stratégique.
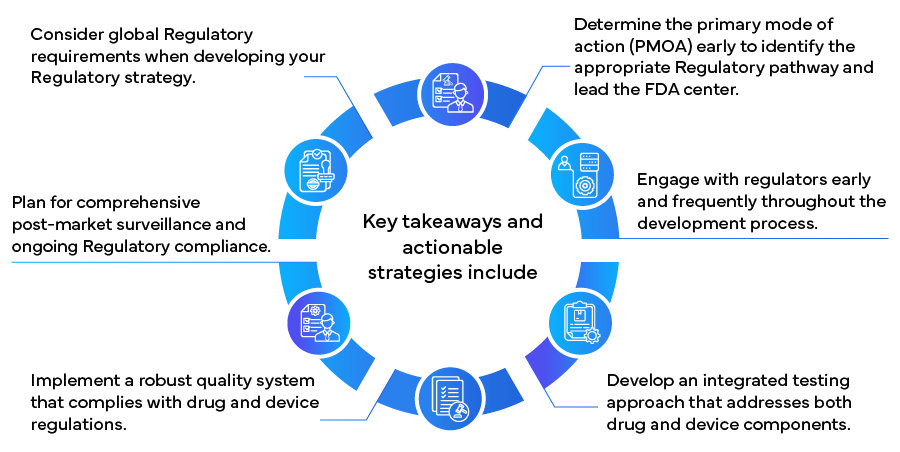
En mettant en œuvre ces stratégies, les fabricants peuvent naviguer plus efficacement dans le paysage réglementaire complexe des produits combinés, accélérant potentiellement la mise sur le marché et assurant une conformité et un succès à long terme. Alors que le domaine des produits combinés continue d'évoluer, rester informé des changements réglementaires et maintenir la flexibilité dans les approches réglementaires sera crucial pour un succès continu dans ce secteur de la santé innovant et en croissance rapide.









