Alors que les produits pharmaceutiques innovants ou de marque entraînent des coûts supplémentaires liés à la recherche et au développement du produit, depuis l'étape d'identification de la molécule jusqu'à l'autorisation de mise sur le marché, les médicaments génériques sont relativement rentables. Ces thérapies réduisent non seulement le coût global du traitement, mais améliorent également de manière significative l'accès des patients aux médicaments vitaux. Étant donné que la dépendance à l'égard de l'importation d'antibiotiques génériques et de thérapies médicamenteuses pour les maladies rares a affecté la disponibilité de ces produits pharmaceutiques à l'échelle mondiale pendant la pandémie, les agences de santé introduisent de nouvelles directives pour soutenir les fabricants de médicaments locaux.
Depuis 1993, l'organisation commerciale Medicines for Europe, anciennement connue sous le nom d'European Generics Medicine Association (EGA), poursuit son objectif de rendre les thérapies rentables accessibles à la population européenne. Au cours de la dernière décennie, elle a fourni avec succès 67 % de tous les médicaments en Europe, augmentant l'accès des patients à 100 % dans sept (07) domaines thérapeutiques clés. Dans le cadre des autorités sanitaires européennes, une « autonomie stratégique » post-Brexit a déclenché une exigence immédiate de remédier efficacement au désavantage concurrentiel auquel sont confrontés les fabricants européens de génériques et de biosimilaires. Avec l'avènement de la pandémie de COVID-19, les capacités de la chaîne d'approvisionnement mondiale ont succombé sous la pression de la demande de médicaments. Des médicaments vitaux qui soulageaient les maladies chroniques ont disparu des rayons des pharmacies locales. Pour surmonter les obstacles liés aux produits pharmaceutiques protégés par des brevets et développer la capacité de fabrication locale de médicaments afin d'améliorer l'accès des patients, le Conseil de l'UE a adopté un règlement qui prévoit une exception pour une molécule originale en accordant un certificat complémentaire de protection (SPC). Cette disposition facilite la fabrication de génériques et de biosimilaires avant l'expiration du brevet à des fins de stockage ou d'exportation. Toutefois, l'exception ne sera applicable que dans les circonstances suivantes.
- Les génériques ou biosimilaires produits sont exclusivement destinés à l'exportation vers un autre pays où le brevet pour la molécule médicamenteuse n'existe pas ou a expiré, ou à des fins de stockage pendant la durée restante du brevet de six (06) mois.
- Conformément à l'exigence, le fabricant a transmis l'information à l'autorité sanitaire locale et au titulaire du Résumé des Caractéristiques du Produit avant trois (03) mois.
- Le fabricant a informé toutes les parties prenantes concernées par la commercialisation du produit.
- Le fabricant s'est assuré que les exigences d'étiquetage stipulent que le produit médicamenteux est uniquement destiné à l'exportation.
En fait
Depuis l'octroi de l'autorisation de mise sur le marché conditionnelle pour les vaccins COVID-19 dans l'UE, le Comité des médicaments à usage humain (CHMP) de l'Agence européenne des médicaments a autorisé quatre (04) sites de production de vaccins en un an ; deux (02) en Suisse et deux (02) aux US. De telles décisions en faveur de l'expansion des sites de production renforceront les capacités de fabrication de vaccins tout en les rendant plus accessibles à la population européenne.
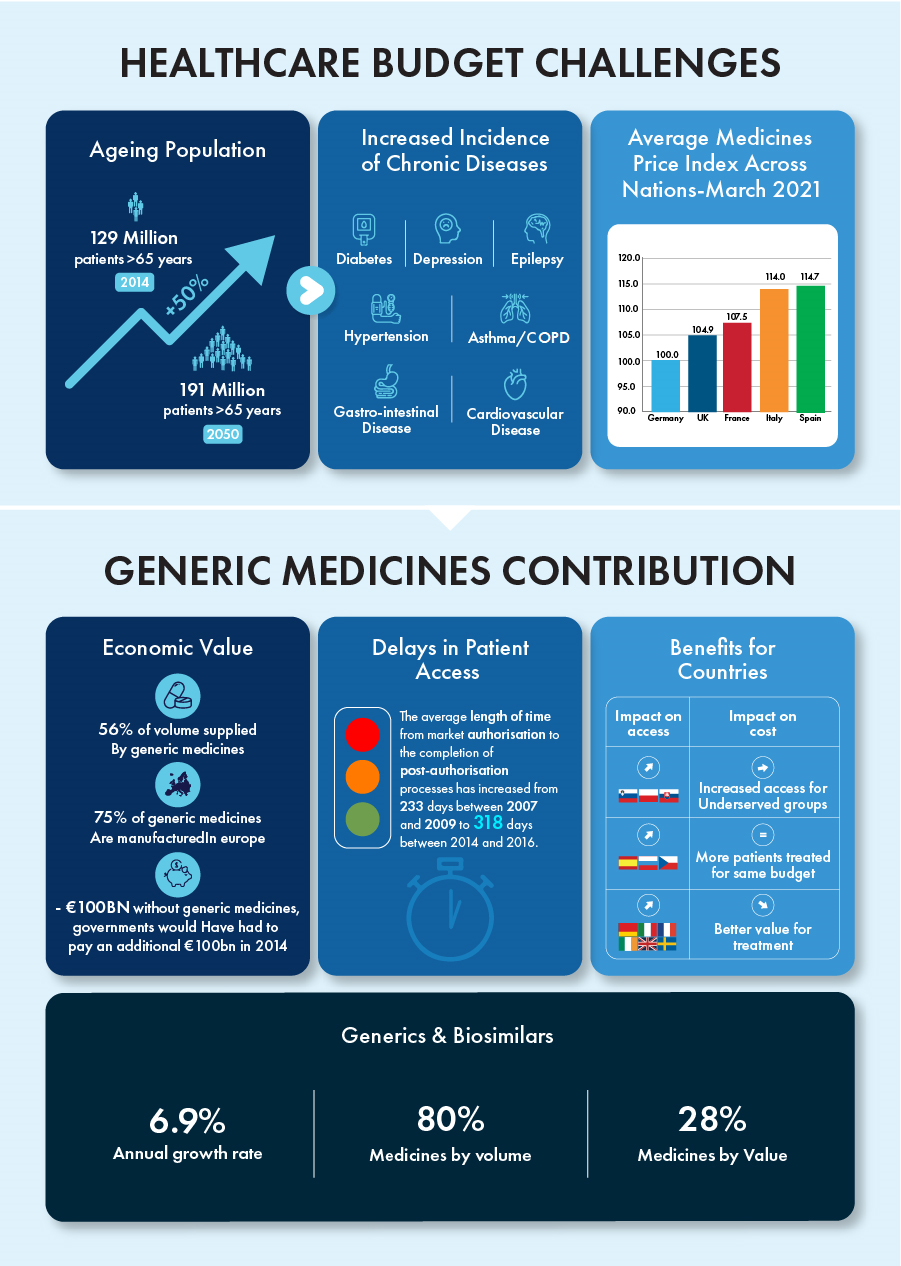
Les génériques et les biosimilaires ont contribué à eux seuls à un taux de croissance annuel de 6,9 %, représentant 80 % de tous les médicaments en volume et 28 % en valeur au cours de la dernière décennie. La durée de brevet de certains produits biologiques, évalués à environ 90 milliards d'euros, prendra fin d'ici 2023, créant un environnement concurrentiel pour ces produits à fort potentiel de croissance.
La mise en œuvre d'une dérogation au CTP (Certificat Complémentaire de Protection) bénéficierait à l'Union européenne en :
- Ajout d'environ 90,5 milliards d'euros supplémentaires par an.
- Créer vingt-cinq mille (25 000) nouvelles opportunités d'emploi, dont deux mille (2 000) emplois directs, pour l'industrie des API de l'UE. Cette initiative aidera les États membres de l'UE à économiser 3,1 milliards d'euros sur les dépenses de santé.
- Constituer des stocks d'alternatives moins chères aux médicaments brevetés innovants afin qu'ils puissent entrer sur le marché immédiatement après l'expiration de la propriété intellectuelle (PI), améliorant ainsi l'accès des patients.
Pour un fabricant de médicaments basé dans l'Union européenne, la mise en œuvre de la dérogation au CCP est l'une des initiatives les plus avantageuses en faveur des génériques. Étant donné que l'Autorité sanitaire de l'UE réglemente les médicaments à usage humain et vétérinaire par le biais d'une procédure centralisée ou décentralisée, naviguer à travers les exigences locales spécifiques peut devenir accablant. Un expert, connaissant les exigences locales concernant les diverses soumissions et les documents de licence, peut vous aider à concentrer vos efforts sur les protocoles de production essentiels plutôt que de vous attarder sur des obstacles réglementaires complexes. Réimaginez votre potentiel commercial en faisant l'expérience de la conformité et de la qualité. Contactez Freyr.









