
Les autorisations d'utilisation d'urgence (EUA) jouent un rôle essentiel pour permettre aux patients Produits médicaux plus rapidement Produits médicaux vitaux. Elles se sont avérées utiles pour faire face à des pandémies telles que celle de la COVID-19. Lancée en 2004 par la Food and Drug Administration (USFDA) des États-Unis, l'EUA est entrée en vigueur lorsque la section 564 de la loi fédérale sur les aliments, les médicaments et les cosmétiques (Federal Food, Drug, and Cosmetic Act) a été modifiée par la loi Project BioShield Act. Ce programme constitue une mesure prise par la FDA protéger la santé publique en garantissant la sécurité, l'efficacité et la qualité des produits médicaux, tout en faisant face aux urgences médicales et aux menaces émergentes pour la santé publique.
Comprenons-le mieux dans les lignes suivantes.
Décrypter l'EUA
La procédure d'autorisation d'utilisation d'urgence (EUA) vise à faciliter l'accès aux contre-mesures médicales en cas d'urgence déclarée. Dans de telles situations, le commissaire de la FDA autoriser les mesures suivantes :
- L'utilisation autorisée de produits médicaux non approuvés.
- L'utilisation non autorisée de produits médicaux approuvés.
Les produits couverts par l'EUA incluent les vaccins, les fluides intraveineux, les médicaments, les dispositifs, les tests, etc., et peuvent être utilisés pour diagnostiquer, traiter ou prévenir des affections potentiellement mortelles. Les produits obtiennent une EUA si les critères suivants sont remplis :
- Preuve d'une condition/maladie potentiellement mortelle.
- Les données scientifiques fournissent suffisamment de preuves que le produit est efficace pour son usage prévu.
- Les avantages du produit l'emportent sur les risques (c'est-à-dire preuve de sécurité).
- Manque de produits alternatifs.
Il est recommandé aux promoteurs de prendre connaissance au préalable des exigences FDAafin de suivre la meilleure procédure réglementaire et de garantir une demande d'autorisation d'utilisation d'urgence (EUA) sans erreur. Vous trouverez ci-dessous les informations obligatoires que le promoteur doit fournir dans sa demande.
Données que le promoteur doit soumettre à la FDA une autorisation d'utilisation d'urgence
- Description du produit et son utilisation prévue.
- Le statut d'autorisation du produit auprès de la FDA.
- Informations sur la sécurité et l'efficacité, telles que les données cliniques et non cliniques, etc.
- Rapport d'analyse des risques et des bénéfices.
- Données de chimie, fabrication et contrôles (CMC).
- Informations sur la posologie, les contre-indications, les mises en garde et les effets indésirables pour la distribution du produit médical concerné.
Comment la FDA délivre-t-elle les autorisations d'utilisation d'urgence (EUA) ?
Voici une interprétation schématique du cycle de vie de l'EUA en bref :
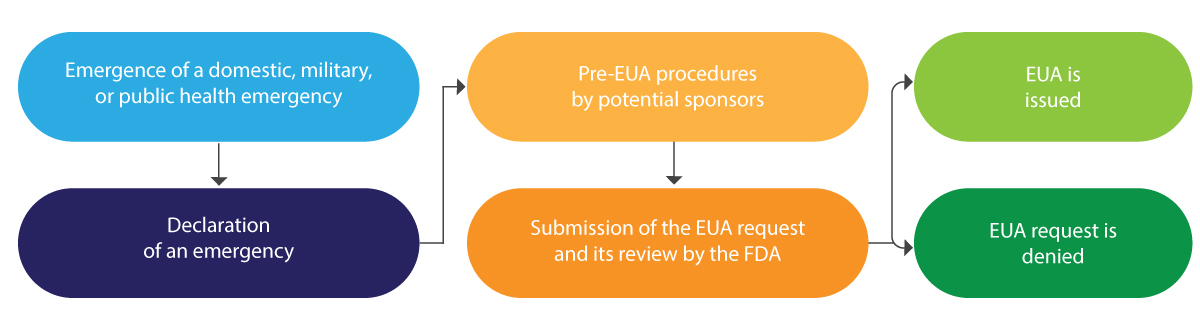
L'autorisation d'utilisation d'urgence (EUA) est généralement délivrée pour une durée limitée et, à la fin de la situation d'urgence en question, elle est révoquée par la FDA.
Autorisation d'Utilisation d'Urgence et COVID-19
Le 31 janvier 2020, le secrétaire à la Santé et aux Sciences humaines (HHS) a déclaré que le COVID-19 constituait une pandémie. Depuis lors, la FDA joué un rôle déterminant dans l'autorisation de plusieurs vaccins et kits de dépistage à domicile dans le cadre de la procédure d'autorisation d'utilisation d'urgence (EUA), afin de faire face à l'épidémie mondiale en cours.
Avec l'émergence de nouveaux variants du COVID-19, l'ensemble de l'industrie pharmaceutique travaille d'arrache-pied pour freiner la propagation et réduire les taux de mortalité. Il existe un besoin de nouveaux Produits médicaux et d'approbations plus rapides par les autorités réglementaires mondiales afin de réduire leur délai de mise sur le marché. La voie de l'autorisation d'utilisation d'urgence (EUA) pour l'enregistrement de nouveaux Produits médicaux/médicaments est la voie à suivre, selon les experts. Plusieurs autres autorités sanitaires comme l'Agence européenne des médicaments (EMA), la Central Drugs Standard Control Organization (CDSCO), la Saudi Food and Drug Authority (SFDA), etc., ont également mis en œuvre la voie de l'EUA pour des approbations plus rapides.
Si vous êtes un fabricant de médicaments et que vous recherchez une EUA pour votre produit vital, vous aurez besoin d'un fournisseur de solutions réglementaires compétent. Contactez Freyr pour un délai de mise sur le marché plus rapide et une voie conforme.










