
Medsafe, également connue sous le nom d'Autorité néo-zélandaise de sécurité des médicaments et des dispositifs médicaux, assure la réglementation des produits thérapeutiques en Nouvelle-Zélande. L'Agence est une unité commerciale du Ministère de la Santé. Elle applique plusieurs législations pour réglementer les produits thérapeutiques, les principales étant la Loi sur les médicaments de 1981 et le Règlement sur les médicaments. Le « but thérapeutique » est décrit dans la Loi sur les médicaments comme le traitement, le diagnostic et la prévention des maladies ou la modification de l'activité physiologique.
Medsafe est responsable de la réglementation de plusieurs catégories de produits qui sont fabriqués, vendus ou fournis en Nouvelle-Zélande. Le diagramme suivant présente les types.

Il existe quatre (04) aspects importants du cadre réglementaire de Medsafe liés aux médicaments et aux dispositifs médicaux. Ils sont décrits ci-après :
Contrôles à l'entrée et à la sortie du marché
Au stade de la pré-commercialisation des médicaments et des produits connexes, il est important d'évaluer leur sécurité, leur qualité et leur efficacité. Sur la base de ces données, Medsafe formule des recommandations au ministère, et ce dernier décide ensuite des mesures à prendre. Un médicament ne peut être mis à disposition sur le marché néo-zélandais que lorsque le ministère l'approuve.
Par la suite, en phase de post-commercialisation, tout signalement d'effet indésirable (EI) peut entraîner le retrait de ces produits du marché. Les réglementations pré-commercialisation et post-commercialisation s'appliquent uniquement aux médicaments (nouveaux et déjà approuvés (avec des modifications de l'ingrédient pharmaceutique actif (API))) et aux produits connexes.
En ce qui concerne les dispositifs médicaux, il n'y a pas besoin d'évaluation et d'approbation pré-commercialisation aujourd'hui. Cependant, les promoteurs doivent notifier le Ministère de leurs dispositifs, afin qu'ils soient enregistrés dans une base de données gérée par Medsafe. Dans la phase post-commercialisation, le Ministère détient le droit de consentir, de révoquer, de retirer ou d'imposer des interdictions sur la vente de dispositifs médicaux.
Qualité
Medsafe garantit la qualité des produits thérapeutiques en Nouvelle-Zélande de plusieurs manières. Voici les principales :
- Établir des normes de qualité au stade de l'approbation préalable à la mise sur le marché pour les médicaments.
- Mettre en œuvre les normes de qualité néo-zélandaises ou les normes de l'Organisation internationale de normalisation (ISO)
- Maintien d'un système d'audit et de licence pour les promoteurs
- Assurer les normes de qualité grâce à une surveillance et un suivi constants.
- Faire respecter les exigences des Bonnes Pratiques de Fabrication (BPF)
Accès
Medsafe suit quelques mesures réglementaires pour contrôler l'accès aux médicaments uniquement. Le système de contrôle est basé sur la classification des médicaments, rendant certains d'entre eux disponibles uniquement par l'intermédiaire de professionnels de la santé qualifiés. La classification est effectuée par le Comité de classification des médicaments, qui travaille sous la supervision du Ministère.
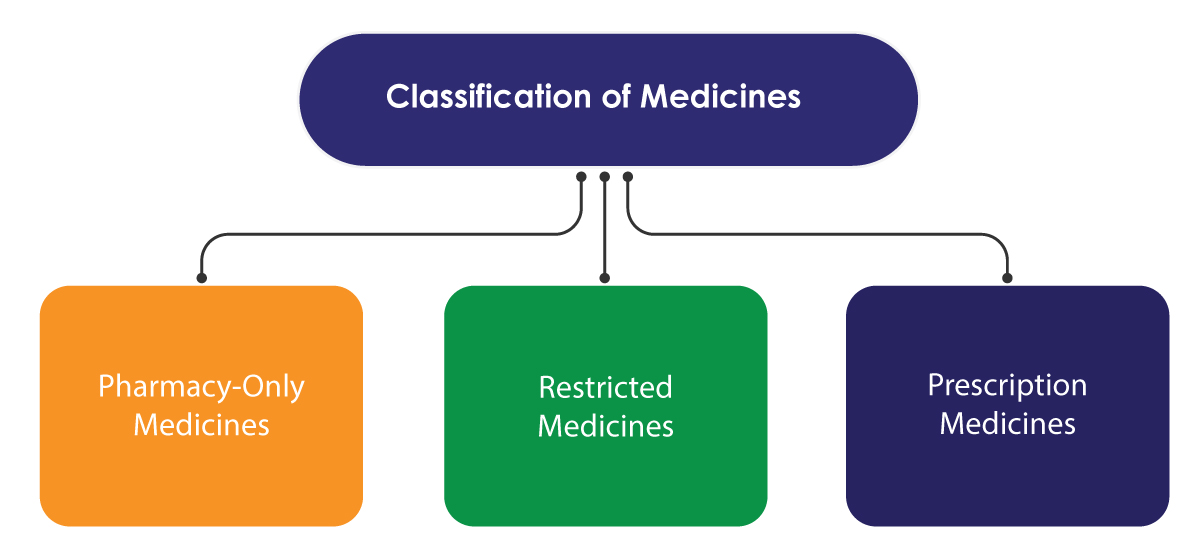
Les médicaments sur ordonnance ne sont vendus que sur prescription d'un professionnel de la santé. Les médicaments à accès restreint peuvent être vendus sans ordonnance, mais doivent être délivrés par un pharmacien agréé. La vente doit être enregistrée pour référence. Les médicaments vendus uniquement en pharmacie peuvent être vendus dans les communautés, les pharmacies hospitalières ou tout magasin agréé pour les vendre.
Il existe une autre catégorie connue sous le nom de Médicaments en Vente Générale. Les médicaments qui ne figurent pas dans les listes de classification de Medsafe relèvent de cette catégorie. Ils peuvent être vendus dans n'importe quel magasin.
Informations
Medsafe exerce une autre fonction réglementaire majeure, qui est la mise à disposition d'informations précises sur les produits en Nouvelle-Zélande. Ces informations incluent, sans s'y limiter, l'étiquetage, les données de prescription et les ordonnances pour les médicaments soumis à restriction, ainsi que les contrôles sur la publicité.
En tant que sponsor/fabricant souhaitant développer ses activités en Nouvelle-Zélande, vous aurez besoin du soutien d'un expert réglementaire éprouvé comme Freyr. Contactez-nous pour des services réglementaires et des solutions fluides et complets.










