
Une lettre d'avertissement est un message officiel adressé par une autorité sanitaire à une organisation qui enfreint les règles et réglementations en vigueur. Dans le cas des entreprises pharmaceutiques, le respect de plusieurs Bonnes Pratiques de Fabrication (BPF), Bonnes Pratiques Cliniques (BPC), Bonnes Pratiques de Distribution (BPD), etc., est obligatoire pour éviter de recevoir un tel avertissement. Il existe plusieurs situations dans lesquelles une autorité sanitaire, et notamment une autorité sanitaire, peut être amenée à émettre un avertissement. FDA , publie ces lettres.
Par exemple, récemment, une entreprise pharmaceutique indienne a reçu une lettre d'avertissement de la Food and Drug Administration des États-Unis ( USFDA ) pour des violations concernant ses ingrédients pharmaceutiques actifs ( APIs ) l'usine de fabrication. Cette action s'est fondée sur l'inspection de l'usine effectuée par le FDA Il y a quelques mois.
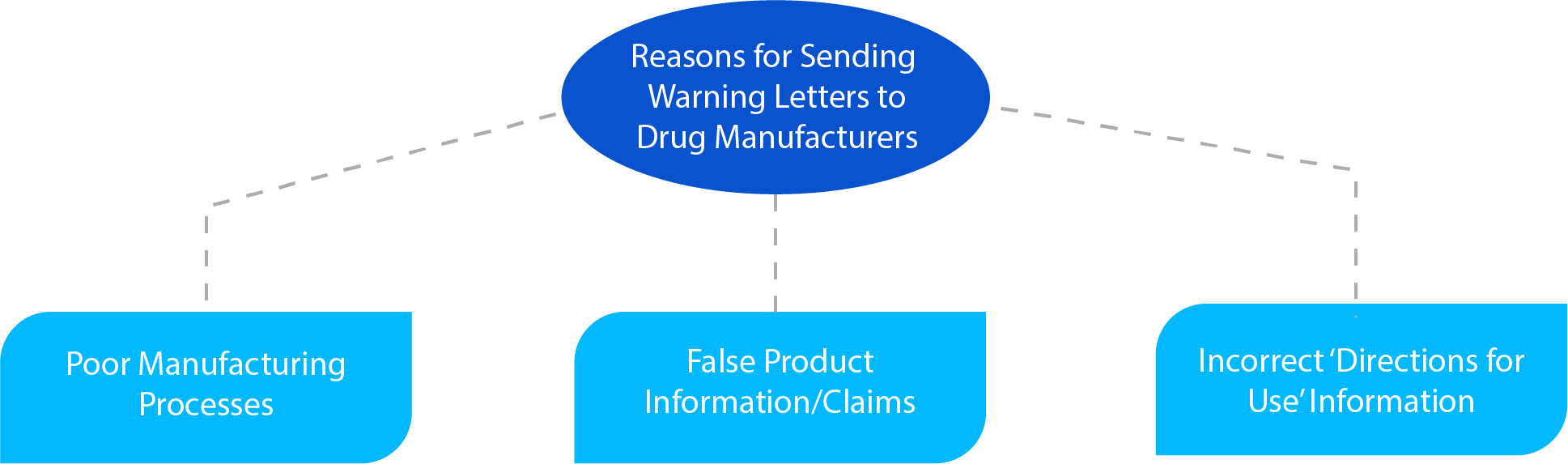
Que peut contenir une lettre d'avertissement ?
La lettre d'avertissement est assez détaillée et peut contenir les informations suivantes selon le cas :
- La violation identifiée par l'HA lors de la conduite d'une inspection, est essentiellement l'une des trois (03) raisons spécifiées dans le diagramme ci-dessus.
- Liste des mesures correctives à prendre pour le problème identifié.
- Délai dans lequel le fabricant doit informer le FDA du plan de correction.
Une lettre d'avertissement, cependant, est un revers qui peut affecter plusieurs facteurs au sein de l'entreprise. En voici quelques-uns ci-dessous.
Répercussions d'une lettre d'avertissement
- Retard de mise sur le marché.
- Revers financier lors de la prise de mesures correctives.
- Responsabilité de la chaîne d'approvisionnement due à un arrêt du processus de fabrication.
Conclusion
Éviter les raccourcis et les violations dans le cycle de vie de la fabrication est le seul moyen d'éviter les lettres d'avertissement des HAs respectives. Quelques entreprises ont dû cesser leurs activités en raison de violations majeures des directives. Le soutien d'un expert réglementaire End-to-End comme Freyr peut aider les fabricants pharmaceutiques à suivre une voie conforme. Contactez Freyr dès maintenant et évitez tout risque.









