Le SmPC, ou Résumé des Caractéristiques du Produit, est un document légal qui fait partie de l'autorisation de mise sur le marché de chaque médicament. Ce document sert de base d'informations sur l'utilisation des médicaments pour les professionnels de la santé. Les informations incluses dans le SmPC sont mises à jour régulièrement en fonction de l'apparition des dernières informations. Le SmPC contient plus d'informations qu'une Notice. Les informations du SmPC peuvent être trouvées via les sources suivantes :
- Sites web des autorités de santé ; tels que l'Agence européenne des médicaments (EMA).
- Dictionnaires des médicaments
De quoi se compose un SmPC ?
- Informations liées à l'utilisation du médicament
- Informations qualitatives et quantitatives sur les bénéfices et les risques des médicaments
- Informations posologiques
- Méthode d'administration
- Informations pharmacologiques
- Informations sur les soins individuels
Structure d'un SmPC
La structure du SmPC est définie par la législation pharmaceutique européenne. Les informations incluses dans le SmPC doivent être spécifiques au produit et peuvent faire l'objet de renvois pour éviter toute redondance. Elles doivent être documentées dans un langage clair et ne doivent pas prêter à confusion. Le SmPC est divisé en 6 sections principales :
- Nom du produit
- Composition
- Forme pharmaceutique
- Informations cliniques spécifiques – Comprend les indications thérapeutiques, les recommandations posologiques et les informations de sécurité
- Propriétés pharmacologiques – Tiennent compte des indications thérapeutiques des éléments cliniques et de leurs effets indésirables potentiels.
- Particularités pharmaceutiques – Comprend les informations réglementaires relatives au médicament
Selon la structure de l'EMA, un SmPC peut être représenté comme suit :
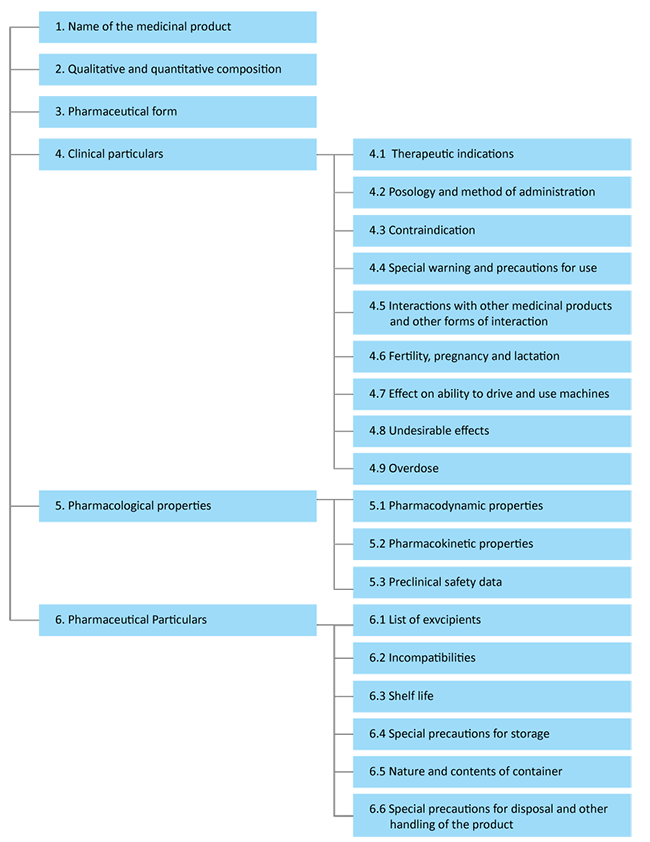
Référence : EMA
Quelles informations sont exclues d'un SmPC ?
- Informations disponibles dans les rapports publics d'évaluation (détails du développement scientifique)
- Informations sur les indications non approuvées.
- Problèmes pour lesquels les données sont insuffisantes
- Conseils généraux sur les affections pharmacologiques
Le maintien d'un SmPC est important pour le cycle de vie de tout médicament, car il fait partie de son autorisation de mise sur le marché. Par conséquent, la rédaction d'un SmPC conforme est fortement recommandée. Cherchez-vous une assistance réglementaire experte pour développer un SmPC ? Contactez Freyr à l'adresse sales@freyrsolutions.com.