
L'étiquetage des médicaments est l'un des aspects les plus scrutés en matière de conformité réglementaire. Une erreur, même mineure, peut avoir des conséquences importantes tant pour la sécurité des patients que pour la réputation d'une entreprise. Considérez les conclusions suivantes :
- Chaque mois, 20 % des entreprises du secteur pharmaceutique et des dispositifs médicaux signalent des problèmes de contrôle qualité liés à l'étiquetage.
- Des études ont montré que, sur certains marchés, 40 % des étiquettes de médicaments ne respectent pas les exigences réglementaires et omettent souvent des informations essentielles en matière de sécurité.
- Au niveau mondial, 35 à 40 % des rappels de produits sont dus à des erreurs d'emballage et d'étiquetage, selon les résumésFDA US .
- Dans le cadre des audits réglementaires, plus de 50 % des constatations concernent la documentation relative à l'étiquetage, qu'il s'agisse des informations de prescription, artwork des traductions.
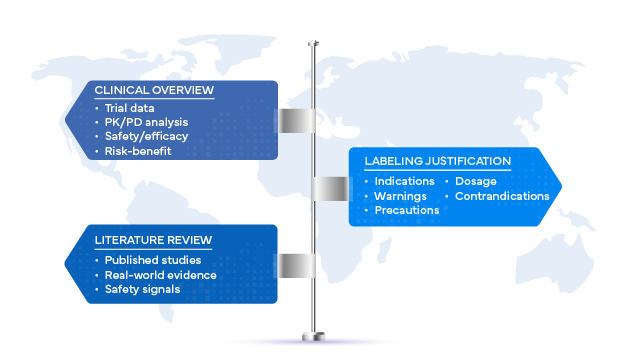
Ces statistiques mettent en évidence une réalité : les décisions en matière d'étiquetage doivent être précises, fondées sur des données probantes et pleinement justifiées. La pierre angulaire de cette justification réside dans l'analyse clinique et les revues systématiques de la littérature.
Le rôle de la synthèse clinique
La synthèse clinique, telle que définie par ICH (R2), est bien plus qu'une simple formalité réglementaire. Il s'agit d'une analyse structurée et critique de l'ensemble des données cliniques disponibles étayant le développement d'un produit. Lorsqu'elle est intégrée à l'étiquetage, elle joue un rôle déterminant pour garantir que la sécurité, l'efficacité et le rapport bénéfice/risque soient clairement présentés dans les informations de prescription.
Les principaux apports de la synthèse clinique à l'étiquetage sont les suivants :
- Mettre en correspondance directe les résultats des essais cliniques avec les allégations relatives au produit
- Justifier l'inclusion d'avertissements, de précautions et de contre-indications
- Garantir la cohérence entre les conclusions en matière de sécurité et les décisions relatives à l'étiquetage
- Présenter aux autorités de réglementation une analyse avantages-risques transparente et fondée sur des données factuelles
Par exemple, si les données d'essai révèlent un effet indésirable statistiquement significatif dans un sous-groupe, l'analyse clinique justifie l'ajout d'avertissements spécifiques à ce sous-groupe dans la notice.
Pourquoi les revues de littérature sont indispensables
Si les données issues des essais cliniques constituent le fondement de la justification de l'étiquetage, les revues systématiques de la littérature élargissent la base de données probantes en intégrant des résultats qui ne proviennent pas uniquement des études menées par les promoteurs. Ces revues synthétisent les publications évaluées par des pairs, les données issues de la pratique clinique et les données de sécurité post-commercialisation afin d'offrir aux autorités de réglementation une perspective plus large et impartiale.
Une analyse documentaire approfondie aide les entreprises à :
- Valider les allégations relatives à la sécurité à l'aide de sources indépendantes
- Détecter les signes avant-coureurs ou les effets indésirables qui ne sont pas apparus lors des essais cliniques
- Comparaison des résultats avec ceux des produits concurrents ou analyse des tendances générales du secteur
- Harmoniser les fiches techniques de base (CCDS) avec les documents sur les produits locaux (LPD) spécifiques à chaque région
Par exemple, des études publiées ou des méta-analyses peuvent mettre en évidence des effets indésirables rares mais graves, ce qui renforce la justification d'ajouter ou de mettre à jour une mise en garde sur l'étiquette.
Exigences réglementaires relatives à la justification de l'étiquetage
Les autorités sanitaires mondiales, notamment laFDA US , EMA, MHRA et PMDA, attendent que les justifications figurant sur l'étiquetage reflètent la rigueur scientifique, la transparence et la cohérence. Les évaluateurs réglementaires examinent souvent :
- Hiérarchie des données probantes : privilégier les données issues d'essais contrôlés randomisés tout en tenant compte des études observationnelles ou des études en conditions réelles pertinentes
- Cohérence entre les documents : veiller à ce que la synthèse clinique, le résumé de la sécurité clinique (SCS) et l'étiquetage proposé soient cohérents
- Justification claire : expliquer pourquoi chaque indication, recommandation posologique ou mise en garde est incluse (ou exclue)
L'absence de données probantes claires à l'appui de l'étiquetage peut entraîner des demandes de précisions de la part des autorités réglementaires, un allongement des délais d'examen, voire un rejet.
Bonnes pratiques pour justifier les décisions en matière d'étiquetage
Les laboratoires pharmaceutiques peuvent renforcer leurs dossiers d'étiquetage en adoptant les bonnes pratiques suivantes :
- Collaboration interfonctionnelle : impliquer les équipes cliniques, de sécurité et réglementaires pour une interprétation globale
- Tirer parti de la technologie : utiliser des outils basés sur l'IA pour les revues de la littérature afin d'accélérer le tri et l'extraction
- Tenir à jour la documentation : consigner les motifs d'inclusion et d'exclusion pour les études afin de répondre aux exigences des audits réglementaires
- Comparaison à l'échelle mondiale : s'aligner sur les produits concurrents et les directives en constante évolution afin de combler les lacunes en matière de conformité
- Mise à jour continue : intégrer les nouvelles publications et les données de pharmacovigilance dans les stratégies d'étiquetage en cours
Conclusion
Compte tenu de la surveillance réglementaire sans précédent et de l'augmentation des coûts liés à la non-conformité, les entreprises ne peuvent se permettre de se baser sur des hypothèses lors de la rédaction des étiquettes de leurs produits. Une analyse clinique rigoureuse, associée à une revue exhaustive de la littérature, garantit que chaque allégation s'appuie sur des preuves scientifiques transparentes.
Chez Freyr Solutions, nous aidons les entreprises pharmaceutiques internationales à s'y retrouver dans cette complexité. Notre end-to-end en matière d'étiquetage réglementaire, de documentation clinique et de stratégies de conformité garantit que vos décisions en matière d'étiquetage sont scientifiquement fondées, conformes aux exigences réglementaires et harmonisées à l'échelle mondiale.
Collaborez dès aujourd'hui avec Freyr pour renforcer votre stratégie d'étiquetage grâce à des justifications fondées sur des données probantes, auxquelles les autorités de réglementation font confiance et sur lesquelles les patients comptent.










