
L'interchangeabilité avec un produit biologique de référence est une étape cruciale dans le processus d'approbation des biosimilaires. Elle garantit qu'un biosimilaire peut être substitué au produit de référence sans risque significatif de réduction de l'efficacité ou d'augmentation des problèmes de sécurité. Ce blog vise à comprendre la dernière mise à jour de la FDA concernant les considérations pour atteindre l'interchangeabilité, ainsi que les meilleures pratiques de l'industrie pour parvenir à l'excellence réglementaire.
Définition de l'interchangeabilité.
L'obtention de l'interchangeabilité est un processus complexe et rigoureux qui exige de satisfaire à des exigences réglementaires strictes. Le défi consiste à démontrer que le biosimilaire correspond non seulement au produit de référence en termes de sécurité et d'efficacité, mais qu'il offre également les mêmes résultats cliniques chez tout patient. Le non-respect de ces exigences peut entraîner des retards ou des refus d'approbation, ce qui affecte l'accès au marché et les soins aux patients.
Exigences réglementaires pour l'interchangeabilité
La FDA décrit des critères spécifiques pour démontrer l'interchangeabilité dans ses documents d'orientation. Ces critères incluent :
- Études analytiques comparatives : Des études analytiques approfondies sont nécessaires pour démontrer que le biosimilaire est très similaire au produit de référence. Ces études évaluent la structure moléculaire, la fonction et la composition du biosimilaire.
- Études cliniques : Des études cliniques sont nécessaires pour confirmer que le biosimilaire ne présente pas de différences cliniquement significatives par rapport au produit de référence en termes de sécurité, de pureté et de puissance. Cela implique souvent des études pharmacocinétiques (PK) et pharmacodynamiques (PD) comparatives.
- Études de substitution : La FDA exige des études de substitution pour évaluer l'impact de l'alternance entre le biosimilaire et le produit de référence. Ces études sont cruciales pour garantir que la substitution n'affecte pas l'efficacité ou la sécurité du traitement.
- Stratégies d'évaluation et d'atténuation des risques (REMS) : Le cas échéant, les REMS doivent être prises en compte pour s'assurer que le biosimilaire peut être utilisé de manière interchangeable sans préoccupations supplémentaires en matière de sécurité.
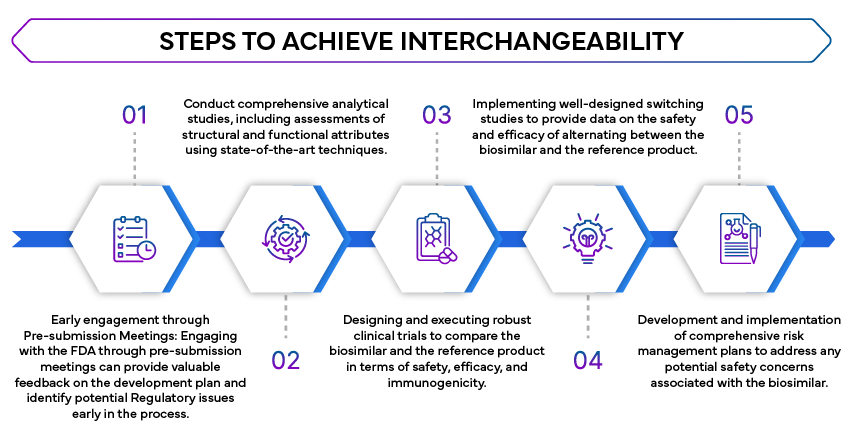
Étapes pour atteindre l'interchangeabilité de manière stratégique
Rôle d'un partenaire réglementaire
Les partenariats réglementaires peuvent améliorer considérablement la probabilité d'atteindre l'interchangeabilité. Voici comment un partenaire réglementaire peut aider :
- Conseils d'experts : Fournit des conseils d'experts sur les exigences réglementaires et les stratégies pour respecter les directives de la FDA.
- Support documentaire : Aide à la préparation de documents de soumission de haute qualité qui sont conformes aux normes réglementaires.
- Conception d'études cliniques : Soutient la conception et l'exécution d'études cliniques et de substitution robustes.
- Interactions avec les autorités sanitaires : Facilite une communication efficace avec les autorités sanitaires, assurant un retour d'information rapide et constructif.
- Gestion des risques : Élaborer des stratégies complètes de gestion des risques pour atténuer les problèmes de sécurité potentiels.
Avantages d'avoir un partenaire réglementaire
| Avantages | Description | |
| 1. | Expertise en exigences réglementaires | Compréhension approfondie des paysages et des exigences réglementaires mondiaux. |
| 2. | Documentation rationalisée | Assure la préparation d'une documentation précise et conforme. |
| 3. | Processus de soumission efficace | Réduit le temps et les coûts grâce à une gestion efficace des soumissions. |
| 4. | Conformité améliorée | Minimise le risque de retards et de rejets grâce à une conformité rigoureuse. |
| 5. | Gestion efficace des risques | Identification proactive et atténuation des risques potentiels. |
Résumé
L'obtention de l'interchangeabilité avec un produit de référence est un processus exigeant mais essentiel pour l'approbation réussie des biosimilaires. Cela requiert une compréhension approfondie des exigences réglementaires, une planification méticuleuse et des données cliniques solides. Collaborer avec un fournisseur de services réglementaires expérimenté peut considérablement augmenter les chances de succès, en garantissant que le biosimilaire respecte les critères stricts établis par les autorités réglementaires. En s'appuyant sur des conseils d'experts, une documentation rigoureuse et une gestion stratégique des risques, les promoteurs peuvent naviguer plus efficacement sur la voie complexe de l'interchangeabilité.










