
Ces dernières années, le paysage des affaires réglementaires a connu une transformation significative. Au cœur de ce changement se trouve un accent croissant sur l'approche centrée sur le patient, les autorités sanitaires (AS) du monde entier reconnaissant le rôle inestimable que jouent les patients dans le développement et l'approbation de nouveaux Produits médicaux. Ce changement n'est pas seulement une tendance ; c'est une réinvention fondamentale de la manière dont nous abordons les soumissions réglementaires et, en fin de compte, de la manière dont nous servons ceux qui comptent le plus – les patients.
Le problème :
Traditionnellement, les soumissions réglementaires se concentraient principalement sur le respect des exigences techniques et scientifiques, négligeant souvent l'impact direct sur l'expérience et les résultats pour les patients. Cette approche, bien que rigoureuse, ne parvient parfois pas à saisir les nuances des besoins, des préférences et de l'utilisation réelle des produits médicaux par les patients. En conséquence, il y avait un décalage entre les approbations réglementaires et la valeur réelle apportée aux patients.
Approches réglementaires centrées sur le patient :
Les autorités sanitaires, notamment la FDA EMA, ont fait des progrès considérables pour intégrer le point de vue des patients dans leurs cadres réglementaires.
Cette approche privilégiant le patient est évidente dans plusieurs domaines clés :
- Développement de médicaments axé sur les patients (PFDD) :
Le programme PFDD FDA est une initiative novatrice qui recueille systématiquement les avis des patients afin d'orienter le développement des médicaments et la prise de décision en matière de réglementation. Ce programme comprend des séances d'écoute des patients, des réunions publiques et l'élaboration de documents d'orientation visant à renforcer l'implication des patients tout au long du cycle de vie des produits. - Preuves issues de la vie réelle (RWE) :
La valeur des données de la vie réelle est de plus en plus reconnue pour comprendre la performance d'un produit au sein de diverses populations de patients. Les autorités sanitaires (HAs) sont désormais plus ouvertes à prendre en compte les RWE dans les dossiers réglementaires, offrant ainsi une vision plus complète des bénéfices et des risques d'un produit. - Résultats rapportés par les patients (PROs) :
L'inclusion des PROs dans les essais cliniques et les soumissions réglementaires est devenue de plus en plus importante. Ces mesures saisissent directement l'expérience du patient, fournissant des informations précieuses sur les symptômes, la qualité de vie et la satisfaction du traitement. - Engagement précoce et conseils scientifiques :
Les autorités sanitaires encouragent les promoteurs à s'engager tôt dans le processus de développement, incluant souvent des représentants de patients dans ces discussions. Ce dialogue précoce aide à aligner les plans de développement sur les besoins des patients et les attentes réglementaires. - Participation des patients aux évaluations bénéfice-risque :
La FDA EMA toutes deux mis en place des cadres visant à intégrer le point de vue des patients dans les évaluations bénéfice-risque, afin de garantir que les décisions réglementaires tiennent compte de ce qui importe le plus aux patients.
Tableau : Principales initiatives axées sur le patient des principales autorités sanitaires
| Autorité de santé | Initiative | Description |
|---|---|---|
| FDA | Développement de médicaments axé sur le patient (PFDD) | Approche systématique pour recueillir les contributions des patients |
| EMA | Groupe de travail Patients et Consommateurs (PCWP) | Forum de dialogue avec les organisations de patients et de consommateurs |
| MHRA | Implication des patients et du public | Stratégie pour impliquer les patients dans les processus réglementaires |
| Santé Canada | Cadre d'engagement pour les médicaments et les produits de santé canadiens | Renforce la participation des patients aux activités réglementaires |
Rôle des fournisseurs de services réglementaires :
Dans ce paysage en évolution, le rôle des professionnels et partenaires des affaires réglementaires est devenu plus crucial que jamais. Ils servent de pont entre les promoteurs, les autorités de santé et les patients, garantissant que les stratégies réglementaires s'alignent sur des approches centrées sur le patient.
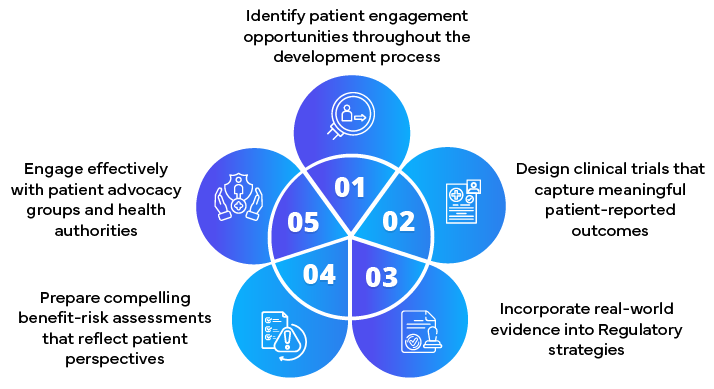
Les principales responsabilités comprennent :
- Élaboration de stratégies d'engagement des patients.
- Intégrer les retours des patients dans les soumissions réglementaires
- Conseiller sur la collecte et la présentation de données centrées sur le patient
- Faciliter un engagement précoce avec les autorités de santé
- Se tenir au courant des exigences réglementaires centrées sur le patient en constante évolution
Rôle des partenaires réglementaires pour des soumissions axées sur le patient
Résumé :
L'orientation vers la patient-centricité dans les affaires réglementaires représente une opportunité significative de développer et d'approuver des produits médicaux qui répondent véritablement aux besoins des patients. En adoptant cette approche, les promoteurs peuvent non seulement naviguer plus efficacement dans les parcours réglementaires, mais aussi fournir des produits qui améliorent significativement la vie des patients. Alors que les autorités sanitaires continuent d'affiner leurs approches centrées sur le patient, l'expertise des prestataires de services réglementaires ou de leurs partenaires devient inestimable pour garantir que les soumissions répondent non seulement aux exigences techniques, mais qu'elles correspondent également aux expériences et aux priorités des patients.
Dans cette nouvelle ère des affaires réglementaires, placer les patients au premier plan n'est pas seulement une bonne pratique – c'est la clé du succès.









