
ATTEINDRE LA DATE LIMITE DE CONFORMITÉ IDMP D'ICI JUILLET 2016 : UNE ENTREPRISE NON TRIVIALE
De nombreuses questions se posent concernant l'IDMP, par exemple : où se trouvent les données au sein d'une organisation ? Le nettoyage et l'alignement des données actuelles sont-ils nécessaires ? Comment les entreprises organisent-elles ces données pour faciliter leur récupération et leur soumission ? L'organisation dispose-t-elle de processus qui pourraient bénéficier d'un référentiel centralisé ?
Atteindre la conformité à l'Identification des Produits médicaux (IDMP) n'est pas une tâche anodine ; l'activité doit prendre en considération diverses pressions réglementaires et opérationnelles. Les organisations doivent attendre que les autorités publient les lignes directrices finales et approuvent les spécifications. En même temps, attendre ces lignes directrices pourrait ne pas leur laisser suffisamment de temps pour mettre leurs affaires en ordre.
L'IDMP est une norme complexe avec des implications globales en matière de données, nécessitant la collaboration et la coopération de nombreuses unités transversales. Cette transition offre l'opportunité d'examiner de manière End-to-End les processus métier et les capacités informatiques d'une organisation à travers de nombreuses unités fonctionnelles. Elle contribue également à la mise en place d'un système robuste de gestion du changement.
Les organisations doivent comprendre qu'une bonne architecture de l'information demande des efforts et du temps pour être mise en place, et doivent également reconnaître que l'IDMP n'est pas simplement un xEVMPD plus grand. Il est également important de noter que les lignes directrices de l'ICH ne représentent qu'une partie de l'ensemble, et que la disponibilité de lignes directrices régionales est essentielle. Il faut aussi prendre en considération que les implémentations régionales parallèles auront des portées et des délais différents, avec une vaste étendue de contributeurs de données.
De plus, les entreprises pharmaceutiques souhaitant commercialiser leurs produits dans les régions réglementées doivent se conformer à l'IDMP à partir de 2016. Récemment, l'EMA a organisé une journée d'information sur l'IDMP et a partagé l'état d'avancement de sa mise en œuvre et son calendrier. Après discussion avec l'industrie pharmaceutique, les fournisseurs de logiciels et l'analyse de son propre système et de la disponibilité de ses ressources, l'EMA a prévu de diviser la mise en œuvre globale de l'EU-IDMP en plusieurs itérations. Ce plan sera proposé à la Commission européenne (CE) pour approbation et, si elle parvient à convaincre la CE, la mise en œuvre de l'IDMP dans l'UE s'étendra de 2016 à 2018. Dans le pire des cas, si la CE n'est pas d'accord, il n'y a pas de plan B. Les amendes pour non-conformité peuvent atteindre 5 % du chiffre d'affaires d'une organisation ; ne pas disposer d'une bonne solution pour la conformité IDMP initiale et continue est un risque qu'aucune entreprise pharmaceutique ne peut se permettre de prendre.
IDMP : DÉVELOPPÉ COMME UN ENSEMBLE DE NORMES MONDIALES SOUS L'ÉGIDE DE L'ISO
Dans le cas où une législation doit être introduite sur l'identification des produits médicaux dans l'un des pays ISO, elle sera basée sur les normes ISO IDMP. Une fois que différentes régions adopteront les normes IDMP, la saisie des données sera cohérente et, à leur tour, les entreprises mondiales et les régulateurs auront accès à des données croisées pour vérifier la cohérence entre les régions. De plus, des vocabulaires contrôlés communs faciliteront grandement ce processus.
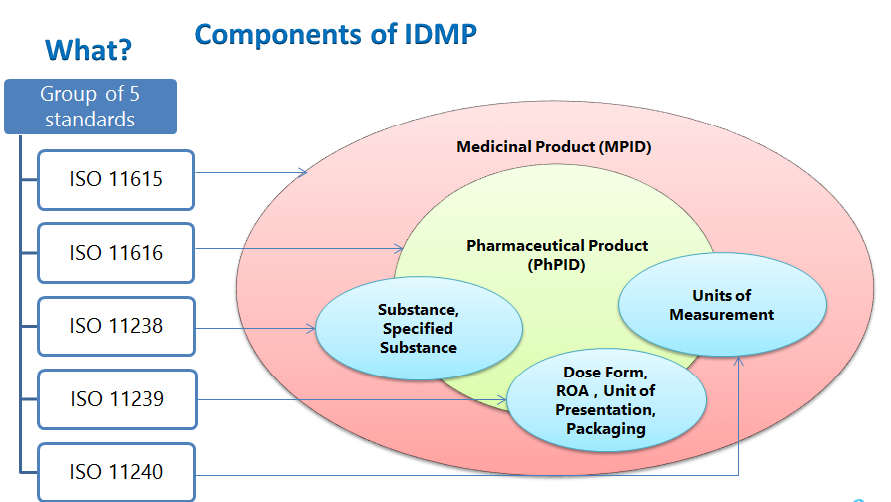
Les éléments structurels de l'IDMP comprennent l'identifiant du produit médicamenteux, l'identifiant du produit pharmaceutique, l'identifiant de la substance, les vocabulaires contrôlés (forme posologique, voie d'administration), les composants de l'emballage, les unités de présentation, les unités de mesure et la description du processus de fabrication à soumettre.
NORMES IDMP
- ISO 11615 – Informations sur les produits médicinaux
- ISO 11616 – Informations sur les produits pharmaceutiques
- ISO 11238 – Substances
- ISO 11239 – Formes pharmaceutiques, Unités de présentation, Voies d'administration et Conditionnement
- ISO 11240 – Unités de mesure
STATUT ACTUEL
ICH prépare des guides de mise en œuvre et révise les normes ISO.
Les régulateurs de l'UE se préparent à l'IDMP
- L'EMA a lancé des travaux pour établir la liaison avec le réseau réglementaire de l'UE afin de définir les cas d'usage des données IDMP.
- L'EMA est en train de mettre en place un “Groupe de travail EU ISO IDMP recruter des experts des comités de l'EMA et du Conseil des données du réseau de l'UE pour y parvenir. Plus précisément, il s'agira de :
- Définir les éléments de données ISO IDMP obligatoires et facultatifs
- Définir les règles métier pour les éléments de données facultatifs
- Définir la conformité et les types de données
- Définir les modèles de gouvernance de l'UE
POSITION DES RÉGULATEURS US
- Un leadership actif pour faire avancer l'IDMP auprès des régulateurs mondiaux (anciennement ICH) et de l'ISO
AUTRES ORGANISMES DE RÉGLEMENTATION
- Suisse – Prévoit de mettre en œuvre après l'UE (suiveur rapide)
- Le Japon et le Canada ont désigné des régulateurs pour être experts au sein du groupe IG sur les substances.
CHRONOLOGIES
Guides d'application européens
- Le projet de guides de mise en œuvre a été lancé et les guides seront disponibles à partir du 1er trimestre 2016
AUTRES
- FDA encore FDA date, mais prévoit d'adapter la SPL si nécessaire
- Japon – Incertain au sein de l'ICH mais travaille désormais au sein du groupe des régulateurs et de l'ISO
- Canada – Devrait être mis en œuvre mais sans détails précis pour l'instant
- Suisse – Pas encore de mises à jour
COMPRENDRE LES EXIGENCES DE CONFORMITÉ IDMP
L'IDMP exige des informations sur les Produits médicaux sous la forme d'un ensemble d'identifiants standard, qui sont basés sur une hiérarchie d'identification créée lors de l'élaboration du Dictionnaire des Produits Médicaux EudraVigilance (EVMPD) ou de sa forme étendue (xEVMPD). Il y aura un chevauchement d'informations avec celles déposées dans les dossiers Structured Product Labeling (SPL) aux US et dans d'autres registres de produits à l'échelle mondiale.
Cependant, l'IDMP propose de nouveaux identifiants, de nouvelles catégories et de nouvelles façons d'exprimer les relations entre les éléments dans le modèle de données. L'IDMP doit être intégré à l'ADN de l'organisation, car il doit piloter la construction des modèles de données dans toute votre entreprise. L'infrastructure informatique d'une organisation peut alors le reconnaître à travers de multiples systèmes, processus métier et unités fonctionnelles comme la RA, la sécurité, la R&D, la documentation et les processus de fabrication.
DÉFIS DE CONFORMITÉ IDMP
Organisationnel
- Données distribuées entre plusieurs départements
- Un parrainage de haut niveau est nécessaire pour encourager la participation
Technique
- Découvrir, collecter et consolider, nettoyer les données
- 250 à 300 champs par produit
Coordination
- Gestion du changement continu
- Coordination entre plusieurs équipes
- Maintenir la conformité des données avec les processus internes
EN CONCLUSION :
IDMP : IMPACT SUR L'INDUSTRIE PHARMACEUTIQUE
La mise en œuvre des normes IDMP devrait avoir un impact sur la préparation et la planification des soumissions, ainsi que sur la maintenance des données à l'échelle de l'entreprise, y compris les données de fabrication et les informations structurées sur les substances jusqu'aux informations d'enregistrement.
NORME IDMP : GAINS D'EFFICACITÉ ASSURÉS LORS DE LA MISE EN ŒUVRE
S'assurer que votre organisation est prête à relever le défi IDMP nécessitera une coopération étroite entre plusieurs départements au sein de votre organisation. Un prestataire de services compétent, doté d'un portefeuille exclusif de compétences réglementaires, peut vous aider à progresser vers la conformité IDMP, ce qui peut aider une organisation à répondre aux nouvelles opportunités émergentes sur le marché.










